Aktive ingredienser: Choriogonadotropin alfa
Ovitrelle 250 mikrogram / 0,5 ml injektionsvæske, opløsning i en fyldt injektionssprøjte
Ovitrelle indlægssedler er tilgængelige til pakningsstørrelser:- Ovitrelle 250 mikrogram / 0,5 ml injektionsvæske, opløsning i en fyldt injektionssprøjte
- Ovitrelle 250 mikrogram injektionsvæske, opløsning i fyldt pen
Hvorfor bruges Ovitrelle? Hvad er det for?
Hvad er Ovitrelle
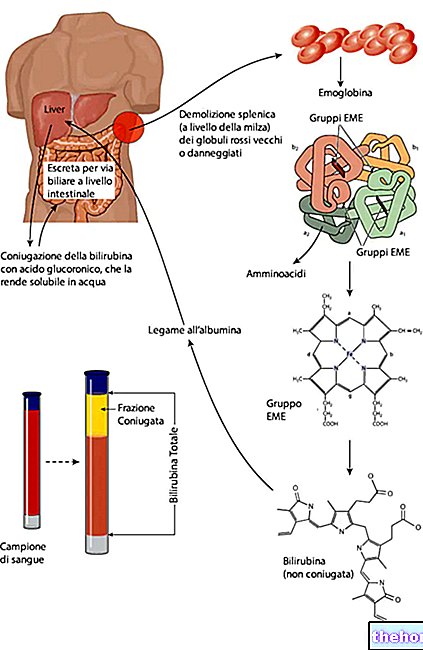
Ovitrelle indeholder et lægemiddel kaldet 'choriogonadotropin alfa', der fremstilles i et laboratorium ved hjælp af særlige rekombinante DNA -teknikker. Choriogonadotropin alfa ligner meget et hormon, der findes naturligt i menneskekroppen, choriongonadotropin, som er involveret i reproduktion og fertilitet.
Hvad er Ovitrelle til
Ovitrelle bruges sammen med anden medicin:
- at fremkalde vækst og udvikling af mange follikler (der hver indeholder en oocyt) hos kvinder, der gennemgår assisteret reproduktionsteknik (en procedure, der kan hjælpe dem med at blive gravide), såsom "in vitro -befrugtning". Andre lægemidler gives først for at fremkalde væksten af flere follikler.
- at fremkalde frigivelse af et æg fra æggestokkene (induktion af ægløsning) hos kvinder, der ikke producerer æg (en tilstand kaldet anovulation) eller som producerer for få æg (oligo-ægløsning). Andre lægemidler til vækst og udvikling gives først folliklerne.
Kontraindikationer Når Ovitrelle ikke bør bruges
Brug ikke Ovitrelle
- hvis du er allergisk over for choriogonadotropin alfa eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i afsnit 6)
- hvis du har en tumor i en del af hjernen kaldet "hypothalamus" eller "hypofyse"
- hvis du har forstørrede æggestokke eller væskelommer i æggestokkene (ovariecyster) af ukendt oprindelse
- hvis du lider af uforklarlig vaginal blødning
- hvis du har kræft i æggestokkene, livmoderen eller brystet
- hvis du har haft en graviditet uden for livmoderen (ektopisk graviditet) inden for de sidste 3 måneder
- hvis du har alvorlig betændelse i venerne eller blodpropper i venerne (aktiv tromboembolisk lidelse)
- hvis du er underlagt forhold, der normalt umuliggør normal graviditet, f.eks. overgangsalder eller for tidlig overgangsalder (ovariesvigt) eller misdannelser i kønsorganerne
Brug ikke Ovitrelle, hvis nogen af disse betingelser gælder for dig. Hvis du er i tvivl, skal du kontakte din læge, før du bruger denne medicin.
Forholdsregler ved brug Hvad du skal vide, før du tager Ovitrelle
Inden behandlingen påbegyndes, bør din og din partners fertilitet vurderes af en læge med erfaring i behandling af fertilitetsproblemer.
Ovarial hyperstimuleringssyndrom (OHSS)
Denne medicin kan øge risikoen for at udvikle OHSS. Dette opstår, når follikler vokser til og bliver til store cyster.
Hvis du har smerter i underlivet, går hurtigt op i vægt, føler dig syg eller kaster op eller har svært ved at trække vejret, må du ikke injicere Ovitrelle og straks tale med din læge (se afsnit 4.) Hvis du udvikler OHSS, kan du få at vide, at du ikke skal have køn eller at bruge en barrieremetode til prævention i mindst fire dage.
Risikoen for OHSS reduceres, når den sædvanlige dosis Ovitrelle bruges, og behandlingsforløbet overvåges nøje (f.eks. Blodmålinger af østradiolniveauer og ultralyd).
Multiple graviditeter og / eller fosterskader
Når du bruger Ovitrelle, har du en større risiko for at have en multipel graviditet, i de fleste tilfælde tvillinger, sammenlignet med naturlig befrugtning. Multiple graviditet kan føre til medicinske komplikationer for dig og dine babyer. Til assisteret reproduktionsteknik, risikoen for at have en graviditet flere gange er relateret til antallet af befrugtede embryoner eller oocytter, der overføres til det Multiple graviditeter og visse egenskaber ved parret med fertilitetsproblemer (f.eks. alder) kan også være forbundet med en øget risiko for fosterskader.
Risikoen for multipel graviditet reduceres, når den sædvanlige dosis Ovitrelle bruges, og behandlingsforløbet overvåges nøje (f.eks. Blodmålinger af østradiolniveauer og ultralyd).
Ektopiske graviditeter
Hos kvinder med beskadigede æggeleder (rørene, der fører ægget fra æggestokken til livmoderen), kan der opstå graviditet uden for livmoderen (ektopisk graviditet). Lægen skal derfor foretage en ultralydsscanning tidligt for at udelukke denne mulighed.
Abort
Når man gennemgår assisteret reproduktionsteknik eller ovariestimulering for at producere æg, er risikoen for abort større end hos andre kvinder.
Problemer med blodpropper (tromboemboliske hændelser)
Hvis du tidligere eller for nylig har haft blodpropper i benene eller lungen eller et hjerteanfald eller slagtilfælde, eller hvis dette er sket i din familie, kan der være en øget risiko for, at disse problemer opstår eller forværres ved behandling. Med Ovitrelle.
Graviditetstest
Hvis du tager en serum- eller urin -graviditetstest efter brug af Ovitrelle og i op til ti dage efter det, kan du få et falsk positivt testresultat. Spørg din læge, hvis du er i tvivl.
Børn og unge
Ovitrelle bør ikke bruges til børn og unge
Interaktioner Hvilke lægemidler eller fødevarer kan ændre effekten af Ovitrelle
Fortæl det til din læge, hvis du tager anden medicin eller har brugt det for nylig.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Brug ikke Ovitrelle, hvis du er gravid eller ammer.
Spørg din læge eller apotek til råds, før du tager medicin.
Kørsel og brug af maskiner
Ovitrelle menes ikke at påvirke evnen til at føre motorkøretøj eller betjene maskiner.
Vigtig information om nogle af ingredienserne i Ovitrelle
Dette lægemiddel indeholder mindre end 1 mmol (23 mg) natrium, dvs. det er i det væsentlige "natriumfrit"
Dosis, metode og administrationstidspunkt Sådan bruges Ovitrelle: Dosering
Brug altid dette lægemiddel nøjagtigt efter lægens anvisning. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Mængde til brug
- Den anbefalede dosis er 1 fyldt injektionssprøjte (250 mikrogram / 0,5 ml) givet som en enkelt injektion.
- Din læge vil have fortalt dig præcis, hvornår du skal injicere.
Brug af denne medicin
- Ovitrelle skal administreres subkutant, hvilket betyder ved 'injektion under huden.
- Hver fyldt injektionssprøjte er kun til engangsbrug. Må kun bruges, hvis opløsningen er klar og fri for partikler.
- Din læge eller sygeplejerske vil vise dig, hvordan du bruger Ovitrelle fyldt injektionssprøjte til at injicere medicinen.
- Injicer Ovitrelle som anvist af din læge eller sygeplejerske.
- Bortskaf den brugte nål sikkert efter injektionen.
Hvis du administrerer Ovitrelle alene, bedes du læse følgende instruktioner omhyggeligt:
- Vask hænder. Det er vigtigt, at dine hænder og det tilbehør, du bruger, er så rene som muligt.
- Saml alt hvad du har brug for. Bemærk, at alkohol-gennemblødte vatrondeller ikke er inkluderet i pakken. Find et rent område, og læg alt, hvad du har brug for: - to alkohol -gennemblødte vatrondeller - en fyldt injektionssprøjte med medicinen.
- Injektion: Indsprøjt straks opløsningen: din læge eller sygeplejerske burde allerede have rådgivet dig, hvor du skal injicere (f.eks. Mave, forside af låret). Rengør det valgte område med en alkohol-gennemblødt vatpind. Hold fast mellem fingrene i huden og indsæt injektionskanylen i en vinkel mellem 45 ° og 90 ° med en pillignende bevægelse. Injektion under huden som beskrevet.Injicer ikke direkte i en vene. Injicer opløsningen ved langsomt at trykke på sprøjtens stempel. Tag så lang tid som nødvendigt at injicere hele opløsningen. Fjern nålen med det samme, og rengør med en alkoholserviet ved hjælp af en cirkulær bevægelse.
- Bortskaffelse af brugte genstande: Når du er færdig med din injektion, skal du straks kassere den tomme sprøjte i en passende beholder.
Overdosering Hvad skal jeg gøre, hvis du har taget en overdosis Ovitrelle
Hvis du har brugt for meget Ovitrelle
Hvis der er brugt for meget Ovitrelle, kan du opleve ovariehyperstimuleringssyndrom. Kontakt straks din læge, hvis du oplever smerter i underlivet, hurtig vægtforøgelse, kvalme eller opkastning, eller hvis du har svært ved at trække vejret.
Hvis du har glemt at bruge Ovitrelle
Hvis du har glemt at bruge Ovitrelle, skal du tale med din læge, så snart du er klar over det.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Bivirkninger Hvad er bivirkningerne af Ovitrelle
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Stop med at bruge Ovitrelle og kontakt straks en læge, hvis du bemærker nogen af følgende alvorlige bivirkninger, da du muligvis har brug for akut lægehjælp:
- allergiske reaktioner såsom hurtig eller uregelmæssig puls, hævelse af tunge og hals, nysen, hvæsen eller alvorlige vejrtrækningsbesvær er meget sjældne (kan forekomme hos op til 1 ud af 10.000 mennesker);
- smerter i underlivet med kvalme eller opkastning kan være symptomer på ovariehyperstimuleringssyndrom (OHSS). Dette kan indikere, at æggestokkene overreagerer på behandling og store ovariecyster har udviklet sig (se også afsnit 2 under "Ovarial hyperstimulationssyndrom"). Dette er en almindelig forekomst (kan forekomme hos op til 1 ud af 10 personer);
- OHSS kan blive alvorlig med mærkbar forstørrelse af æggestokkene, nedsat urinproduktion, vægtøgning, vejrtrækningsbesvær og mulig ophobning af væske i maven eller brystet. Dette er usædvanligt (kan forekomme hos op til 1 ud af 100 personer);
- Alvorlige koagulationskomplikationer (tromboemboliske hændelser) uafhængigt af OHSS findes meget sjældent, hvilket kan forårsage brystsmerter, åndenød, slagtilfælde eller hjerteanfald (se også afsnit 2 under "Blodkoagulationsproblemer").
Andre bivirkninger
Almindelig (kan forekomme hos op til 1 ud af 10 personer)
- Hovedpine, træt.
- Lokale reaktioner på injektionsstedet, såsom smerter, rødme eller hævelse.
Ikke almindelig (kan forekomme hos op til 1 ud af 100 personer)
- Diarré.
- Følelse af deprimeret, irritabel eller rastløs.
- Brystsmerter.
Meget sjælden (kan forekomme hos op til 1 ud af 10.000 mennesker)
- Milde allergiske hudreaktioner såsom udslæt.
Graviditet uden for livmoderen, ovarietorsion (en sygdom, der påvirker æggestokkene) og andre komplikationer kan skyldes den assisterede reproduktionsteknik, som lægen anvender.
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, som ikke er nævnt i denne indlægsseddel. Du kan også indberette bivirkninger direkte via det nationale rapporteringssystem anført i tillæg V. Ved at rapportere bivirkninger kan du hjælpe med at give mere information om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Opbevar denne medicin utilgængeligt for børn
Brug ikke dette lægemiddel efter den udløbsdato, der står på etiketten og kartonen efter EXP. Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Opbevares i køleskab (2 ° C - 8 ° C). Opbevares i den originale emballage. Ovitrelle 250 mikrogram injektionsvæske, opløsning kan opbevares i op til 30 dage ved stuetemperatur (ikke over 25 ° C) uden at blive lagt tilbage i køleskabet, og efter denne periode på 30 dage, hvis den ikke bruges, skal den kasseres.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Sammensætning og farmaceutisk form
Ovitrelle indeholder
- Det aktive stof er choriogonadotropin alfa, produceret ved rekombinant DNA -teknologi.
- Hver fyldt injektionssprøjte indeholder 250 mikrogram / 0,5 ml (svarende til 6.500 IE).
- Øvrige indholdsstoffer er mannitol, methionin, poloxamer 188, phosphorsyre, natriumhydroxid, vand til injektionsvæsker.
Hvordan Ovitrelle ser ud og pakningens indhold
Ovitrelle leveres som injektionsvæske, opløsning. Den fås i en enkelt fyldt injektionssprøjte (pakning med 1).
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
OVITRELLE 250 MCG / 0,5 ML, LØSNING TIL INJEKTION I FØRFyldt sprøjte
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver fyldt injektionssprøjte indeholder 250 mikrogram choriogonadotropin alfa * (svarende til cirka 6.500 IE) i 0,5 ml opløsning.
* rekombinant humant choriogonadotropin, r-hCG, produceret ved hjælp af rekombinant DNA-teknologi i kinesiske hamster-ovarieceller (CHO).
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Injektionsvæske, opløsning i fyldt injektionssprøjte.
Klar farveløs eller lysegul opløsning.
Opløsningens pH er 7,0 ± 0,3, osmolaliteten er 250-400 mOsm / kg.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Ovitrelle er indiceret til behandling af:
• Voksne kvinder, der har undergået superovulation som forberedelse til assisteret reproduktionsteknik såsom in vitro -befrugtning (IVF): Ovitrelle administreres for at fremkalde den endelige follikelmodning og luteinisering efter stimulering af follikelvækst.
• Anovulatoriske eller oligo-ægløsende voksne kvinder: Ovitrelle administreres for at fremkalde ægløsning og luteinisering hos anovulatoriske eller oligo-ægløsende kvinder efter stimulering af follikelvækst.
04.2 Dosering og indgivelsesmåde
Ovitrelle -behandling bør overvåges af en læge med erfaring i behandling af fertilitetsproblemer.
Dosering
Den maksimale dosis er 250 mcg. Følgende terapeutiske skema bør anvendes:
• Kvinder, der har gennemgået superovulation som forberedelse til assisteret reproduktionsteknik såsom in vitro -befrugtning (IVF):
Administrer indholdet af en Ovitrelle fyldt injektionssprøjte (250 mcg) 24 til 48 timer efter den sidste administration af follikelstimulerende hormon (FSH) eller humant menopausal gonadotropin (HMG), efter opnåelse af optimal stimulering af follikelvækst.
• Anovulatoriske eller oligo-ægløsende kvinder:
Administrer indholdet af en Ovitrelle fyldt injektionssprøjte (250 mcg) 24 til 48 timer efter optimal stimulering af follikelvækst er opnået. Det anbefales efter optimal follikulær vækststimulering er opnået. Patienten anbefales at have samleje til formeringsformål både på dagen for Ovitrelle -injektionen og dagen efter.
Særlige populationer
Nyre- eller leverinsufficiens
Ovitrelles sikkerhed, virkning og farmakokinetik hos patienter med nedsat nyre- eller leverfunktion er ikke klarlagt.
Pædiatrisk population
Der er ingen indikation for en specifik anvendelse af Ovitrelle i den pædiatriske population.
Indgivelsesmåde
Til subkutan brug. Ovitrelle selvadministration bør kun udføres af patienter, der er tilstrækkeligt uddannede, og som kan benytte sig af ekspertrådgivning.
Ovitrelle er kun til engangsbrug.
04.3 Kontraindikationer
• Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt. 6.1.
• Tumorer i hypothalamus eller hypofysen
• Ovarieforstørrelse eller cyste skyldes ikke polycystisk ovariesyndrom
• Gynækologiske blødninger af ukendt ætiologi
• Kræft i æggestokkene, livmoderen eller brystet
• Ekstrauterin graviditet, der fandt sted inden for de foregående tre måneder
• Tromboemboliske lidelser i gang
• Primær ovariesvigt
• Misdannelser af kønsorganerne, der er uforenelige med graviditet
• Uterine fibromer uforenelige med graviditet
• Postmenopause.
04.4 Særlige advarsler og passende forholdsregler ved brug
Inden behandlingen påbegyndes, bør parrets infertilitet undersøges, og eventuelle kontraindikationer mod graviditet skal evalueres. Specielt skal patienter undersøges for hypothyroidisme, binyrebarkinsufficiens, hyperprolactinæmi og tumorer i hypofysen eller hypotalamus og skal gennemgå specifik behandling.
Der er ingen klinisk erfaring med Ovitrelle i behandlingen af andre sygdomme (såsom corpus luteum insufficiens eller mandlige sygdomme); derfor er Ovitrelle ikke indiceret til behandling af disse sygdomme.
Ovarial hyperstimulationssyndrom (Ovarial hyperstimuleringssyndrom, OHSS)
Patienter, der gennemgår ovariestimulering, har en øget risiko for at udvikle OHSS på grund af multipel follikulær udvikling.
Ovariehyperstimuleringssyndrom kan blive en alvorlig bivirkning, kendetegnet ved store ovariecyster, der let kan briste, vægtøgning, dyspnø, oliguri eller tilstedeværelse af ascites inden for et klinisk billede af kredsløbsdysfunktion. I sjældne tilfælde kan alvorlig OHSS kompliceres af hæmoperitoneum , akut åndedrætsbesvær, ovarietorsion og tromboemboli.
For at minimere risikoen for OHSS anbefales ultralydsovervågning af follikulær udvikling og / eller bestemmelse af serumøstradiolniveauer før og med regelmæssige intervaller under behandlingen. Ved anovulation øges risikoen for OHSS i nærvær af serum -østradiolniveauer> 1.500 pg / ml (5.400 pmol / L) og mere end 3 follikler med en diameter på 14 mm eller derover. Ved assisteret reproduktionsteknik er risikoen af OHSS stiger med serumøstradiolniveauer> 3.000 pg / ml (11.000 pmol / L) og 18 eller flere follikler med en diameter større end eller lig med 11 mm.
OHSS på grund af overdreven ovarierespons kan undgås ved at afbryde hCG -administration. Derfor i nærvær af tegn på ovariehyperstimulering, såsom serumøstradiolniveauer> 5.500 pg / ml (20.000 pmol / L) og / eller i nærvær af 30 eller flere follikler i alt, anbefales det, at hCG -administrationen suspenderes, og patienten rådes til at afstå fra samleje eller at bruge præventionsmetoder i mindst 4 dage.
Multiple graviditeter
Hos patienter, der gennemgår ægløsning, er forekomsten af flere graviditeter og fødsler (hovedsageligt tvillinger) højere end ved naturlig befrugtning. Risikoen for flere graviditeter efter assisteret reproduktionsteknikker er relateret til antallet af overførte embryoner.
Overholdelse af den anbefalede Ovitrelle -dosis, administrationsregime og omhyggelig overvågning af behandlingen vil minimere risikoen for OHSS og multipel graviditet.
Abort
Abortraten, både hos anovulatoriske patienter og hos kvinder, der gennemgår assisteret reproduktionsteknik, er højere end den, der findes i den normale befolkning, men kan sammenlignes med den frekvens, der observeres hos kvinder med andre infertilitetsproblemer.
Ektopiske graviditeter
Siden ufrugtbare kvinder, der gennemgår assisteret reproduktionsteknik (Assisteret reproduktionsteknologi, ART) og især IVF ofte har tubale anomalier, forekomsten af ektopiske graviditeter kan være højere. Det er vigtigt at bekræfte tidligt ved ultralyd, at graviditeten er intrauterin og at udelukke, at det er ekstrauterin.
Medfødte misdannelser
Forekomsten af medfødte misdannelser efter ART kan være lidt højere end ved naturlig befrugtning.Det menes at skyldes forældrekarakteristika (f.eks. Moderens alder, sædkarakteristika) og den højere forekomst af flere graviditeter.
Tromboemboliske begivenheder
Hos kvinder med nylig eller igangværende tromboembolisk sygdom eller hos kvinder med generelt anerkendte risikofaktorer for tromboemboliske hændelser, såsom personlig eller familiehistorie, kan behandling med gonadotropiner yderligere øge risikoen for forværring eller forekomst af disse hændelser. Kvinder, fordelene ved gonadotropin administration skal afvejes mod risiciene. Det skal dog bemærkes, at selve graviditeten samt OHSS medfører en øget risiko for tromboemboliske hændelser, såsom lungeemboli, iskæmisk slagtilfælde eller myokardieinfarkt.
Interferens med serologiske eller urintest
Efter administration kan Ovitrelle interferere med immunanalysen til bestemmelse af serum eller urin -hCG i op til 10 dage efter administration, hvilket kan resultere i en falsk positiv graviditetstest.
Patienter bør gøres opmærksom på denne risiko.
Andre oplysninger
Mild stimulering af skjoldbruskkirtlen af ukendt klinisk relevans er mulig under behandling med Ovitrelle.
Dette lægemiddel indeholder mindre end 1 mmol (23 mg) natrium pr. Dosis, dvs. det er i det væsentlige "natriumfrit".
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Der er ikke udført specifikke interaktionsundersøgelser mellem Ovitrelle og andre lægemidler, men der er ikke rapporteret signifikante interaktioner med andre lægemidler under hCG -terapi.
04.6 Graviditet og amning
Graviditet
Der er ingen indikationer for brug af Ovitrelle under graviditet Der foreligger ingen kliniske data om eksponerede graviditeter Der er ikke udført reproduktionsundersøgelser med dyr med choriogonadotropin alfa (se pkt. 5.3). Den potentielle risiko for mennesker er ikke kendt.
Fodringstid
Ovitrelle er ikke indiceret under amning Der er ingen data om udskillelse af choriogonadotropin alfa i mælk.
Fertilitet
Anvendelse af Ovitrelle er indiceret til behandling af infertilitet (se afsnit 4.1).
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Ovitrelle menes ikke at påvirke eller ubetydeligt påvirke evnen til at føre motorkøretøj eller betjene maskiner.
04.8 Bivirkninger
Resumé af sikkerhedsprofilen
I sammenlignende kliniske undersøgelser med forskellige styrker af Ovitrelle blev følgende bivirkninger forbundet med Ovitrelle påvist på en dosisafhængig måde: OHSS, opkastning og kvalme. OHSS blev observeret hos ca. 4% af patienterne behandlet med Ovitrelle. Alvorlig OHSS blev rapporteret hos mindre end 0,5% af patienterne (se pkt. 4.4).
Liste over bivirkninger
Følgende definitioner gælder for den nedenfor anvendte frekvensterminologi: meget almindelig (≥1 / 10), almindelig (≥1 / 100,
Forstyrrelser i immunsystemet
Meget sjælden: milde eller alvorlige overfølsomhedsreaktioner, herunder anafylaktiske reaktioner og anafylaktisk chok
Psykiatriske lidelser
Ikke almindelig: depression, irritabilitet, rastløshed
Nervesystemet lidelser
Almindelig: hovedpine
Vaskulære patologier
Meget sjælden: tromboemboli, normalt forbundet med alvorlig OHSS
Gastrointestinale lidelser
Almindelig: opkastning, kvalme, mavesmerter
Ikke almindelig: diarré
Hud og subkutan væv
Meget sjælden: Milde reversible hudreaktioner, der manifesterer sig som udslæt
Sygdomme i reproduktive system og bryst
Almindelig: Mild eller moderat OHSS
Ikke almindelig: alvorlig OHSS, brystsmerter
Generelle lidelser og tilstande på administrationsstedet
Almindelig: træthed, reaktion på injektionsstedet.
Ektopisk graviditet, ovarietorsion og andre komplikationer er blevet rapporteret hos patienter efter hCG -administration. Disse menes at være samtidige virkninger relateret til assisteret reproduktionsteknik.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør kontinuerlig overvågning af lægemidlets fordel / risiko -balance.Professionelle sundhedspersoner anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. I "bilag V .
04.9 Overdosering
Virkningerne af en overdosis Ovitrelle kendes ikke.Det er imidlertid muligt, at en overdosis af Ovitrelle inducerer OHSS (se pkt. 4.4).
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: kønshormoner og modulatorer i kønssystemet, gonadotropiner.
ATC -kode: G03GA08.
Handlingsmekanisme
Ovitrelle er en choriogonadotropin alfa -medicin fremstillet ved rekombinant DNA -teknik. Det deler den samme aminosyresekvens som urin -hCG. Choriongonadotropin binder på theca (og granulosa) ovarieceller til en transmembranreceptor, som den deler med luteiniseringshormonet: LH / CG -receptoren.
Farmakodynamiske virkninger
Den vigtigste farmakodynamiske aktivitet hos kvinder består i genoptagelse af oocytmeiose, i brud på folliklen (ægløsning), i dannelsen af corpus luteum og i produktionen af progesteron og østradiol af corpus luteum.
Hos kvinder fungerer choriongonadotropin som en surrogat for det luteiniserende hormonstop, der inducerer ægløsning.
Ovitrelle bruges til at fremkalde endelig follikulær modning og tidlig luteinisering efter brug af lægemidler, der stimulerer follikelvækst.
Klinisk effekt og sikkerhed
I sammenlignende kliniske undersøgelser var administrationen af en dosis på 250 mcg Ovitrelle lige så effektiv ved 5.000 IE og 10.000 IU urin -hCG til at inducere endelig follikulær modning og tidlig luteinisering under assisteret reproduktionsteknik og lige så effektiv ved 5.000 UI af urin -hCG i induktion af ægløsning.
Til dato er der ingen indikationer på udviklingen af antistoffer mod Ovitrelle hos mennesker. Gentagen eksponering for Ovitrelle er kun undersøgt hos mandlige patienter.Kvinder har klinisk undersøgelse af indikationerne: assisteret reproduktionsteknik (ART) og anovulation været begrænset til ét behandlingsforløb.
05.2 "Farmakokinetiske egenskaber
Efter intravenøs administration distribueres choriogonadotropin alfa til det ekstracellulære væskekammer med en fordelingshalveringstid på cirka 4,5 timer. Distributionsvolumen ved steady-state og total clearance er henholdsvis 6 l og 0,2 l / t. Der er ingen indikationer på en anden metabolisme og udskillelse af choriogonadotropin alfa sammenlignet med endogent hCG.
Efter subkutan administration elimineres choriogonadotropin alfa fra kroppen med en terminal halveringstid på cirka 30 timer, den absolutte biotilgængelighed er cirka 40%.
En sammenlignende undersøgelse viste bioækvivalensen mellem lyofilisatformuleringen og den flydende formulering.
05.3 Prækliniske sikkerhedsdata
Ikke-kliniske data afslører ingen særlig fare for mennesker baseret på konventionelle undersøgelser af sikkerhedsfarmakologi, toksicitet og gentoksicitet ved gentagne doser. Undersøgelser af kræftfremkaldende potentiale er ikke blevet udført. Dette er berettiget i betragtning af det aktive stofs proteinkarakter og de negative resultater af gentoksicitetstest.
Dyrets reproduktionsundersøgelser er ikke udført.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Mannitol
Methionin
Poloxamer 188
Fosforsyre (til pH -justering)
Natriumhydroxid (til pH -justering)
Vand til injektionsvæsker
06.2 Uforenelighed
I mangel af kompatibilitetsundersøgelser må dette lægemiddel ikke blandes med andre lægemidler.
06.3 Gyldighedsperiode
2 år.
Lægemidlet skal bruges umiddelbart efter åbning, men der er påvist stabilitet i 24 timer ved temperaturer mellem 2 ° C og 8 ° C.
06.4 Særlige opbevaringsforhold
Opbevares i køleskab (2 ° C - 8 ° C). Opbevares i den originale emballage. I produktets holdbarhed kan opløsningen opbevares i 30 dage ved en temperatur på højst 25 ° C uden at blive lagt i køleskabet igen. I dette tilfælde, efter denne periode på 30 dage, skal opløsningen, hvis den ikke bruges, smides væk.
06.5 Den umiddelbare emballages art og emballagens indhold
Forfyldt sprøjte (glas af type I) indeholdende 0,5 ml opløsning, med stempelprop (halobutylgummi), stempel (plast) og injektionsnål (rustfrit) - pakning med 1.
06.6 Brugsanvisning og håndtering
Opløsningen bør ikke administreres, hvis den indeholder partikler eller ikke er klar. Kun til engangsbrug.
Ovitrelle selvadministration bør kun udføres af patienter, der er tilstrækkeligt uddannede, og som kan benytte sig af ekspertrådgivning.
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Merck Serono Europe Limited
56, Marsh Wall London E14 9TP Storbritannien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/00/165/007
035188073
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 2. februar 2001
Dato for seneste fornyelse: 2. februar 2006
10.0 DATO FOR REVISION AF TEKSTEN
D.CCE maj 2015