Aktive ingredienser: Colistin (Sodium colistimethate)
Colimycin 1.000.000 IE / 4 ml pulver og solvens til injektions- eller infusionsvæske, opløsning
Hvorfor bruges Colimycin? Hvad er det for?
Colimycin indeholder natriumcolistimethat.
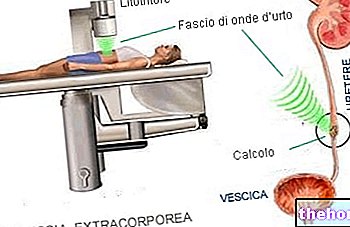
Colimycin gives som injektion til behandling af nogle typer alvorlige infektioner forårsaget af visse bakterier. Colimycin bruges, når andre antibiotika ikke er egnede.
Kontraindikationer Når Colimycin ikke bør bruges
Brug ikke Colimycin
- hvis du er allergisk (overfølsom) over for natriumcolistimethat, colistin eller andre polymyxiner
- hvis du er gravid (se afsnittet "Graviditet og amning")
- hvis du ammer (se afsnittet "Graviditet og amning")
Forholdsregler ved brug Hvad du skal vide, før du tager Colimycin
Tal med din læge, apotek eller sygeplejerske, før du bruger Colimycin:
- hvis du har eller har haft nyreproblemer
- hvis du lider af myasthenia gravis
- hvis du lider af porfyri
Hos for tidligt fødte og nyfødte bør der udvises særlig forsigtighed ved brug af Colimycin, fordi nyrerne endnu ikke er fuldt udviklede.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Colimycin
Fortæl det til din læge eller apotek, hvis du tager anden medicin eller har brugt det for nylig.
Det er især vigtigt, at du kontakter din læge, hvis du er:
- medicin, der kan påvirke nyrefunktionen. Hvis du tager denne type medicin samtidig med Colimycin, kan risikoen for nyreskader stige.
- medicin, der kan påvirke nervesystemet. Hvis du tager denne type medicin samtidig med Colimycin, kan risikoen for bivirkninger, der påvirker nervesystemet, øges.
- medicin kaldet muskelafslappende midler, ofte brugt under generel anæstesi. Colimycin kan forstærke virkningerne af disse lægemidler. Hvis du får generel bedøvelse, bedes du fortælle din anæstesilæge om din brug af Colimycin.
Hvis du har myasthenia gravis og også tager andre antibiotika kaldet makrolider (f.eks. Azithromycin, clarithromycin eller erythromycin) eller antibiotika kaldet fluoroquinoloner (f.eks. Ofloxacin, norfloxacin og ciprofloxacin), øger kolimycin yderligere risikoen for muskelsvaghed og vejrtrækningsbesvær.
Hvis du får natriumcolistimethat på samme tid som infusion og inhalation, kan risikoen for bivirkninger stige.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Hvis du er gravid eller ammer, tror at du er gravid eller planlægger at blive gravid, skal du spørge din læge til råds, før du bruger denne medicin.
Colimycin må ikke bruges under graviditet eller hvis du ammer (se afsnittet "Brug ikke Colimycin").
Kørsel og brug af maskiner
Under behandling med Colimycin kan der opstå lidelser i nervesystemet som prikken omkring munden, prikken i ekstremiteterne, kløe og svimmelhed. Hvis dette sker, må du ikke køre bil eller bruge værktøj eller maskiner.
Dosis, metode og administrationstidspunkt Sådan bruges Colimycin: Dosering
Colimycin gives af din læge som en infusion i en vene, der varer 30 til 60 minutter.
Ved behandling af bakterielle infektioner er det vigtigt at fuldføre hele behandlingsforløbet.Lægen vil beslutte, hvordan og hvor længe han skal give dig Colimycin.
Den sædvanlige daglige dosis for voksne er 9 millioner enheder, opdelt i to eller tre doser. Hvis du er ret syg, får du en dosis større end 9 millioner enheder én gang i starten af behandlingen.
I nogle tilfælde kan din læge beslutte at give dig en højere daglig dosis, op til maksimalt 12 millioner enheder.
Den sædvanlige daglige dosis for børn, der vejer op til 40 kg, er 75.000-150.000 enheder pr. Kg legemsvægt, opdelt i tre doser.
Der er lejlighedsvis blevet givet højere doser ved cystisk fibrose.
Børn og voksne med nyreproblemer, selv ved dialyse, får normalt lavere doser. Din læge vil kontrollere din nyrefunktion regelmæssigt, mens du får Colimycin.
Overdosering Hvad skal man gøre, hvis man har taget en overdosis Colimycin
Hvis du har brugt for meget Colimycin
Da Colimycin vil blive givet til dig af en læge, er det usandsynligt, at du får en forkert dosis. Spørg din læge eller sygeplejerske, hvis du har spørgsmål om mængden af denne medicin, du skal have: Symptomer på at tage for meget colimycin omfatter:
- sløvhed (søvnighed);
- forvirring (psykisk lidelse);
- psykose (alvorlig ændring af den psykiske balance);
- svimmelhed (ustabilitet)
- ataksi (manglende evne til at stå oprejst)
- ansigtsparæstesi (ændret følsomhed i ansigtet);
- nystagmus (hurtige og ukontrollerede bevægelser af øjnene);
- vanskeligheder med at tale;
- alvorlige nyresygdomme såsom kraftigt fald i urinmængde og stigninger i nitrogen og kreatinin i blodet
- muskelsvaghed;
- apnø (åndedrætsbesvær).
Hvis du har glemt at bruge Colimycin
Hvis du tror, du har glemt en dosis Colimycin, skal du fortælle det til din læge eller apotek eller sygeplejerske.
Hvis du holder op med at bruge Colimycin
Din læge vil beslutte, hvor længe du får Colimycin. Det er vigtigt, at du afslutter din behandling som anbefalet af din læge, ellers kan dine symptomer blive værre.
Spørg din læge, apotek eller sygeplejerske, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Bivirkninger Hvad er bivirkningerne af Colimycin
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Nogle bivirkninger kan være alvorlige
Fortæl det straks til din læge eller sygeplejerske, hvis du bemærker et af følgende symptomer:
- hvæsen eller vejrtrækningsbesvær, som kan føre til sammenbrud, udslæt, kløe eller nældefeber på huden. Disse kan være tegn på en alvorlig allergisk reaktion;
- diarré. Det kan være et symptom på en alvorlig tarminfektion.
Følgende bivirkninger er også blevet rapporteret:
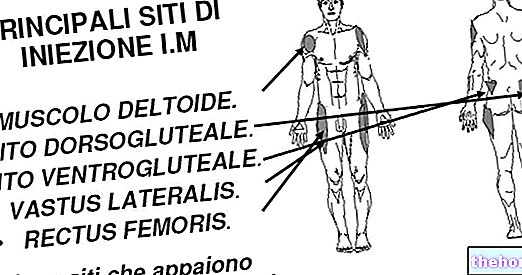
- Reaktion på injektionsstedet;
- Nyreproblemer som nyresvigt, nyretoksicitet, øget nitrogen og kreatinin i blodet, nedsat urinmængde Disse effekter er mere sandsynlige hos patienter, der allerede har nedsat nyrefunktion, eller som får Colimycin samtidig med andre lægemidler, der påvirker nyre eller gives i en for høj dosis.Disse problemer forbedres normalt, når behandlingen stoppes, eller dosis af Colimycin reduceres.
- Neurologiske problemer såsom manglende evne til at trække vejret på grund af lammelse af brystmusklerne, følelsesløshed eller prikken (især omkring ansigtet), svimmelhed eller tab af balance, ændringer i blodtryk eller blodgennemstrømning (som omfatter svaghed og rødmen), vanskeligheder med at tale. Bivirkninger, der påvirker nervesystemet, er mere tilbøjelige til at forekomme, når dosen af Colimycin er for høj, hos mennesker, der har nedsat nyrefunktion eller hos dem, der også får muskelafslappende medicin eller andre lægemidler, der har en lignende virkning ved at virke på nervesystemet system.
- Forvirring og psykiske problemer (herunder tab af virkelighedsfornemmelse)
- Visuelle problemer
- svimmelhed
- Feber.
- Mave -tarmkanalen: diarré.
Indberetning af bivirkninger
Tal med din læge eller apotek eller sygeplejerske, hvis du får bivirkninger. Dette omfatter eventuelle bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også rapportere bivirkninger direkte.: Https://www.aifa.gov.it/content /segnalazioni-reazioni-avverse
Ved at rapportere bivirkninger kan du hjælpe med at give flere oplysninger om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Opbevar denne medicin utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen og flasken efter: EXP. Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Må ikke opbevares over 25 ° C.
Pulveret i hætteglasset må kun opløses på tidspunktet for brug med den fysiologiske opløsning i hætteglasset indeholdt i pakningen.
Under denne operation er det muligt at opfange variationer i det tryk, der skal udøves på sprøjtens stempel for at indføre opløsningsmidlet i hætteglasset med pulveret. Disse forskelle, som kan ses mellem forskellige pakninger med Colimycin, er ikke i sig selv en indikation af en defekt i lægemidlets kvalitet.
Hvert rekonstitueret hætteglas med Colimycin injektions- eller infusionsvæske, opløsning er kun til engangsbrug. Eventuel resterende ubrugt opløsning skal smides (engangsbrug).
Efter rekonstituering skal Colimycin anvendes straks.
Den rekonstituerede opløsning bør kun bruges, hvis den er klar og fri for partikler.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Colimycin indeholder
- Den aktive ingrediens er natriumcolistimethat
- De øvrige ingredienser i opløsningsmiddelampullen er natriumchlorid og vand til injektionsvæsker.
Beskrivelse af hvordan Colimycin ser ud og pakningens indhold
I hver pakke Colimycin er der et hætteglas, der indeholder den aktive ingrediens i pulver, og et hætteglas, der indeholder opløsningsmidlet (fysiologisk natriumchloridopløsning og vand til injektionsvæsker).
Colimycin pulver er hvidt. Opløsningsmidlet er en klar og farveløs opløsning.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
COLIMYCINE 1.000.000 IE / 4 ml pulver og opløsningsmiddel til opløsning til injektion eller til infusion
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hvert hætteglas indeholder: natriumcolistimethat 1.000.000 IE.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Pulver og solvens til injektions- eller infusionsvæske, opløsning.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Colimycin er indiceret til voksne og børn, herunder nyfødte, til behandling af alvorlige infektioner på grund af visse gramnegative patogener hos patienter, for hvilke behandlingsmulighederne er begrænsede (se pkt. 4.2, 4.4, 4.8 og 5.1).
Vær opmærksom på de officielle retningslinjer for korrekt brug af antibakterielle midler.
04.2 Dosering og indgivelsesmåde
Den dosis, der skal administreres, og behandlingsvarigheden bør fastlægges under hensyntagen til infektionens sværhedsgrad og det kliniske respons. De terapeutiske retningslinjer skal følges.
Dosen udtrykkes i internationale enheder (IE) natriumcolistimethat (CMS). I slutningen af afsnittet er der en konverteringstabel fra IE til mg CMS og til mg basistaktivitet af colistin (colistinbaseaktivitet, CBA).
Dosering
Følgende doseringsanbefalinger er baseret på begrænsede populationsfarmakokinetiske data om kritisk syge patienter (se pkt.4.4):
Voksne og unge
Vedligeholdelsesdosis: 9 MIU / dag fordelt på 2-3 doser.
Hos kritisk syge patienter bør der indgives en ladningsdosis på 9 MIU.
Det mest passende interval til den første vedligeholdelsesdosis er ikke fastlagt.
Modeller tyder på, at belastnings- og vedligeholdelsesdoser på op til 12 MIU kan være påkrævet hos patienter med god nyrefunktion i nogle tilfælde. Den kliniske erfaring med disse doser er imidlertid yderst begrænset, og sikkerheden er ikke fastslået.
Indlæsningsdosis er gældende for patienter med normal eller nedsat nyrefunktion, herunder patienter, der gennemgår nyreerstatningsterapi.
Nedsat nyrefunktion
Dosis bør justeres i tilfælde af nedsat nyrefunktion, men de farmakokinetiske data, der er tilgængelige for patienter med nedsat nyrefunktion, er meget begrænsede.
Følgende dosisændringer er angivet til vejledning.
En dosisreduktion anbefales til patienter med kreatininclearance
to daglige administrationer anbefales.
MIU = million IE
Hæmodialyse og kontinuerlig hæmo (dia) filtrering
Colistin virker dialyserbar ved konventionelle metoder til hæmodialyse og kontinuerlig veno-venøs hæmo (dia) filtrering (kontinuerlig venovenøs hæmo (dia) filtrering, CVVHF, CVVHDF). Ekstremt begrænsede data er tilgængelige fra farmakokinetiske populationsundersøgelser hos et meget lille antal patienter, der gennemgår nyreerstatningsterapi. Ingen endelige doseringsanbefalinger kan fremsættes. Følgende terapeutiske behandlinger kan overvejes.
Hæmodialyse
Dage uden hæmodialyse: 2,25 MIU / dag (2,2-2,3 MIU / dag).
Hæmodialysedage: 3 MIU / dag på hæmodialysedage, der skal administreres efter hæmodialysesessionen.
To daglige administrationer anbefales.
CVVHF / CVVHDF
Som hos patienter med normal nyrefunktion. Tre daglige administrationer anbefales.
Nedsat leverfunktion
Der foreligger ingen data om patienter med nedsat leverfunktion. Der udvises forsigtighed ved administration af natriumcolistimethat til disse patienter.
Ældre borgere
Ingen dosisjusteringer anses for nødvendige hos ældre patienter med normal nyrefunktion.
Pædiatrisk population
Data til støtte for doseringsregimet hos pædiatriske patienter er meget begrænsede. Der bør tages hensyn til nyrefunktion ved bestemmelse af dosis. Dosis bør baseres på vægten af den magre kropsmasse.
Børn ≤40 kg
75.000-150.000 IE / kg / dag fordelt på 3 doser.
For børn, der vejer mere end 40 kg, bør de anbefalinger, der gælder for voksne, overvejes.
Anvendelse af doser> 150.000 IE / kg / dag til børn med cystisk fibrose er blevet rapporteret.
Der er ingen data tilgængelige om brug eller omfang af indlæsning af doser til kritisk syge børn.
Der er ikke blevet anbefalet dosering til børn med nedsat nyrefunktion.
Intratekal og intraventrikulær administration
Baseret på begrænsede data anbefales følgende dosis til voksne:
Intraventrikulær rute
125.000 IE / dag
Doser administreret intratekalt bør ikke overstige de anbefalede til intraventrikulær brug.
Der kan ikke fremsættes specifikke doseringsanbefalinger for intratekale og intraventrikulære indgivelsesveje til børn.
Indgivelsesmåde
Administrer colimycin intravenøst ved langsom infusion, der varer 30-60 minutter.
I vandig opløsning hydrolyseres natriumcolistimethat til den aktive ingrediens colistin. Til forberedelse af dosis, især når den består af indholdet i flere hætteglas, skal den nødvendige dosis rekonstitueres under absolut asepsis (se afsnit 6.6).
Konverteringstabel
I EU bør dosis af natriumcolistimethat (CMS) kun ordineres og administreres i internationale enheder (IE). Etiketten viser antallet af IE pr. Hætteglas.
Tidligere har der været forvekslings- og administrationsfejl på grund af brugen af forskellige dosisenheder med hensyn til styrke. I USA og andre dele af verden udtrykkes dosis i milligram basiskolistinaktivitet (milligram colistinbaseaktivitet, mg CBA).
Følgende konverteringstabel er vejledende, og værdierne skal kun betragtes som nominelle og omtrentlige.
Konverteringstabel for CMS
* Nominel styrke af lægemiddelstoffet = 12.500 IE / mg
04.3 Kontraindikationer
Overfølsomhed over for colistin og over for andre antibiotika fra polymyxinfamilien eller over for et af hjælpestofferne anført i pkt.6.1.
Graviditet og amning (se afsnit 4.6).
04.4 Særlige advarsler og passende forholdsregler ved brug
Når det er muligt, bør samtidig administration af intravenøst natriumcolistimethat og et andet antibakterielt middel overvejes under hensyntagen til den resterende følsomhed for det patogen eller de patogener, der behandles. Da udviklingen af resistens over for intravenøs colistin er blevet rapporteret, især når den bruges alene, bør co-administration med andre antibakterielle midler også overvejes for at forhindre udvikling af resistens.
Der er kun begrænsede kliniske data om effekt og sikkerhed af intravenøst administreret natriumcolistimethat tilgængelige. De anbefalede doser i alle delpopulationer er også baseret på begrænsede data (klinisk og farmakokinetisk / farmakodynamisk). Især er der sikkerhedsdata tilgængelige. Begrænset til brug af høje doser (> 6 mio. IU / dag), til brug af en ladningsdosis og til særlige populationer (patienter med nedsat nyrefunktion og pædiatrisk population) Natriumcolistimethat bør kun anvendes, når andre antibiotika, der oftest ordineres, er ineffektive eller uegnede.
Overvågning af nyrefunktionen bør udføres hos alle patienter ved behandlingsstart og med jævne mellemrum under behandlingen. Dosen natriumcolistimethat bør justeres i henhold til kreatininclearance (se pkt. 4.2) Hypovolæmiske og hypovolæmiske patienter, der modtager andre potentielt nefrotoksiske lægemidler, har en øget risiko for nefrotoksicitet på grund af colistin (se afsnit 4.5 og 4.8) I nogle undersøgelser var nefrotoksicitet forbundet med kumulativ dosis og behandlingsvarighed Fordelen ved langvarig behandling skal afvejes i forhold til den potentielle øgede risiko for nyretoksicitet.
Der udvises forsigtighed, når natriumcolistimethat administreres til spædbørn under 1 år, da nyrefunktionen ikke har nået fuld modenhed i denne aldersgruppe.Derudover er virkningen af umoden nyre- og metabolisk funktion ikke kendt på omdannelsen af natriumcolistimethat til colistin.
I tilfælde af en allergisk reaktion skal behandlingen med natriumcolistimethat afbrydes, og der skal træffes passende foranstaltninger.
Forhøjede serumkoncentrationer af natriumcolistimethat, som kan skyldes overdosering eller glemt dosisreduktion hos patienter med nedsat nyrefunktion, er blevet observeret for at forårsage neurotoksiske virkninger såsom ansigtsparæstesi, muskelsvaghed, svimmelhed, sløret tale, vasomotorisk ustabilitet, synsforstyrrelser, forvirring , psykose og apnø (se afsnit 4.7). Åndedrætsassistance er påkrævet, indtil blodniveauerne er reduceret. Terapien kan genoptages, hvis der er en livstruende situation for patienten, ved lavere doser. De subjektive symptomer, som den voksne rapporterer, manifesteres muligvis ikke hos børn. Mindre, så deres nyrefunktion skal overvåges.
Patienter bør overvåges for perioral paræstesi og ekstremitetsparæstesi, som er tegn på overdosering (se pkt. 4.9).
Natriumcolistimethat er kendt for at reducere presynaptisk frigivelse af acetylcholin ved det neuromuskulære kryds og skal bruges med største forsigtighed og kun hvis det er klart nødvendigt for patienter med myasthenia gravis.
Tilfælde af åndedrætsstop er blevet rapporteret efter intramuskulær administration af natriumcolistimethat. Nedsat nyrefunktion øger sandsynligheden for apnø og neuromuskulær blokering efter administration af natriumcolistimethat.
Natriumcolistimethat bør anvendes med ekstrem forsigtighed hos patienter med porfyri.
Antibiotika-associeret colitis og pseudomembranøs colitis er blevet rapporteret med næsten alle antibakterielle midler og kan også forekomme med natriumcolistimethat. Deres sværhedsgrad kan variere fra mild til livstruende. Det er vigtigt at overveje denne diagnose hos patienter, der udvikler diarré under eller efter brug af natriumcolistimethat (se pkt. 4.8) Afbrydelse af behandlingen og påbegyndelse af specifik behandling bør overvejes. Clostridium difficile. Lægemidler, der hæmmer peristaltik, bør ikke gives.
Intravenøst administreret natriumcolistimethat krydser ikke blod -hjerne -barrieren i et klinisk relevant omfang. Intratekal eller intraventrikulær administration af natriumcolistimethat til behandling af meningitis er ikke blevet systematisk evalueret i kliniske undersøgelser og understøttes kun af individuelle sagsrapporter. Dataene til støtte for doseringen er meget begrænsede. Den mest almindeligt observerede bivirkning efter administration af CMS var aseptisk meningitis (se pkt. 4.8).
Under systemisk behandling anbefales det, at plasmakoncentrationer overvåges hos nyfødte, patienter med nyreinsufficiens og patienter med cystisk fibrose.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
I tilfælde af samtidig brug af intravenøst natriumcolistimethat med andre potentielt nefrotoksiske eller neurotoksiske lægemidler (f.eks. Følgende antibiotika: kanamycin, neomycin, streptomycin, gentamicin, tobramycin) skal der udvises ekstrem forsigtighed.
Visse antibiotika, såsom aminoglycosider og andre polymyxiner, er blevet rapporteret at forstyrre nervetransmission ved det neuromuskulære kryds.
Aminoglycosider og polymyxiner kan ikke administreres sammen med colimycin parenteralt, medmindre det er under strengt lægeligt tilsyn.
Der bør udvises forsigtighed i tilfælde af samtidig brug med andre farmaceutiske former for natriumcolistimethat, da erfaring er begrænset, og der er risiko for kumulativ toksicitet.
Der er ikke udført interaktionsundersøgelser in vivo. Mekanismen for omdannelse af natriumcolistimethat til den aktive ingrediens colistin er ikke karakteriseret. Mekanismen for colistin -clearance, herunder nyreprocesser, er også ukendt. Hverken natriumcolistimethat eller colistin inducerede aktiviteten af nogen af de analyserede P450 (CYP) enzymer (CYP1A2, 2B6, 2C8, 2C9, 2C19 og 3A4 / 5) i undersøgelser in vitro på humane hepatocytter.
Potentielle lægemiddelinteraktioner bør tages i betragtning ved samtidig administration af Colimycin med lægemidler, der vides at hæmme eller fremkalde enzymer, der er ansvarlige for lægemiddelmetabolisme, eller som er substrater for renaltransportmekanismer.
På grund af colistins virkninger på acetylcholinfrigivelse bør ikke-depolariserende muskelafslappende midler anvendes med forsigtighed hos patienter, der får natriumcolistimethat, da deres virkning kan være forlænget (se pkt. 4.4).
Samtidig behandling med natriumcolistimethat og makrolider såsom azithromycin og clarithromycin eller fluorquinoloner som norfloxacin og ciprofloxacin bør udføres med forsigtighed hos patienter med myasthenia gravis (se pkt. 4.4).
04.6 Graviditet og amning
Anvendelse af lægemidlet er kontraindiceret i tilfælde af graviditet og under amning (se afsnit 4.3).
I anden og tredje trimester af graviditeten er der risiko for mulig fostertoksicitet.Colistin er til stede i mælk, men absorberes dårligt fra tarmen.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Neurologiske lidelser kan forekomme under behandlingen (se pkt. 4.4). Patienter bør rådes til ikke at køre bil eller betjene maskiner, hvis disse effekter opstår.
04.8 Bivirkninger
Følgende bivirkninger er blevet rapporteret:
Forstyrrelser i immunsystemet: overfølsomhedsreaktioner såsom udslæt og angioødem.
Psykiatriske lidelser: forvirring, psykose.
Nervesystemet lidelser: neurotoksiske virkninger, paræstesi, svimmelhed, prikken i ekstremiteterne og tungen, sjældent taleforstyrrelser og ubalance i det autonome nervesystem. Neuromuskulær blokering ved overdosering eller kombination med helbredende midler eller ved utilstrækkelig renal eliminering.
Øjenlidelser: synsforstyrrelser.
Øre- og labyrintforstyrrelser: svimmelhed.
Åndedræts-, thorax- og mediastinumforstyrrelser: åndedrætsbesvær op til insufficiens, apnø.
Gastrointestinale lidelser: diarré (se pkt. 4.4).
Hud og subkutan væv: generaliseret kløe, nældefeber, udslæt.
Nyre- og urinlidelser: nyresvigt, nedsat nyrefunktion påvist af øget kreatinin og / eller urinstof i blodet og / eller nedsat nyreclearance af kreatinin.
Generelle lidelser og tilstande på administrationsstedet: feber, reaktion på injektionsstedet.
Diagnostiske tests: nedsat urinproduktion, nedsat kreatininclearance.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets nytte- / risikobalance. Sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Italian Medicines Agency , websted: www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Symptomer på overdosering kan observeres hos patienter med nedsat nyrefunktion. Doser højere end de maksimale kan forårsage akut nyresvigt, som manifesterer sig med oliguri, azotæmi, hypercreatininæmi, normalt reversibel ved at afbryde behandlingen.
Forhøjede serumkoncentrationer af natriumcolistimethat, som kan skyldes overdosering eller glemt dosisreduktion hos patienter med nedsat nyrefunktion, er blevet observeret for at forårsage neurotoksiske virkninger såsom sløvhed, ataksi, paræstesi i ansigtet, muskelsvaghed, svimmelhed, talevanskeligheder, vasomotorisk ustabilitet, synsforstyrrelser, forvirring, psykose.
Apnø kan også forekomme som et resultat af hvilket åndedrætsstop og død kan forekomme.
Patienter bør overvåges for perioral paræstesi og ekstremitetsparæstesi, som er tegn på overdosering (se pkt. 4.4). I tilfælde af overdosering bør behandlingen med natriumcolistimethat afbrydes, og passende støttende foranstaltninger skal anvendes.
Colistin elimineres ikke ved hæmodialyse.
Det vides ikke, om natriumcolistimethat kan fjernes ved hæmodialyse eller peritonealdialyse i tilfælde af overdosering.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: antibakterielle midler til systemisk brug, andre antibakterielle midler, polymyxiner.
ATC -kode: J01XB01.
Handlingsmekanisme
Colistin er et cyklisk polypeptid antibakterielt tilhørende gruppen af polymyxiner. Polymyxins virkning er baseret på beskadigelse af cellemembranen, og de deraf følgende fysiologiske virkninger er dødelige for bakterier. Polymyxiner er selektive for aerobe gramnegative bakterier med en hydrofob ydre membran.
Modstand
Resistente bakterier kendetegnes ved modifikationer af lipopolysaccharidets phosphatgrupper, som erstattes med ethanolamin eller amino-arabinose. Naturligt resistente Gram-negative bakterier, som f.eks Proteus mirabilis Og Burkholderia cepacia, viser en fuldstændig substitution af lipidphosphatet med ethanolamin eller amino-arabinose.
Krydsresistens forventes mellem colistin (polymyxin E) og polymyxin B. Da virkningsmekanismen for polymyxin er forskellig fra andre antibakterielle stoffer, bør resistens over for colistin og polymyxin på grund af mekanismen beskrevet ovenfor alene ikke forårsage resistens mod andre klasser af stoffer.
Farmakokinetisk / farmakodynamisk korrelation
Polymyxiner er blevet observeret for at udvise en koncentrationsafhængig bakteriedræbende virkning på modtagelige bakterier. FAUC / MIC menes at være relateret til klinisk effekt.
EUCAST -grænseværdier
til De begrænsende koncentrationer er gældende for en dosis på 2-3 MIU x 3. Indlæsning af dosis (9 MIU) kan være nødvendig.
Følsomhed
Forekomsten af erhvervet resistens kan variere geografisk og over tid for visse arter, og lokal information om resistens er tilrådelig, især til behandling af alvorlige infektioner. Efter behov bør der søges ekspertrådgivning, når den lokale forekomst af resistens er sådan, at lægemidlets anvendelighed, i hvert fald ved nogle typer infektioner, er tvivlsom.
05.2 "Farmakokinetiske egenskaber
Der er begrænset information om farmakokinetikken af natriumcolistimethat (CMS) og colistin. Nogle data indikerer, at farmakokinetikken hos kritisk syge patienter er forskellig fra den, der observeres hos patienter med mindre alvorlige fysiologiske ubalancer og hos raske frivillige. Følgende data er baseret på undersøgelser udført med HPLC -metoden til bestemmelse af plasmakoncentrationer af CMS / colistin.
Efter infusion af natriumcolistimethat omdannes det inaktive prodrug til det aktive stof colistin. Højeste plasmakoncentration af colistin blev observeret med en maksimal forsinkelse på 7 timer efter administration af natriumcolistimethat til kritisk syge patienter.
Fordeling
Distributionsvolumen af colistin hos raske frivillige er lavt og svarer nogenlunde til den ekstracellulære væske. Distributionsmængden stiger betydeligt hos kritisk syge personer. Proteinbinding er moderat og falder ved højere koncentrationer. I mangel af meningeal betændelse er cerebrospinalvæskeindtrængning minimal, men øges i nærvær af meningeal betændelse.
Både CMS og colistin udviser lineær farmakokinetik over det klinisk relevante dosisinterval.
Eliminering
Det anslås, at ca. 30% natriumcolistimethat omdannes til colistin hos raske forsøgspersoner; dets clearance er afhængig af kreatininclearance, og en højere procentdel af CMS omdannes til colistin i tilfælde af nedsat nyrefunktion. Hos patienter med svært nedsat nyrefunktion (glomerulær filtrering af kreatininclearance. Hos raske personer udskilles 60% -70% af CMS uændret i urinen inden for 24 timer.
Elimineringen af det aktive stof colistin er kun delvist karakteriseret. Colistin reabsorberes i vid udstrækning i nyretubuli og kan elimineres både ikke-renalt og via renal metabolisme, med risiko for akkumulering i nyrerne. Colistin-clearance reduceres i tilfælde af nyre værdiforringelse, muligvis på grund af "øget CMS -konvertering."
Halveringstiden for colistin hos raske forsøgspersoner og hos personer med cystisk fibrose udgør henholdsvis ca. 3 timer og 4 timer med en total clearance på ca. 3 L / t. Hos kritisk syge patienter forlænges halveringstiden til ca. 9- 18 timer.
05.3 Prækliniske sikkerhedsdata
De toksiske virkninger af Colistin kan skyldes natriumcolistimethat og udtrykkes i form af tubulær skade. Med 3 mg / kg kan der være en stigning i azotæmi; med 2,5 mg / kg kan der være albuminuri og hæmaturi. Disse fænomener er imidlertid reversible efter afbrydelse af behandlingen. Høje og forlængede doser af natriumcolistimethat hos patienter med patologier nyre kan forårsage neurotoksicitet og nefrotoksicitet, for hvilke doserne skal reduceres passende.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Natriumchlorid, vand til injektionsvæsker.
06.2 Uforenelighed
I mangel af uforenelighedsundersøgelser må dette lægemiddel ikke blandes med andre lægemidler.
06.3 Gyldighedsperiode
3 år i intakt emballage.
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 25 ° C.
06.5 Den umiddelbare emballages art og emballagens indhold
Hætteglas med 1.000.000 IE natriumcolistimethat + 1 hætteglas med opløsningsmiddel 4 ml.
06.6 Brugsanvisning og håndtering
Pulveret i hætteglasset opløses kun på tidspunktet for brug med den fysiologiske opløsning i hætteglasset. Under denne operation er det muligt at opfange variationer i det tryk, der skal udøves på sprøjtens stempel for at indføre opløsningsmidlet i hætteglasset med pulveret. kan bemærke mellem forskellige pakninger med Colimycin, de er ikke i sig selv en indikation af en kvalitetsfejl i medicinen.
Efter rekonstituering skal opløsningen fortyndes til et passende volumen til en 30-60 minutters infusion med natriumchlorid 9 mg / ml (0,9%) infusionsvæske, opløsning.
Opløsningen bør inspiceres visuelt for tilstedeværelse af partikler eller misfarvning inden administration. Opløsningen bør kun bruges, hvis den er klar og fri for partikler.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
UCB Pharma S.p.A. - Via Varesina, 162 - 20156 Milano (Italien).
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
A.I.C. n. 011297013
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 23. juni 1956
Dato for seneste fornyelse: juni 2010
10.0 DATO FOR REVISION AF TEKSTEN
28. juli 2015