Aktive ingredienser: Rotigotine
Neupro 2 mg / 24 timer depotplaster
Neupro 4 mg / 24 timer depotplaster
Neupro 6 mg / 24 timer depotplaster
Neupro 8 mg / 24 timer depotplaster
Hvorfor bruges Neupro? Hvad er det for?
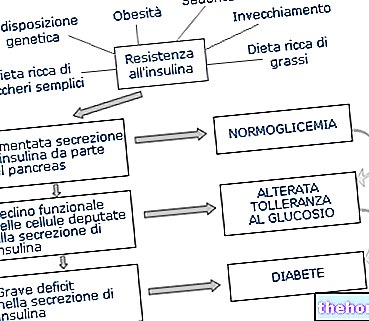
Neupro indeholder det aktive stof rotigotin. Det tilhører en klasse af lægemidler kaldet dopaminagonister, som stimulerer en bestemt celletype, og som binder sig til dopaminreceptorer i hjernen.
Neupro er indiceret til voksne til behandling af tegn og symptomer på Parkinsons sygdom alene eller i kombination med et lægemiddel kaldet levodopa.
Kontraindikationer Når Neupro ikke bør bruges
Tag ikke Neupro
- hvis du er allergisk over for rotigotin eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i afsnit 6).
- hvis du skal gennemgå magnetisk resonansbilleddannelse (en diagnostisk metode, der bruges til at visualisere kroppens indre organer og væv) eller kardioversion (behandling af unormale hjerterytmer). Du skal fjerne Neupro -plasteret, før du gennemgår disse procedurer. i slutningen af procedure kan du anvende en ny patch.
Forholdsregler ved brug Det, du skal vide, før du tager Neupro
Tal med din læge, apotek eller sygeplejerske, før du tager Neupro.
- Denne medicin kan ændre dit blodtryk: Derfor er det tilrådeligt at måle dit blodtryk regelmæssigt, især i starten af behandlingen.
- Bevidsthedstab kan forekomme. Dette kan især ske, når du begynder at bruge Neupro, eller når dosis øges. Fortæl det til din læge, hvis du mister bevidstheden eller føler dig svimmel.
- Øjenundersøgelse med regelmæssige mellemrum anbefales, mens du bruger Neupro. Men hvis du bemærker synsproblemer mellem undersøgelserne, skal du straks kontakte din læge.
- Hvis du har alvorlige leverproblemer, kan din læge ændre din dosis. Hvis dine leverproblemer bliver værre under behandlingen, skal du kontakte din læge hurtigst muligt.
- Hvis du føler dig meget døsig, eller hvis du pludselig falder i søvn, skal du kontakte din læge (se også nedenfor i dette afsnit, "Kørsel og betjening af maskiner").
- Fortæl det til din læge, hvis du eller din familie / omsorgspersoner bemærker, at du udvikler trang eller ønsker, der fører til adfærd, der er usædvanlig for dig, og at du ikke er i stand til at modstå trangen eller fristelsen til at udføre bestemte aktiviteter. Som kan skade dig eller andre. Disse kaldes impulskontrolforstyrrelser og kan omfatte adfærd som spilafhængighed, overdreven spisning eller forbrug, en unormal, overdrevet seksuel lyst eller frygt for øgede tanker eller følelser om seksuel baggrund. Din læge kan finde det nødvendigt at ændre din dosis eller stoppe behandlingen.
- Neupro kan forårsage unormal tænkning og adfærd. Denne unormale tankegang og adfærd kan bestå af en eller flere forskellige manifestationer, herunder unormale tanker om virkeligheden, delirium, hallucinationer (se eller høre ting, der ikke er virkelige), forvirring, desorientering, aggressiv adfærd, uro og delirium. Kontakt din læge, hvis du bemærker disse virkninger.
- Neupro kan forårsage hudreaktioner, såsom rødme og kløe. Disse er normalt milde eller moderate og påvirker kun det område, der er dækket af plasteret. Reaktionerne forsvinder normalt inden for få timer efter fjernelse af plasteret. Hvis du oplever en hudreaktion, der varer mere end et par dage, en alvorlig hudreaktion eller spredes udenfor det hudområde, der er dækket af plasteret, skal du kontakte din læge. Undgå at udsætte områder af din hud, der udviser reaktioner forårsaget af Neupro, for sollys og solarier. For at undgå hudreaktioner skal du påføre plasteret hver dag et andet sted og kun bruge det samme sted efter 14 dage.
Børn og unge
Neupro bør ikke bruges til børn, fordi dets sikkerhed og virkning ikke er fastslået hos børn.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre effekten af Neupro
Brug af anden medicin sammen med Neupro
Fortæl det til din læge eller apotek, hvis du tager anden medicin eller har brugt det for nylig.
Du bør ikke tage følgende medicin, mens du bruger Neupro, da de kan reducere deres virkning: antipsykotika (bruges til behandling af visse psykiske tilstande) eller metoclopramid (bruges til behandling af kvalme og opkastning)
Hvis du behandles med Neupro og levodopa på samme tid, kan nogle bivirkninger blive værre, såsom at høre eller se ting, der ikke er virkelige (hallucinationer), ufrivillige bevægelser relateret til Parkinsons sygdom (dyskinesi) og hævelse i ben og fødder .
Spørg din læge, hvis du kan:
- tager medicin, der sænker blodtrykket. Neupro kan sænke dit blodtryk, når du står op; denne virkning kan forværres af medicin, der bruges til at sænke blodtrykket.
- tager beroligende midler (f.eks. benzodiazepiner, medicin, der bruges til behandling af psykiske lidelser eller depression), mens du bruger Neupro.
Neupro sammen med mad, drikke og alkohol
Da rotigotin passerer ind i blodet gennem huden, har mad og drikke ingen effekt på, hvordan stoffet virker. Du bør kontakte din læge, hvis du kan drikke alkohol, mens du bruger Neupro.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Hvis du er gravid eller ammer, tror at du er gravid eller planlægger at blive gravid, skal du spørge din læge eller apotek til råds, før du tager denne medicin.
Du bør ikke bruge Neupro, hvis du er gravid, da virkningerne af rotigotin på graviditet og det ufødte barn ikke kendes. Amning anbefales ikke under behandling med Neupro. Rotigotin kan passere over i modermælken og påvirke barnet og muligvis også reducere mængden af produceret mælk.
Kørsel og brug af maskiner
Neupro kan få dig til at føle dig meget døsig og kan få dig til at falde i søvn pludselig. Hvis dette sker for dig, bør du ikke køre bil eller deltage i aktiviteter (f.eks. Brug af maskiner), hvor manglende opmærksomhed kan udsætte dig eller andre for risikoen for en alvorlig ulykke. I isolerede tilfælde er patienter faldet i søvn, mens de kørte biler og dermed forårsaget ulykker.
Neupro indeholder natriummetabisulfit (E223)
Natriummetabisulfit (E223) kan sjældent forårsage alvorlige overfølsomhedsreaktioner og bronkospasme.
Dosis, metode og administrationstidspunkt Sådan bruges Neupro: Dosering
Brug altid dette lægemiddel nøjagtigt som din læge eller apotek har fortalt dig. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Neupro initieringspakken indeholder 4 separate pakninger (en for hver mængde aktiv ingrediens) med 7 plastre hver. Disse pakninger bruges normalt i de første fire uger af behandlingen, men afhængigt af din reaktion på Neupro behøver du muligvis ikke at bruge alle pakker, der er vedlagt, eller du skal muligvis bruge andre højere doser efter uge 4, som ikke er inkluderet i denne pakning.
På den første behandlingsdag skal du starte med Neupro 2 mg (pakning mærket "uge 1") og tage et Neupro 2 mg depotplaster hver dag. Brug Neupro 2 mg i 7 dage (hvis du f.eks. Starter på søndag, skal du gå videre til den næste dosis den følgende søndag).
I begyndelsen af den anden uge skal du tage Neupro 4 mg (pakning mærket "uge 2").
I begyndelsen af den tredje uge skal du tage Neupro 6 mg (pakning mærket "uge 3").
I begyndelsen af den fjerde uge skal du tage Neupro 8 mg (pakning mærket "uge 4").
Den mest passende dosis til dig afhænger af dine behov.
4 mg Neupro om dagen kan være en effektiv dosis for nogle patienter. Hos de fleste patienter med Parkinsons sygdom på et tidligt stadium opnås den effektive dosis inden for 3 eller 4 uger med doser på henholdsvis 6 mg / 24 timer eller 8 mg / 24 timer. Den maksimale dosis er 8 mg pr. Dag. For de fleste patienter med fremskreden Parkinsons sygdom opnås den effektive dosis inden for 3 til 7 uger med doser på 8 mg dagligt op til den maksimale dosis på 16 mg pr. Dag. Se afsnit 3, "Hvis du holder op med at tage Neupro", hvis du har brug for at stoppe behandlingen.
Følg disse instruktioner for at bruge Neupro:
Neupro er et plaster til transdermal brug, der skal påføres huden. Du skal anvende et nyt Neupro -plaster på huden en gang om dagen. Lad plasteret ligge på din hud i 24 timer, fjern det derefter og tag et nyt på. Sørg for, at du har fjernet den gamle plaster, inden du påfører en ny. Læg den nye plaster på et andet område af huden. Du bør altid skifte plaster på omtrent samme tid hver dag. Skær ikke Neupro -plastrene i stykker.
Hvor skal plasteret påføres
Påfør plasterets klæbende side på ren, tør og sund hud i følgende områder som angivet i de grå områder i figuren:
- skulder
- overarm
- bug
- lår
- hofte
- flanke (mellem ribben og hofte)
For at undgå hudirritation:
- påfør plasteret på et andet område af huden hver dag, f.eks. en dag til højre for kroppen og derefter den næste dag til venstre; en dag i den øverste del af kroppen, derefter i den nederste del.
- Anvend ikke Neupro igen på det samme hudområde i 14 dage.
- Påfør ikke plasteret på ødelagt eller rød hud eller på rød eller irriteret hud.
Hvis du har hudproblemer på grund af plasteret, kan du se afsnit 4 'Mulige bivirkninger' for at få oplysninger om, hvad du skal gøre.
For at forhindre tab eller afskalning af plasteret
- Påfør ikke plasteret på et område, der kan gnides med stramt tøj.
- Brug ikke cremer, olier, lotioner, pulvere eller andre hudprodukter på det område, hvor du skal påføre plasteret eller i nærheden af et andet plaster, du allerede har taget på.
- Hvis du skal påføre plasteret på et hårdækket område, skal du barbere det berørte område mindst tre dage, før du påfører plasteret.
Hvis plasteret falder af, skal der påføres et nyt plaster resten af dagen, og derefter udskiftes plasteret på samme tid som normalt.
BEMÆRK
- Neupros handling påvirkes normalt ikke af badning, brusebad eller fysisk aktivitet. Sørg dog for, at plasteret ikke er slukket.
- Undgå at udsætte hudområdet, hvor plasteret er påført ekstern varme (f.eks. Overdreven sollys, sauna, meget varme bade, termiske puder eller varmtvandsflasker).
- Hvis plasteret har forårsaget hudirritation, må det berørte område ikke udsættes for sollys, da huden ellers kan ændre farve.
Sådan bruges plasteret
Hver patch er pakket i en separat pose. Påfør Neupro på huden umiddelbart efter åbning af posen og fjernelse af beskyttelsesfilmen.
- For at åbne posen skal du holde de to sider af posen i din hånd. Adskil de to lag af folien, og åbn posen.
- Tag plasteret ud af posen.
- Den klæbrige del af plasteret er dækket af et gennemsigtigt beskyttende lag. Hold plasteret med begge hænder, med det beskyttende lag vendt mod dig.
- Fold plasteret på midten, så den S-formede åbningslinje åbnes.
- Skræl den ene side af beskyttelsesforingen af. Rør ikke den klæbrige side af plasteret med fingrene.
- Hold på den anden side af beskyttelsesforingen, og påfør plasterets klæbende side på huden. Tryk fast på plasterets klæbende side.
- Fold den anden halvdel af plasteret tilbage, og fjern den anden side af beskyttelseslaget.
- Med håndfladen skal du trykke godt på plasteret i 20-30 sekunder for at sikre, at plasteret er i kontakt med huden, og at hjørnerne er tætte.
Vask dine hænder med sæbe og vand umiddelbart efter håndtering af plasteret.
Sådan fjernes en brugt patch
Fjern det brugte plaster langsomt og forsigtigt.
For at fjerne eventuelle klæberester, der er tilbage af plasteret, skal du forsigtigt vaske det berørte område med varmt vand og mild sæbe. For klæbemiddelrester, der ikke kommer af med vand, skal du bruge en lille mængde babyolie. Brug ikke alkohol eller andre opløsningsmidler, såsom neglelakfjerner, da de kan forårsage irritation.Vælg et nyt hudområde for at påføre plasteret, og følg derefter instruktionerne ovenfor.
Overdosering Hvad skal jeg gøre, hvis du har taget for meget Neupro
Hvis du har brugt mere Neupro, end du burde
Brug af højere doser af Neupro end dem, din læge har ordineret, kan forårsage bivirkninger som kvalme (opkastning), lavt blodtryk, hallucinationer (se eller høre ting, der ikke er virkelige), forvirring, ekstrem søvnighed, ufrivillige bevægelser og kramper . Hvis du har påført flere plastre, end din læge har ordineret, skal du kontakte din læge eller hospitalet for øjeblikkelig rådgivning og følge deres råd om fjernelse af plastrene.
Hvis du har påført et andet plaster end det, som din læge har foreskrevet (f.eks. Neupro 4 mg / 24 timer i stedet for Neupro 2 mg / 24 timer), skal du kontakte din læge eller sygehuset for øjeblikkelig rådgivning og følge deres råd om ændring af plastrene. der opstår ubehagelige reaktioner, skal du kontakte din læge.
Hvis du har glemt at ændre plasteret på det sædvanlige tidspunkt
Hvis du har glemt at udskifte plasteret på det sædvanlige tidspunkt, skal du tage det gamle plaster af og tage et nyt på, så snart du husker det. Hvis du har glemt at tage et nyt plaster på efter at have taget det gamle af, skal du tage et nyt på så snart du husker det. I begge tilfælde den næste dag skal du ændre plasteret på det sædvanlige tidspunkt. Anvend ikke en dobbeltdosis som erstatning for en glemt dosis. Hvis du holder op med at bruge Neupro Stop ikke pludselig med at bruge Neupro uden at informere din læge. Et pludseligt stop kan få dig til at udvikle en medicinsk tilstand kaldet neuroleptisk malignt syndrom, som kan udgøre en større sundhedsrisiko. Symptomer omfatter: akinesi (tab af muskelbevægelse), stive muskler, feber, ustabilt blodtryk, takykardi (hurtig puls), forvirring, nedsat bevidsthed (f.eks. Koma).
Den daglige dosis af Neupro bør gradvist reduceres
- 2 mg hver anden dag - hvis du bruger Neupro til Parkinsons sygdom
Spørg din læge, apotek eller sygeplejerske, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Bivirkninger Hvad er bivirkningerne af Neupro
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Du kan føle dig kvalm og kaste op i starten af behandlingen. Disse effekter er normalt milde eller moderate og varer kun i kort tid. Du bør kontakte din læge, hvis de varer i lang tid eller bekymre dig.
Hudproblemer forårsaget af plasteret
Plasteret kan forårsage hudreaktioner såsom rødme, kløe. De er normalt milde eller moderate og påvirker kun det område af huden, hvor plasteret blev påført. Reaktionerne forsvinder normalt et par timer efter, at plasteret er fjernet. Hvis du har en hudreaktion, der varer mere end et par dage, og som er alvorlig eller breder sig ud af det plasterede hudområde, skal du kontakte din læge.
Følgende bivirkninger kan forekomme:
Manglende evne til at modstå trangen, viljen eller fristelsen til at tage handlinger, der kan være skadelige for dig eller andre, som kan omfatte:
- stærk trang til at spille overdrevent på trods af alvorlige personlige eller familiemæssige konsekvenser
- ændret eller øget seksuel interesse og adfærd, der er af væsentlig betydning for dig eller andre, for eksempel en stigning i seksuel lyst
- ukontrollabel og overdreven shopping
- overspisning (spise store mængder mad på kort tid) eller tvangsspisning (spise mere mad end normalt og mere end nødvendigt for at tilfredsstille din appetit)
Fortæl din læge, hvis nogen af disse adfærd sker, så de kan beslutte, hvad de skal gøre for at håndtere eller reducere symptomer.
Hævelse af ansigt, tunge og / eller læber kan forekomme. Kontakt din læge, hvis disse symptomer udvikler sig.
Hvis du bruger Neupro til Parkinsons sygdom, kan følgende bivirkninger observeres:
Meget almindelige bivirkninger: kan forekomme hos mere end 1 ud af 10 patienter
- døsighed, svimmelhed, hovedpine
- kvalme, opkastning
- hudirritationer under plasteret, såsom rødme og kløe
Almindelige bivirkninger: kan forekomme hos op til 1 ud af 10 patienter
- følelse af at se eller høre ting, der ikke er virkelige (hallucinationer)
- søvnbesvær, søvnforstyrrelser, søvnbesvær, mareridt, usædvanlige drømme
- bevidsthedstab, ufrivillige bevægelser relateret til Parkinsons sygdom (dyskinesi), svimmelhed ved at rejse sig fra en siddende eller liggende stilling på grund af et fald i blodtrykket
- svimmelhed (fornemmelse af roterende bevægelse)
- følelse af hjerteslag (hjertebanken)
- fald i blodtrykket, når du rejser dig fra en siddende eller liggende stilling, stigning i blodtrykket
- hikke
- forstoppelse, mundtørhed, halsbrand
- rødme, øget svedtendens, kløe
- hævede ben og fødder
- følelse af svaghed, træthed
- efterår
- vægttab
- manglende evne til at modstå trangen til at udføre en handling, der kan forårsage skade, herunder overdreven spil, meningsløse gentagne handlinger, overspisning og tvangshandel og tvangshandel
Ikke almindelige bivirkninger: kan forekomme hos op til 1 ud af 100 patienter
- Allergisk reaktion
- pludselig faldet i søvn uden advarselsskilte
- paranoia
- desorientering
- agitation
- øget seksuel aktivitet
- forvirring
- sløret syn
- synsforstyrrelser såsom syn af farver eller lys
- uregelmæssig hjerterytme
- fald i blodtryk
- ondt i maven og smerterne
- generaliseret kløe, hudirritation
- manglende evne til at opnå eller opretholde en erektion
- øgede eller unormale resultater i leverfunktionstest
- vægtøgning
- acceleration af hjerteslag
- øgede niveauer af kreatinfosfokinase (CPK) i blodet hos japanske patienter (CPK er et enzym, der hovedsageligt findes i skeletmuskler). Der er ingen oplysninger tilgængelige i andre populationer.
Sjældne bivirkninger: kan forekomme hos op til 1 ud af 1000 patienter
- psykotiske lidelser
- aggressiv adfærd / aggression
- ufrivillige muskelspasmer (kramper)
- generaliseret udslæt
- irritabilitet delirium
- begejstret
Ikke kendt: hyppigheden kan ikke estimeres ud fra de tilgængelige data
- overdreven brug af Neupro (trang til høje doser dopaminerge lægemidler, der overstiger det, der er nødvendigt for at kontrollere motoriske symptomer, kendt som dopaminerg dysregulationssyndrom)
Indberetning af bivirkninger
Tal med din læge, apotek eller sygeplejerske, hvis du får bivirkninger. Dette omfatter eventuelle bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også rapportere bivirkninger direkte via det nationale rapporteringssystem anført i tillæg V. Bivirkninger kan hjælpe give mere information om sikkerheden ved dette lægemiddel
Udløb og opbevaring
Opbevar denne medicin utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på etiketten og kartonen.
Må ikke opbevares over 25 ° C.
Bortskaffelse af brugte eller ubrugte plastre
Brugte plastre indeholder stadig den aktive ingrediens, som kan være skadelig for andre mennesker. Fold det brugte plaster med den klæbrige side i. Returner plasteret til den originale pose og bortskaf det sikkert uden for børns rækkevidde.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Sammensætning og farmaceutisk form
Hvad Neupro indeholder
- Den aktive ingrediens er rotigotin.
Neupro 2 mg / 24 timer
Hver plaster frigiver 2 mg rotigotin pr. 24 timer.
Hver 10 cm2 plaster indeholder 4,5 mg rotigotin.
Neupro 4 mg / 24 timer
Hver plaster frigiver 4 mg rotigotin pr. 24 timer.
Hver 20 cm2 plaster indeholder 9,0 mg rotigotin.
Neupro 6 mg / 24 timer
Hver plaster frigiver 6 mg rotigotin pr. 24 timer.
Hver plaster på 30 cm2 indeholder 13,5 mg rotigotin.
Neupro 8 mg / 24 timer
Hvert plaster frigiver 8 mg rotigotin pr. 24 timer.
Hver 40 cm2 plaster indeholder 18,0 mg rotigotin.
- Øvrige indholdsstoffer er: poly (dimethylsiloxan, trimethylsilylsilikat) copolymeriseret, povidon K90, natriummetabisulfit (E223), ascorbylpalmitat (E304) og DL-α-tocopherol (E307).
- Støttelag: polyesterfilm belagt med silikone og aluminium, farvet med et lag pigment (titandioxid (E171), gult pigment 95, pigmentrødt 166) og forsynet med en påskrift (pigmentrød 144, pigmentgul 95, pigment sort 7). Beskyttelseslag: polyesterfilm belagt med gennemsigtig fluorpolymer
Hvordan Neupro ser ud og pakningens indhold
Neupro er et depotplaster. Den er tynd og består af tre lag. Det er en firkantet patch med afrundede hjørner. Ydersiden af underlaget er beige og præget med Neupro 2 mg / 24 timer, 4 mg / 24 timer, 6 mg / 24 timer eller 8 mg / 24 timer.
Neupro fås i følgende pakningsstørrelser: Behandlingsstartpakken indeholder 28 depotplastre i 4 kartoner indeholdende 7 plastre på 2 mg, 4 mg, 6 mg og 8 mg hver, forseglet i en enkelt pose.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
NEUPRO
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Neupro 2 mg / 24 timer depotplaster
Hver plaster frigiver 2 mg rotigotin pr. 24 timer. Hver 10 cm2 plaster indeholder 4,5 mg rotigotin.
Neupro 4 mg / 24 timer depotplaster
Hver plaster frigiver 4 mg rotigotin pr. 24 timer. Hver 20 cm2 plaster indeholder 9,0 mg rotigotin.
Neupro 6 mg / 24 timer depotplaster
Hver plaster frigiver 6 mg rotigotin pr. 24 timer. Hver plaster på 30 cm2 indeholder 13,5 mg rotigotin.
Neupro 8 mg / 24 timer depotplaster
Hvert plaster frigiver 8 mg rotigotin pr. 24 timer. Hver 40 cm2 plaster indeholder 18,0 mg rotigotin.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Transdermal plaster.
Tynd, matrix, firkantet patch med afrundede hjørner, bestående af tre lag. Ydersiden af bagsidelaget er beige i farven og præget med "Neupro 2 mg / 24 timer, 4 mg / 24 timer, 6 mg / 24 timer eller 8 mg / 24 timer".
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Neupro er indiceret til behandling af tegn og symptomer på idiopatisk Parkinsons sygdom på et tidligt stadium som monoterapi (dvs. uden levodopa) eller i kombination med levodopa; eller i sygdomsforløbet, herunder de sene faser, når levodopas virkning reduceres eller afbrydes, og udsving i den terapeutiske effekt forekommer (end-of-dosis effekt eller "on / off" fænomener).
04.2 Dosering og indgivelsesmåde
Dosering:
Neupro påføres en gang dagligt. Plasteret skal påføres på omtrent samme tid hver dag. Plasteret forbliver i kontakt med huden i 24 timer og erstattes efterfølgende med et nyt plaster placeret på et andet applikationssted.
Hvis patienten glemmer at påføre plasteret på det sædvanlige tidspunkt, eller hvis plasteret falder af, skal der påføres et andet plaster resten af dagen.
Dosering:
Doseringsanbefalinger refererer til den nominelle dosis.
Dosering hos patienter med tidlig Parkinsons sygdom:
En enkelt dosis på 2 mg / 24 timer bør startes og øges ugentligt med 2 mg / 24 timer, indtil den effektive dosis er nået, op til maksimalt 8 mg / 24 timer. Hos nogle patienter kan administration af 4 mg / 24 timer svare til den effektive dosis. Hos de fleste patienter opnås den effektive dosis inden for 3 eller 4 uger med doser på henholdsvis 6 mg / 24 timer eller 8 mg / 24 timer.
Den maksimale dosis er 8 mg / 24 timer.
Dosering hos patienter med fremskreden Parkinsons sygdom med udsving:
En enkelt dosis på 4 mg / 24 timer bør startes og øges ugentligt med 2 mg / 24 timer, indtil den effektive dosis er nået, op til maksimalt 16 mg / 24 timer. Hos nogle patienter kan administration af 4 mg / 24 timer eller 6 mg / 24 timer svare til den effektive dosis. Hos de fleste patienter opnås den effektive dosis inden for 3 til 7 uger med doser på 8 mg / 24 timer, op til maksimalt 16 mg / 24 timer.
Neupro -behandlingsstartpakken indeholder 4 forskellige pakninger (en for hver mængde aktiv ingrediens) med 7 plastre hver, der skal bruges i de første fire uger af behandlingen. Afhængigt af patientens reaktion er det muligvis ikke nødvendigt at gennemgå alle trinene til dosering beskrevet nedenfor, eller der kan være behov for yderligere højere doser efter uge 4, som ikke er inkluderet i denne pakning.
På den første dag starter patienten behandlingen med Neupro 2 mg / 24 timer. I løbet af den anden uge påfører patienten Neupro 4 mg / 24 timer plastre. I løbet af den tredje uge skifter patienten til Neupro 6 mg / 24 timer og derefter i den fjerde uge til Neupro 8 mg / 24 timer. Pakningerne er mærket "Uge 1 (2, 3 eller 4)".
Afbrydelse af behandlingen:
Neupro skal afbrydes gradvist. Den daglige dosis bør reduceres i trin på 2 mg / 24 timer ad gangen, muligvis hver anden dag, indtil Neupro afbrydes fuldstændigt (se pkt. 4.4).
Særlige populationer:
Ændringer i lever- og nyrefunktion: det er ikke nødvendigt at justere dosis til patienter med milde til moderate ændringer i leverfunktionen eller med milde til alvorlige ændringer i nyrefunktionen, herunder dem, der gennemgår dialyse. Der udvises forsigtighed ved behandling af patienter med svært nedsat leverfunktion, da dette kan resultere i lavere rotigotinclearance. Rotigotin er ikke blevet evalueret i denne patientgruppe. En dosisreduktion kan være nødvendig i tilfælde af forværring af leverfunktionen. Uventet ophobning af rotigotinniveauer kan observeres i tilfælde af akut forværring af nyrefunktionen (se pkt. 5.2).
Pædiatrisk population
Sikkerhed og effekt af rotigotin i den pædiatriske population er endnu ikke fastslået. Der foreligger ingen data.
Indgivelsesmåde:
Plasteret skal påføres ren, tør, intakt og sund hud på maven, lår, hofter, hofter, skuldre eller arme. Genanvendelse på det samme administrationssted bør undgås i 14 dage. Neupro bør ikke placeres på rød, irriteret eller beskadiget hud (se pkt. 4.4).
Anvendelse og anvendelse:
Hvert plaster er pakket i en pose og skal påføres umiddelbart efter åbningen af posen. Skræl den ene halvdel af beskyttelseslaget af og påfør den klæbende del på huden, tryk den fast på huden. Fold derefter plasteret tilbage og skræl af huden. "anden halvdel af beskyttelseslaget. Undgå at røre ved den klæbrige side af plasteret. Tryk plasteret fast på huden med din håndflade i mindst 20-30 sekunder, så det sidder godt fast.
Hvis et plaster falder af, skal der påføres et nyt plaster i den resterende tid af 24 timers doseringsinterval.
Plasteret må ikke skæres i stykker.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne.
Magnetisk resonansbilleddannelse eller kardioversionstest (se pkt. 4.4).
04.4 Særlige advarsler og passende forholdsregler ved brug
Hvis en patient med Parkinsons sygdom ikke reagerer tilstrækkeligt på rotigotinbehandling, kan det være en ekstra fordel at skifte til en anden dopaminagonist (se pkt.5.1).
Magnetisk resonansbilleddannelse og kardioversion:
Baglaget i Neupro indeholder aluminium. For at undgå forbrændinger af huden skal Neupro fjernes, hvis patienten skal undergå magnetisk resonansbilleddannelse (MRI) eller kardioversion.
Ortostatisk hypotension:
Dopaminagonister vides at ændre den systemiske regulering af blodtryk, hvilket resulterer i postural / ortostatisk hypotension.Disse effekter blev også set under behandling med rotigotin, men forekomsten lignede den, der blev set hos patienter behandlet med placebo.
Synkope forbundet med brugen af rotigotin er blevet rapporteret, men med en lignende frekvens som patienter behandlet med placebo.
Det anbefales, at blodtrykket overvåges, især i starten af behandlingen, på grund af risikoen for ortostatisk hypotension, der generelt er forbundet med dopaminerg behandling.
Pludselig søvn og døsighed:
Rotigotin har været forbundet med søvnighed og pludselige episoder med søvn. Der har været rapporter om pludselig søvnbegyndelse under daglige aktiviteter, i nogle tilfælde uden advarselstegn. Læger bør konstant spørge patienten om tilstedeværelsen af døsighed og søvnighed, da patienten muligvis ikke genkender disse symptomer uden et specifikt spørgsmål om dem. I dette tilfælde bør muligheden for at reducere dosis eller afbryde behandlingen overvejes nøje.
Impulskontrolforstyrrelser:
Tilfælde af patologisk spil, øget libido og hyperseksualitet er blevet rapporteret hos patienter behandlet med dopaminagonister, herunder rotigotin.
Neuroleptisk malignt syndrom
Symptomer, der kan tilskrives et neuroleptisk malignt syndrom, er blevet rapporteret i tilfælde af pludselig afbrydelse af dopaminerg behandling. Det anbefales derfor gradvist at afbryde behandlingen (se pkt.4.2).
Hallucinationer:
Hallucinationer er blevet rapporteret, og patienter bør informeres om dette.
Fibrotiske komplikationer:
Fibrotiske komplikationer: Tilfælde af retroperitoneal fibrose, lungeinfiltrater, pleural effusion, pleural fortykkelse, pericarditis og hjertevalvulopati er blevet rapporteret hos nogle patienter behandlet med ergot-afledte dopaminerge midler. Disse komplikationer kan komme tilbage ved afbrydelse af behandlingen, men ikke. En fuldstændig opløsning forekommer altid.
Selvom disse bivirkninger anses for at være relateret til ergolinstrukturen af disse forbindelser, vides det ikke, om andre dopaminagonister, der ikke stammer fra ergot, kan forårsage deres forekomst.
Neuroleptika:
Administrer ikke neuroleptika som antiemetika til patienter behandlet med dopaminagonister (se også afsnit 4.5).
Oftalmologisk overvågning:
Regelmæssig oftalmologisk overvågning anbefales eller i nærvær af synsforstyrrelser.
Varme applikation:
Undgå at udsætte det hudområde, hvor plasteret er påført, for varmekilder, såsom overdreven sollys, varmepuder og andre varmekilder, såsom en sauna eller et meget varmt bad.
Reaktioner på applikationsstedet:
Hudreaktioner, normalt milde eller moderate i intensitet, kan forekomme på applikationsstedet. Det anbefales, at plasterpåføringsstedet varieres dagligt (f.eks. Højre til venstre og overkrop til underkrop). Undgå at genanvende plasteret på det samme sted i 14 dage. Hvis reaktionerne på applikationsstedet vedvarer i flere dage eller vedvarer, forværres, eller hvis hudreaktionen strækker sig ud over applikationsstedet, bør fordel / risiko -forholdet for den pågældende patient vurderes på ny. I tilfælde af hududslæt eller irritation forårsaget af depotplasteret, undgå udsættelse for direkte sollys, indtil hudlæsionen heler. Eksponering for sollys kan føre til misfarvning af huden.
I tilfælde af en generaliseret hudreaktion (f.eks. Allergisk udslæt, herunder erytematøst, makulært, papulært eller pruritusudslæt) i forbindelse med brug af Neupro, bør behandlingen med Neupro afbrydes.
Dopaminerge bivirkninger:
Forekomsten af nogle bivirkninger af dopaminerg type som hallucinationer, dyskinesi og perifert ødem er generelt højere ved samtidig administration med L-DOPA til patienter med Parkinsons sygdom Dette skal tages i betragtning ved ordination af rotigotin.
Perifert ødem:
I kliniske undersøgelser af patienter med Parkinsons sygdom var den specifikke hyppighed af perifert ødem efter 6 måneder cirka 4% og forblev sådan i hele observationsperioden på 36 måneder.
Følsomhed over for sulfitter:
Neupro indeholder natriummetabisulfit, en sulfit, der hos nogle følsomme mennesker kan forårsage allergiske reaktioner, herunder anafylaktiske symptomer og livstruende astmaepisoder eller mindre alvorlige astmaepisoder.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Da rotigotin er en dopaminagonist, antages det, at dopaminantagonister, såsom neuroleptika (f.eks. Phenothiaziner, butyrophenoner, thioxanthener) eller metoclopramid kan reducere Neupros effekt og derfor deres samtidige administration På grund af mulige additive virkninger bør der udvises forsigtighed hos patienter, der tager beroligende midler, andre CNS (centralnervesystem) depressiva (f.eks. benzodiazepiner, antipsykotika, antidepressiva) eller alkohol i kombination med rotigotin.
Samtidig administration af L-dopa og carbidopa med rotigotin havde ingen effekt på rotigotins farmakokinetik, og rotigotin havde ingen effekt på farmakokinetikken for L-dopa og carbidopa.
Samtidig administration af domperidon og rotigotin havde ingen effekt på rotigotins farmakokinetik.
Samtidig administration af omeprazol (CYPC19-hæmmer) i doser på 40 mg pr. Dag havde ingen effekt på farmakokinetikken og metabolismen af rotigotin hos raske frivillige. Neupro kan forstærke dopaminerge bivirkninger af L-DOPA og kan forårsage og / eller forværre eksisterende dyskinesier, som beskrevet for andre dopaminagonister.
Samtidig administration af rotigotin (3 mg / 24 timer) ændrede ikke farmakodynamikken og farmakokinetikken af orale præventionsmidler (0,03 mg ethinylestradiol, 0,15 mg levonorgestrel). Interaktioner med andre former for hormonel prævention er ikke undersøgt.
04.6 Graviditet og amning
Graviditet:
Der er ikke tilstrækkelige data om brug af rotigotin til gravide Dyrestudier viser ingen teratogene virkninger hos rotter og kaniner, men embryotoksiske effekter blev observeret hos rotter og mus efter administration af toksiske doser til gravide kvinder (se pkt. 5.3). potentiel risiko for mennesker er ukendt. Brug af rotigotin bør undgås under graviditet.
Fodringstid:
Da rotigotin reducerer prolaktinsekretion hos mennesker, forventes en hæmmende effekt på diegivningen. Undersøgelser hos rotter har vist, at rotigotin og / eller dets metabolit (er) udskilles i modermælk. I mangel af humane data bør amning afbrydes.
Fertilitet:
For information om fertilitetsundersøgelser, se afsnit 5.3.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Rotigotin kan forringe evnen til at føre motorkøretøj eller betjene maskiner.
Patienter behandlet med rotigotin, der oplever somnolens og / eller episoder med pludseligt søvnangreb, må ikke køre bil og bør ikke deltage i aktiviteter (f.eks. Betjening af maskiner), hvor nedsat årvågenhed kan udsætte sig selv eller andre. Mennesker med risiko for alvorlig skade eller død indtil disse tilbagevendende episoder og søvnighed er forsvundet (se også pkt. 4.4 og 4.5).
04.8 Bivirkninger
Baseret på analyse af samlede data fra placebokontrollerede kliniske forsøg, herunder i alt 1.307 patienter behandlet med Neupro og 607 patienter behandlet med placebo, hos 72,3% af patienterne behandlet med Neupro og 57,8% af patienterne behandlet med placebo, mindst én bivirkning reaktion forekom.
Dopaminerge bivirkninger, såsom kvalme og opkastning, kan forekomme ved behandlingsstart. De er generelt milde eller moderate i intensitet og forbigående, selvom behandlingen ikke stoppes. Bivirkninger rapporteres hos mere end 10% af patienterne behandlet med Neupro depotplaster er kvalme, opkastning, reaktioner på applikationsstedet, døsighed, svimmelhed og hovedpine.
I undersøgelser, hvor applikationsstedet blev ændret som beskrevet i instruktionerne i produktresuméet og indlægssedlen, oplevede 35,7% af 830 patienter behandlet med Neupro depotplaster reaktioner på applikationsstedet. De fleste af disse reaktioner var milde eller moderate i intensitet og begrænset til applikationsstedet, og afbrydelse af Neupro -behandling var nødvendig hos kun 4,3% af alle behandlede patienter.
Inden for hver frekvensklasse rapporteres bivirkninger i faldende sværhedsgrad.
Tabellen nedenfor opsummerer de bivirkninger, der er rapporteret i alle undersøgelser udført med patienter med Parkinsons sygdom. Inden for systemorganklassifikationerne er bivirkninger opført efter hyppighed (antal patienter, der forventes at udvikle reaktionen), ved hjælp af følgende kategorier: meget almindelig (≥1 / 10); almindelig (≥1 / 100 til
sigt på højt niveau
Beskrivelse af udvalgte bivirkninger:
Pludselig søvn og døsighed:
Rotigotin har været forbundet med somnolens, herunder "overdreven søvnighed i dagtimerne og episoder med pludselig søvnindbrud. I isolerede tilfælde er" den "pludselige begyndelse af søvn" sket, mens patienten kørte et motorkøretøj, hvilket resulterede i ulykker på vej. Se også afsnit 4.4 og 4.7.
Impulskontrolforstyrrelser:
Patienter behandlet med dopaminagonister, herunder rotigotin, har udvist symptomer, der kan tilskrives patologisk spil, øget libido og hyperseksualitet, generelt reversible efter dosisreduktion eller afbrydelse af behandlingen.
04.9 Overdosering
De mest sandsynlige bivirkninger ville være dem, der er relateret til den farmakodynamiske profil af en dopaminagonist og omfatter: kvalme, opkastning, hypotension, ufrivillige bevægelser, hallucinationer, forvirring, anfald og andre tegn på central dopaminerg stimulering. Der er ingen kendte modgift til behandling af overdosering af dopaminagonister. Hvis der er mistanke om overdosering, skal plasteret / plasterne straks fjernes fra patientens hud. Rotigotinniveauer falder efter fjernelse af plasteret. Inden administrationen af rotigotin stoppes fuldstændigt, se pkt.4.2.
Patienten bør overvåges nøje, herunder vurdering af puls og rytme og blodtryk. Da mere end 90% af rotigotin er bundet til plasmaproteiner, forventes der ingen klinisk fordel ved dialyse.
Behandling af overdosering kan kræve generelle terapeutiske foranstaltninger for at holde vitale tegn stabile.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: Antiparkinson, dopaminagonister; ATC -kode: N04BC09.
Rotigotine er en ikke-ergolin D3 / D2 / D1 dopaminagonist indiceret til behandling af Parkinsons sygdom. Det menes, at dens positive virkninger skyldes aktiveringen af D3-, D2- og D1-receptorerne i cerebralområdet i caudat-putamen. Rotigotin lindrer tegn og symptomer på idiopatisk Parkinsons sygdom.
Kliniske undersøgelser:
Rotigotins effekt ved behandling af tegn og symptomer på idiopatisk Parkinsons sygdom blev evalueret i et multinationalt klinisk udviklingsprogram omfattende 4 centrale, dobbeltblinde, placebokontrollerede, randomiserede, parallelle gruppestudier.
To undersøgelser vedrørende rotigotins effekt ved behandling af tegn og symptomer på idiopatisk Parkinsons sygdom blev udført hos patienter, der ikke tidligere fik samtidig dopaminagonistbehandling, som aldrig havde modtaget L-DOPA, eller hvor administrationen af L-DOPA ikke var længere end 6 måneder Den primære effektvariabel var komponentens værdi Aktiviteter i dagligdagen (ADL), del II, plus komponenten Motorisk undersøgelsedel III af "Unified Parkinsons sygdomsvurderingsskala (UPDRS).
Effekten blev bestemt på grundlag af patientens respons på terapi, udtrykt i procent af respondenterne og forbedring udtrykt som en absolut værdi på ADL- og motorundersøgelsesskalaerne (UPDRS del II + III) .I en første dobbeltundersøgelse blindet , blev rotigotin administreret til 177 patienter og placebo til 96 patienter. Dosen af rotigotin eller placebo blev titreret til den optimale dosis og administreret til patienter i ugentlige trin på 2 mg / 24 timer, startende med 2 mg / 24 timer og op til en maksimal dosis på 6 mg / 24 timer Patienter i hver gruppe modtog deres optimale vedligeholdelsesdosis i 6 måneder.
Ved afslutningen af vedligeholdelsesbehandlingen var den optimale dosis for 91% af patienterne i rotigotin -gruppen den maksimalt tilladte dosis, dvs. 6 mg / 24 timer. En forbedring på 20% blev set hos 48% af rotigotinbehandlede patienter og 19% af placebobehandlede patienter (forskel 29% CI95% 18%; 39%, p
I en anden dobbeltblind undersøgelse fik 213 patienter rotigotin, 227 patienter blev behandlet med ropinirol og 117 patienter fik placebo. Dosen af rotigotin blev titreret til den optimale dosis og administreret til patienter i ugentlige trin på 2 mg / 24 timer, startende med 2 mg / 24 timer og op til en maksimal dosis på 8 mg / 24 timer i en periode på 4 uger I ropinirolgruppen blev dosis titreret op til den optimale dosis, op til maksimalt 24 mg / dag, over 13 uger. Patienter i hver gruppe modtog deres vedligeholdelsesdosis i 6 måneder.
Ved afslutningen af vedligeholdelsesbehandlingen var den optimale dosis hos 92% af patienterne i rotigotingruppen den maksimalt tilladte dosis, dvs. 8 mg / 24 timer. En forbedring på 20% blev set hos 52% af rotigotinbehandlede forsøgspersoner, 68% af ropinirolbehandlede forsøgspersoner og 30% af placebobehandlede patienter (forskel mellem rotigotin versus placebo 21,7%; 95% KI 11,1%; 32,4%, forskel i ropinirol versus placebo 38,4%CI95%28,1%; 48,6%, forskel i ropinirol versus rotigotin 16,6%; CI95%7,6%; 25,7%). Den gennemsnitlige forbedring i UPDRS -score (del II + III) var 6,83 point (baseline 33,2 point) i rotigotin -gruppen, 10,78 point i ropinirolgruppen (baseline 32,2 point) og 2, 33 point i placebogruppen (baseline 31,3 point) . Alle forskelle mellem aktive behandlinger og placebo var statistisk signifikante. Forskellen i effekt mellem ropinirol og rotigotin var også statistisk signifikant til fordel for ropinirol. To yderligere undersøgelser blev udført på patienter, der fik samtidig levodopa -behandling. Den primære effektvariabel var reduktionen i "slukket" tid (timer). Effekten blev bestemt på grundlag af patientens respons på terapi, målt i procent af respondenterne og forbedringen i den absolutte værdi af varigheden af "off" -tiden.
I den første dobbeltblinde undersøgelse modtog 113 patienter rotigotin op til en maksimal dosis på 8 mg / 24 timer, 109 patienter fik rotigotin op til en maksimal dosis på 12 mg / 24 timer og 119 patienter fik placebo. Dosen af rotigotin eller placebo blev titreret til den optimale dosis og administreret til patienter i ugentlige trin på 2 mg / 24 timer, startende med 4 mg / 24 timer.Patienter i hver gruppe modtog deres optimale vedligeholdelsesdosis i 6 måneder. Ved afslutningen af vedligeholdelsesbehandlingen blev der set en forbedring på mindst 30% hos 57% og 55% af patienterne, der blev administreret henholdsvis 8 mg / 24 timer og 12 mg / 24 timer rotigotin og hos 34% patienter behandlet med placebo. (forskelle på henholdsvis 22%og 21%, CI95%henholdsvis 10%, 35%og 8%, 33%, s
I den anden dobbeltblinde undersøgelse modtog 201 patienter rotigotin, 200 patienter fik pramipexol og 100 patienter fik placebo. Dosen af rotigotin blev titreret til den optimale dosis og administreret til patienter i ugentlige trin på 2 mg / 24 timer, startende med 4 mg / 24 timer og op til en maksimal dosis på 16 mg / 24 timer. I pramipexolgruppen modtog patienterne 0,375 mg den første uge, 0,75 mg den anden uge, og dosis blev titreret i yderligere ugentlige trin på 0,75 mg, indtil den optimale dosis var nået, op til et maksimum på 4,5 mg / dag. Patienter i hver gruppe modtog deres vedligeholdelsesdosis i 4 måneder.
Ved afslutningen af vedligeholdelsesbehandlingen blev der set en forbedring på mindst 30% hos 60% af patienterne behandlet med rotigotin, 67% af patienterne behandlet med pramipexol og 35% af patienterne behandlet med placebo (forskel mellem rotigotin imod placebo 25%; CI95% 13%; 36%, forskel mellem pramipexol imod placebo 32% CI95% 21%; 43%, forskel mellem pramipexol imod rotigotin 7%; CI95% - 2%; 17%). Den gennemsnitlige reduktion i "slukket" tid var 2,5 timer i rotigotingruppen, 2,8 timer i pramipexolgruppen og 0,9 timer i placebogruppen. Alle forskelle mellem aktive behandlinger og placebo var statistisk signifikante.
05.2 "Farmakokinetiske egenskaber
Absorption:
Efter påføring frigiver det depotplaster konstant rotigotin, som absorberes af huden. stabil tilstand opnås en eller to dage efter plasterpåføring og opretholdes på et stabilt niveau med en enkelt daglig påføring af plasteret i 24 timer Rotigotin plasmakoncentrationer viser en dosisproportional stigning i intervallerne fra 1 mg / 24 timer til 24 mg / 24 timer.
I løbet af 24 timer frigives cirka 45% af den aktive ingrediens i plasteret. Den absolutte biotilgængelighed efter transdermal påføring er cirka 37%.
Rotation af plasterpåføringsstedet kan resultere i daglige forskelle i plasmaniveauer. Forskellene i biotilgængeligheden af rotigotin er mellem 2% (øvre lem versus flanke) og 46% (skulder versus lår). Der er imidlertid ingen indikationer på en relevant indvirkning af disse forskelle på det kliniske resultat.
Fordeling:
In vitro, plasmaproteinbindingen af rotigotin er cirka 92%.
Det tilsyneladende fordelingsvolumen hos mennesker er cirka 84 l / kg.
Metabolisme:
Rotigotin metaboliseres i udstrakt grad: metabolisme sker via N-dealkylering og direkte og sekundær konjugering. De opnåede resultater in vitro angiver, at forskellige CYP-isoformer er i stand til at katalysere N-dealkyleringen af rotigotin. Hovedmetabolitterne er sulfater og glucuronider konjugeret af hovedproduktet samt biologisk inaktive N-dealkylerede metabolitter.
Data om metabolitter er ufuldstændige.
Eliminering:
Ca. 71% af rotigotin udskilles i urinen, og en mindre del, svarende til ca. 23%, udskilles i fæces.
Rotigotins clearance efter transdermal administration er ca. 10 l / min, og eliminationshalveringstiden er mellem 5 og 7 timer.
Da lægemidlet administreres transdermalt, forventes der ingen ændringer relateret til tilstedeværelsen af mad eller gastrointestinale forstyrrelser.
Særlige kategorier af patienter:
Da Neupro -behandling påbegyndes med en lav dosis, som gradvist øges i henhold til klinisk tolerabilitet for at opnå et optimalt terapeutisk resultat, er det ikke nødvendigt at justere dosis baseret på køn, vægt eller alder.
Der blev ikke observeret signifikante stigninger i rotigotinplasmaniveauer hos patienter med moderat nedsat leverfunktion eller lette til svære ændringer i nyrefunktionen.
Neupro er ikke undersøgt hos patienter med svært nedsat leverfunktion.
Plasmaniveauer af rotigotinkonjugater og dets dealkylerede metabolitter stiger i tilfælde af nedsat nyrefunktion. Disse metabolitter bidrager dog usandsynligt til kliniske virkninger.
05.3 Prækliniske sikkerhedsdata
I undersøgelser med gentagen dosis og langtids toksicitet var hovedeffekterne forbundet med farmakodynamik af dopaminagonister og den deraf følgende reduktion i prolaktinsekretion.
Efter en enkelt indgivelse af rotigotin var binding til melaninholdige væv (f.eks. Øjne) tydelig hos pigmenterede rotter og aber, men faldt langsomt tilbage i løbet af den 14-dages observationsperiode.
I et 3-måneders studie med albino rotter blev retinal degeneration observeret ved transmissionsmikroskopi efter administration af doser svarende til 2,8 gange den maksimalt anbefalede humane dosis, beregnet i mg / m2. Effekter de var mere udtalte hos hunrotter. Ingen yderligere undersøgelser var udført for at evaluere den specifikke patologi. I nogen af de udførte toksikologiske undersøgelser og hos ingen af de anvendte dyrearter blev retinal degeneration observeret ved rutinemæssig histopatologisk undersøgelse af øjet. Den kliniske relevans af disse data for mennesker er stadig ukendt.
Tumorer og Leydig cellehyperplasi blev fundet hos hanrotter i carcinogenicitetsundersøgelser. Udseende af maligne tumorer blev overvejende fundet i livmoderen hos hunner behandlet med mellemstore og høje doser Disse ændringer repræsenterer velkendte virkninger af dopaminagonister hos rotter efter livslang behandling og anses ikke for relevante for mennesker. Rotigotins virkninger på reproduktion blev undersøgt hos rotter, kaniner og mus. Rotigotin viste sig at være ikke-teratogent i alle tre arter, men var embryotoksisk hos rotter og mus efter administration af toksiske doser til gravide hunner. Hos rotter havde rotigotin ingen effekt på hanfrugtbarhed, men det fremkaldte en signifikant reduktion i hunfrugtbarhed hos rotter og mus på grund af dets virkninger på prolaktinniveauer, som er særligt signifikante hos gnavere.
Rotigotin inducerede ikke genmutationer i Ames -testen, men viste effekter i muslymfoma -assayet hos mus. in vitro efter metabolisk aktivering og mindre markante effekter uden metabolisk aktivering. Denne mutagene virkning er blevet tilskrevet en clastogen effekt af rotigotin. Denne effekt er ikke bekræftet in vivo i musens mikronukleustest i musen og i den ikke -planlagte DNA -syntesetest (UDS) i rotten. Da det stort set har vist sig at parallelle en relativ reduktion i den totale cellevækst, kan det være relateret til en cytotoksisk virkning af stoffet. Derfor er betydningen af et enkelt positivt resultat i den mutagene test in vitro det vides ikke.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Understøttelseslag:
Polyesterfilm belagt med silikone og aluminium, farvet med et lag pigment (titandioxid (E171), gult pigment 95, pigmentrødt 166) og forsynet med en påskrift (pigmentrød 144, pigmentgul 95, pigment sort 7).
Selvklæbende matrix:
Poly (dimethylsiloxan, trimethylsilylsilikat) copolymeriseret, Povidone K90, natriummetabisulfit (E223), ascorbylpalmitat (E304) og DL-α-tocopherol (E307).
Beskyttende lag:
Polyesterfilm belagt med gennemsigtig fluorpolymer.
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
18 måneder.
06.4 Særlige opbevaringsforhold
Opbevares i køleskab (2 ° C - 8 ° C).
06.5 Den umiddelbare emballages art og emballagens indhold
Afrivningspose i papkasse: den ene side består af en ethylencopolymer (indre lag), en aluminiumsfilm, en lavdensitets polyethylenfilm og papir; den anden side består af polyethylen (indre lag), aluminium, ethylencopolymer og papir.
Behandlingsstartpakken indeholder 28 depotplastre i 4 kartoner indeholdende 7 plastre på 2 mg, 4 mg, 6 mg og 8 mg hver, forseglet i en enkelt pose.
06.6 Brugsanvisning og håndtering
Efter brug indeholder plasteret stadig den aktive ingrediens. Efter fjernelse foldes plasteret på midten, med det klæbende lag vendt indad, for ikke at udsætte matricen, og derefter lægge det tilbage i den originale pose og bortskaffe det uden for rækkevidde af børn. børn. Eventuelle brugte eller ubrugte plastre skal bortskaffes i overensstemmelse med lokale krav eller returneres til apoteket.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
SCHWARZ PHARMA Ltd.
Shannon, industriområde,
Co. Clare, Irland
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/05/331/013 A.I.C. 037152131
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 15. februar 2006












.jpg)