Aktive ingredienser: Omeprazol
Nansen 20 mg gastroresistente kapsler
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN -
NANSEN 20 MG HARDE GASTRORESISTANTE KAPPELER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING -
Hver mave-resistente hård kapsel indeholder:
aktivt princip: omeprazol 20 mg.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM -
Hårde kapsler indeholdende gastro-resistente granulater.
04.0 KLINISKE OPLYSNINGER -
04.1 Terapeutiske indikationer -
NANSEN fås udelukkende som en 20 mg gastro-resistent hård kapselformulering.
NANSEN gastro-resistente hårde kapsler er indiceret til:
Voksne
• Behandling af sår på tolvfingertarmen
• Forebyggelse af gentagelse af duodenalsår
• Behandling af mavesår
• Forebyggelse af gentagelse af mavesår
• Udryddelse af Helicobacter pylori (H. pylori) ved mavesår i forbindelse med passende antibiotikabehandling
• Behandling af mavesår og duodenalsår forbundet med brug af NSAID
• Forebyggelse af mavesår og duodenalsår forbundet med brug af NSAID'er hos risikopatienter
• Behandling af refluksøsofagitis
• Langsigtet behandling af patienter med helet refluksøsofagitis
• Behandling af symptomatisk gastroøsofageal reflukssygdom
• Behandling af Zollinger-Ellisons syndrom
Pædiatrisk population
Børn over 1 år og med en kropsvægt ≥ 10 kg
• Behandling af refluksøsofagitis
• Symptomatisk behandling af halsbrand og sure opstød ved gastroøsofageal reflukssygdom
Børn og unge over 4 år
• Behandling af duodenalsår forårsaget af H. pylori, i forbindelse med antibiotikabehandling
04.2 Dosering og indgivelsesmåde -
Dosering
Behandling af sår på tolvfingertarmen
Den anbefalede dosis til patienter med aktivt duodenalsår er NANSEN 20 mg én gang dagligt. Hos de fleste patienter opnås sårheling inden for to uger efter behandlingens start. I tilfælde af sår, der ikke er helet helt under det første behandlingsforløb, opnås normalt helbredelse under langvarig behandling i yderligere to uger. Hos patienter med dårligt reagerende sår på tolvfingertarmen anbefales NANSEN 40 mg én gang dagligt, og helbredelse opnås normalt inden for fire uger.
Forebyggelse af tilbagefald af duodenalsår
Til forebyggelse af tilbagefald af duodenalsår hos negative patienter H. pylori eller når udryddelsen af H. pylori ikke mulig, er den anbefalede dosis NANSEN 20 mg en gang dagligt. Hos nogle patienter kan en dosis på 10 mg være tilstrækkelig. I tilfælde af terapeutisk svigt kan dosis øges til 40 mg.
Behandling af mavesår
Den anbefalede dosis er NANSEN 20 mg en gang dagligt. Hos de fleste patienter opnås helbredelse inden for fire uger efter behandlingens start. Ved sår, der ikke er helet fuldstændigt efter det første behandlingsforløb, opnås normalt helbredelse under forlænget behandling i yderligere fire uger. Hos patienter med sår. Gastrisk respons , administration af NANSEN 40 mg én gang dagligt anbefales, og helbredelse opnås generelt inden for otte uger.
Forebyggelse af tilbagefald hos patienter med mavesår
For at forhindre tilbagefald hos patienter med dårligt reagerende mavesår er den anbefalede dosis NANSEN 20 mg én gang dagligt. Om nødvendigt kan dosis øges til NANSEN 40 mg én gang dagligt.
Udryddelse af H. pylori i mavesår
Til "udryddelse af"H. pylori, Antibiotisk udvælgelse skal baseres på patientens individuelle lægemiddeltolerance, og behandlingen skal foretages i henhold til lokale, regionale, nationale resistensmønstre og behandlingsretningslinjer.
• NANSEN 20 mg + clarithromycin 500 mg + amoxicillin 1.000 mg hver to gange dagligt i en uge, eller
• NANSEN 20 mg + clarithromycin 250 mg (alternativt 500 mg) + metronidazol 400 mg (eller 500 mg eller tinidazol 500 mg), hver to gange dagligt i en uge, eller
• NANSEN 40 mg én gang dagligt med amoxicillin 500 mg og metronidazol 400 mg (eller 500 mg eller tinidazol 500 mg), begge tre gange om dagen i en uge.
Hvis patienten stadig tester positiv for hver af behandlingsregimerne H. pylori terapi kan gentages.
Behandling af mavesår og duodenalsår forbundet med indtagelse af NSAID
Til behandling af NSAID-associerede mavesår og duodenalsår er den anbefalede dosis NANSEN 20 mg én gang dagligt. Hos de fleste patienter opnås heling inden for fire uger efter behandlingsstart. Hos patienter, der ikke er helbredt efter det første behandlingsforløb, opnås normalt helbredelse ved at forlænge behandlingen i yderligere fire uger.
Forebyggelse af mavesår og duodenalsår forbundet med brug af NSAID'er hos risikopatienter
Til forebyggelse af mavesår eller duodenalsår forbundet med brug af NSAID'er hos risikopatienter (alder> 60 år, mavesår og duodenalsår, historie med øvre gastrointestinal blødning) er den anbefalede dosis NANSEN 20 mg én gang dagligt.
Behandling af refluksøsofagitis
Den anbefalede dosis er NANSEN 20 mg en gang dagligt. Hos de fleste patienter opnås helbredelse inden for fire uger efter behandlingens start. Ved sår, der ikke er helet helt efter det første behandlingsforløb, opnås normalt helbredelse ved at forlænge behandlingen i yderligere fire uger.
Hos patienter med alvorlig øsofagitis anbefales NANSEN 40 mg én gang dagligt for at opnå helbredelse normalt inden for otte uger.
Langsigtet behandling af patienter med helet refluksøsofagitis
Til langtidsbehandling af patienter med helet refluksøsofagitis er den anbefalede dosis NANSEN 10 mg én gang dagligt. Om nødvendigt kan dosis øges til NANSEN 20-40 mg én gang dagligt.
Behandling af symptomatisk gastroøsofageal reflukssygdom
Den anbefalede dosis er NANSEN 20 mg dagligt. Patienter kan reagere tilstrækkeligt på den daglige dosis på 10 mg, derfor bør individuel dosisjustering overvejes.
Hvis der ikke opnås symptomatisk kontrol efter fire ugers behandling med NANSEN 20 mg dagligt, anbefales yderligere undersøgelse.
Behandling af Zollinger-Ellisons syndrom
Hos patienter med Zollinger-Ellisons syndrom skal doseringen justeres individuelt, og behandlingen skal fortsættes så længe klinisk indiceret. Den anbefalede startdosis er NANSEN 60 mg pr. Dag. Alle patienter med alvorlig sygdom, der reagerede dårligt på andre behandlinger, opretholdt effektiv kontrol og kontrol blev opretholdt hos mere end 90% af patienterne med NANSEN -doser mellem 20 mg og 120 mg / dag. Daglige doser over 80 mg skal opdeles i to daglige administrationer
Pædiatrisk population
Børn over 1 år og med en kropsvægt ≥ 10 kg
Behandling af refluksøsofagitis
Symptomatisk behandling af halsbrand og sure opstød ved gastroøsofageal reflukssygdom
De anbefalede doser er som følger:
Refluks esophagitis: Behandlingsperioden er 4-8 uger.
Symptomatisk behandling af halsbrand og sure opstød ved gastroøsofageal reflukssygdom: Behandlingen varer 2-4 uger. Hvis der ikke opnås symptomatisk kontrol efter 2-4 uger, skal patienten undersøges nærmere.
Børn og unge over 4 år
Behandling af duodenalsår forårsaget af H. pylori
Officielle lokale, regionale og nationale retningslinjer vedrørende bakteriel resistens, behandlingsvarighed (oftest 7 dage, men undertiden op til 14 dage) og passende brug af antibiotika bør overvejes, når den korrekte kombinationsbehandling vælges.
Behandlingen skal udføres under opsyn af en specialist.
Den anbefalede dosering er som følger:
Særlige populationer
Nedsat nyrefunktion
Ingen dosisjustering er nødvendig hos patienter med nedsat nyrefunktion (se pkt. 5.2).
Nedsat leverfunktion
Hos patienter med nedsat leverfunktion kan en daglig dosis på 10-20 mg være tilstrækkelig (se pkt. 5.2).
Ældre (> 65 år)
Ingen dosisjustering er nødvendig hos ældre patienter (se pkt. 5.2).
Indgivelsesmåde
Det anbefales at tage NANSEN kapsler om morgenen, helst på tom mave, synkes hele med et halvt glas vand. Kapslerne må ikke tygges eller knuses.
Til patienter med synkebesvær og til børn, der kan drikke eller sluge halvfast mad
Patienter kan åbne kapslen og sluge indholdet med et halvt glas vand eller blandes med let sure væsker, såsom frugtsaft eller æblemos eller stille vand. Patienterne bør informeres om, at dispersionen i sådanne tilfælde skal sluges med det samme (eller inden for 30 minutter), og at den altid skal blandes lige før den drikkes. Skyl bunden med et halvt glas vand og drik indholdet.
Alternativt kan patienter opløse kapslen i munden og sluge de indeholdte granulater med et halvt glas vand. De mave-resistente granulater bør ikke tygges.
04.3 Kontraindikationer -
Overfølsomhed over for omeprazol, benzimidazolerstatninger eller over for et eller flere af hjælpestofferne.
Omeprazol bør, ligesom andre protonpumpehæmmere (PPI'er), ikke administreres samtidigt med nelfinavir (se pkt. 4.5).
04.4 Særlige advarsler og passende forholdsregler ved brug -
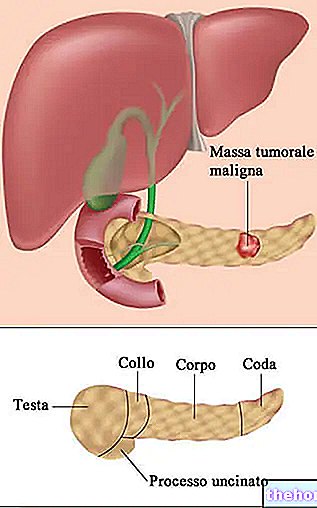
Ved tilstedeværelse af nogle alarmerende symptomer (f.eks. Betydeligt utilsigtet vægttab, tilbagevendende opkastning, dysfagi, hæmatemese eller melaena) og når der er mistanke om eller bekræftelse af tilstedeværelsen af et mavesår, bør sårets maligne karakter udelukkes i, hvordan den symptomatiske reaktion til behandling kan forsinke en korrekt diagnose.
Samtidig administration af atazanavir og protonpumpehæmmere anbefales ikke (se pkt. 4.5). Hvis kombinationen af atazanavir og protonpumpehæmmer vurderes uundgåelig, anbefales omhyggelig klinisk overvågning (f.eks. Viral belastning) i kombination med en stigning i atazanavir -dosis til 400 mg med 100 mg ritonavir; omeprazols dosis må ikke overstige 20 mg.
Omeprazol kan, ligesom alle syreundertrykkende lægemidler, reducere absorptionen af vitamin B12 (cyanocobalamin) på grund af hypo- eller achlorhydria.Dette bør tages i betragtning hos patienter med lave reserver eller risikofaktorer for reduceret vitaminoptagelse.B12 i tilfælde af langvarig -terminale terapier.
Omeprazol er en CYP2C19 -hæmmer. Potentiel interaktion med lægemidler, der metaboliseres af CYP2C19, bør overvejes ved start eller afslutning af behandling med omeprazol Der er observeret en interaktion mellem clopidogrel og omeprazol (se pkt. 4.5). Den kliniske relevans af denne interaktion er usikker. Som en sikkerhedsforanstaltning bør samtidig anvendelse af clopidogrel og omeprazol frarådes.
Interferens med laboratorietest
Det øgede CgA -niveau kan forstyrre undersøgelser af neuroendokrine tumorer. For at undgå denne interferens skal omeprazolbehandling stoppes mindst fem dage før starten af CgA -målinger (se pkt. 5.1).
Hypomagnesæmi
Protonpumpehæmmere (PPI'er) såsom omeprazol er blevet observeret for at forårsage alvorlig hypomagnesæmi hos patienter behandlet i mindst tre måneder og i mange tilfælde i et år.
Alvorlige symptomer på hypomagnesæmi omfatter træthed, tetany, delirium, kramper, svimmelhed og ventrikulær arytmi. De kan i første omgang manifestere sig lumsk og blive negligeret.
Hypomagnesæmi forbedres hos de fleste patienter efter at have taget magnesium og afbrudt protonpumpehæmmeren.
Sundhedspersonale bør overveje at måle magnesiumniveauer, før PPI -behandling påbegyndes og periodisk under behandling hos patienter i længerevarende behandling eller behandling med digoxin eller lægemidler, der kan forårsage hypomagnesæmi (f.eks. Diuretika). Alvorlig hypomagnesæmi kan forårsage hypocalcæmi.
Subakut kutan lupus erythematosus (SCLE)
Protonpumpehæmmere er forbundet med ekstremt sjældne tilfælde af SCLE. Ved tilstedeværelse af læsioner, især på hudens dele udsat for sollys, og hvis den ledsages af artralgi, skal patienten straks kontakte en læge, og sundhedspersonalet bør vurdere, om det er hensigtsmæssigt at stoppe behandlingen med Nansen. SCLE efter behandling med en protonpumpehæmmer kan øge risikoen for SCLE med andre protonpumpehæmmere.
Protonpumpehæmmere, især når de bruges i høje doser og i længere perioder (> 1 år), kan forårsage en lidt øget risiko for hofte-, håndleds- og rygsøjlefrakturer, især hos ældre patienter eller i nærvær af andre kendte risikofaktorer. Observationsstudier tyder på, at protonpumpehæmmere kan øge den samlede risiko for brud med 10% til 40%. Denne stigning kan delvis skyldes andre risikofaktorer.Patienter med risiko for knogleskørhed bør modtage behandling i henhold til gældende klinisk praksis retningslinjer og skal tage en "passende mængden af D -vitamin og calcium.
Nogle børn med kroniske tilstande kan have brug for langvarig behandling, selvom det ikke anbefales.
Behandling med protonpumpehæmmere kan forårsage en let øget risiko for gastrointestinale infektioner, f.eks Salmonella Og Campylobacter (se afsnit 5.1).
Som med alle langtidsbehandlinger, især hvis behandlingsvarigheden er større end 1 år, bør patienter overvåges regelmæssigt.
04.5 Interaktioner med andre lægemidler og andre former for interaktion -
Omeprazols indflydelse på andre aktive stoffers farmakokinetik
Aktive ingredienser med pH-afhængig absorption
Gastrisk pH-afhængig absorption af aktive stoffer kan øges eller reduceres ved nedsat intragastrisk surhed under behandling med omeprazol.
Nelfinavir, atazanavir
Plasmaniveauer af nelfinavir og atazanavir falder, når omeprazol administreres samtidigt.
Samtidig administration af omeprazol og nelfinavir er kontraindiceret (se pkt. 4.3). Samtidig administration af omeprazol (40 mg én gang dagligt) reducerede middeleksponeringen af nelfinavir med cirka 40% og reducerede den gennemsnitlige eksponering af den farmakologisk aktive metabolit M8 med cirka 75-90%. Interaktionen kan også involvere inhibering af CYP2C19.
Samtidig administration af omeprazol og atazanavir anbefales ikke (se pkt. 4.4). Samtidig administration af omeprazol (40 mg én gang dagligt) og atazanavir 300 mg / ritonavir 100 mg til raske frivillige resulterede i en reduktion i atazanavir-eksponeringen på 75%. Stigningen i atazanavirdosis til 400 mg opvejede ikke omeprazols indvirkning på atazanavirs eksponering . Samtidig administration af omeprazol (20 mg én gang dagligt) og atazanavir 400 mg / ritonavir 100 mg til raske frivillige resulterede i en reduktion på cirka 30% i eksponeringen af atazanavir sammenlignet med atazanavir 300 mg / ritonavir 100 mg én gang om dagen.
Digoxin
Samtidig behandling med omeprazol (20 mg / dag) og digoxin hos raske personer resulterede i en 10% stigning i biotilgængeligheden af digoxin. Digoxintoksicitet er sjældent blevet rapporteret. Der bør imidlertid udvises forsigtighed ved brug af høje doser omeprazol til ældre patienter, derfor bør terapeutisk monitorering af digoxin øges.
Clopidogrel
Resultater fra undersøgelser hos raske patienter viste en "farmakokinetisk (PK) / farmakodynamisk (PD) interaktion mellem clopidogrel (ladningsdosis 300 mg / vedligeholdelsesdosis 75 mg dagligt) og omeprazol (80 mg po dagligt), hvilket resulterede i et gennemsnitligt fald på 46 % i eksponering for den aktive metabolit af clopidogrel og i et gennemsnitligt fald på 16% i maksimal inhibering (ADP -induceret) af trombocytaggregation.
Divergerende data fra observations- og kliniske undersøgelser er blevet rapporteret om de kliniske konsekvenser af en PK / PD -interaktion af omeprazol med hensyn til større kardiovaskulære hændelser. Som en sikkerhedsforanstaltning bør samtidig anvendelse af omeprazol og clopidogrel frarådes (se pkt. 4.4).
Andre aktive ingredienser
Absorptionen af posaconazol, erlotinib, ketoconazol og itraconazol reduceres betydeligt, og derfor kan den kliniske effekt blive kompromitteret. Samtidig brug af posaconazol og erlotinib bør undgås.
Aktive stoffer metaboliseret af CYP2C19
Omeprazol er en moderat hæmmer af dets vigtigste metaboliserende enzym, CYP2C19. Derfor kan metabolismen af samtidige aktive stoffer, der også metaboliseres af CYP2C19, reduceres og systemisk eksponering for disse stoffer øges. Eksempler på sådanne lægemidler er R-warfarin og andre vitamin K-antagonister, cilostazol, diazepam og phenytoin.
Cilostazol
Omeprazol, givet i en dosis på 40 mg til raske frivillige i et cross-over-studie, øgede Cmax og AUC for cilostazol med henholdsvis 18% og 26% og en af dets aktive metabolitter med henholdsvis 29% og 69% ...
Phenytoin
Overvågning af phenytoin -plasmakoncentration anbefales i løbet af de første to uger efter start af omeprazolbehandling, og hvis en phenytoin -dosisjustering er påkrævet, anbefales monitorering og yderligere dosisjustering, når behandlingen afsluttes med omeprazol.
Mekanisme ukendt
Saquinavir
Samtidig administration af omeprazol og saquinavir / ritonavir resulterede i øgede plasmaniveauer af saquinavir op til cirka 70% med god tolerabilitet hos HIV-positive patienter.
Tacrolimus
Samtidig administration af omeprazol er rapporteret at øge serumniveauerne af tacrolimus. Overvågning af tacrolimuskoncentrationer og nyrefunktion (kreatininclearance) bør øges, og om nødvendigt skal tacrolimus -dosis justeres.
Methotrexat
Når det gives sammen med protonpumpehæmmere, er der rapporteret en stigning i methotrexatniveauer hos nogle patienter. Når methotrexat administreres i høje doser, kan det være nødvendigt at overveje en midlertidig seponering af omeprazol.
Indflydelse af andre aktive stoffer på omeprazols farmakokinetik
CYP2C19 og / eller CYP3A4 -hæmmere
Da omeprazol metaboliseres af CYP2C19 og CYP3A4, kan aktive stoffer, der hæmmer CYP2C19 eller CYP3A4 (såsom clarithromycin og voriconazol) øge serumniveauerne af omeprazol og reducere dets metabolisme. Samtidig administration af voriconazol resulterer i mere end fordoblet eksponering for omeprazol Da administration af høje doser omeprazol tolereres godt, er det generelt ikke nødvendigt med dosisjustering af omeprazol, men dosisjustering bør dog foretages. Overvejes hos patienter med svært nedsat leverfunktion og ved langtidsbehandling.
Inducere af CYP2C19 og / eller CYP3A4
Aktive stoffer, der inducerer CYP2C19 eller CYP3A4 eller begge dele (f.eks. Rifampicin og perikon) kan forårsage et fald i serumniveauerne af omeprazol og øge dets metaboliske hastighed.
04.6 Graviditet og amning -
Graviditet
Resultaterne af tre prospektive epidemiologiske undersøgelser (mere end 1000 eksponerede patientresultater) indikerer ingen negative virkninger af omeprazol på graviditet eller foster / nyfødt helbred. Omeprazol kan bruges under graviditet.
Fodringstid
Omeprazol udskilles i modermælk, men påvirker sandsynligvis ikke barnet, når det administreres i terapeutiske doser.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner -
Det er usandsynligt, at NANSEN påvirker evnen til at føre motorkøretøj eller betjene maskiner. Bivirkninger som svimmelhed og synsforstyrrelser kan forekomme (se pkt.4.8). Hvis de lider af det, bør patienter ikke køre bil eller betjene maskiner.
04.8 Bivirkninger -
De mest almindelige bivirkninger (1-10% af patienterne) er hovedpine, mavesmerter, forstoppelse, diarré, flatulens, kvalme / opkastning.
Følgende bivirkninger, identificeret eller mistænkt, er blevet fremhævet under kliniske forsøg med omeprazol og efter markedsføring. Der blev under ingen omstændigheder konstateret en sammenhæng med den administrerede lægemiddeldosis. Bivirkninger er klassificeret efter frekvens og organklassifikationssystem (SOC). Hyppighedskategorier defineres ved hjælp af følgende konvention: Meget almindelig (≥1 / 10), Almindelig (≥1 / 100 til
SOC / frekvens Bivirkninger
Forstyrrelser i blod og lymfesystem
Sjælden: leukopeni, trombocytopeni
Meget sjælden: Agranulocytose, pancytopeni
Forstyrrelser i immunsystemet
Sjælden: Overfølsomhedsreaktioner, fx feber, angioødem og anafylaktisk reaktion / chok
Metabolisme og ernæringsforstyrrelser
Sjælden: Hyponatriæmi
Ikke kendt: Hypomagnesiæmi (se pkt. 4.4 Særlige advarsler og forsigtighedsregler ved brug); hypokalcæmi *
Psykiatriske lidelser
Ikke almindelig: Søvnløshed
Sjælden: Agitation, forvirring, depression
Meget sjælden: Aggression, hallucinationer
Nervesystemet lidelser
Almindelig: Hovedpine
Ikke almindelig: Svimmelhed, paræstesi, søvnighed
Sjælden: Ændringer i smag
Øjenlidelser
Sjælden: Sløret syn
Øre- og labyrintforstyrrelser
Ikke almindelig: Svimmelhed
Åndedræts-, thorax- og mediastinumforstyrrelser
Sjælden: Bronkospasme
Gastrointestinale lidelser
Almindelig: Mavesmerter, forstoppelse, diarré, flatulens, kvalme / opkastning
Sjælden: Tør mund, stomatitis, gastrointestinal candidiasis
Ikke kendt: Mikroskopisk colitis
Lever- og galdeforstyrrelser
Ikke almindelig: Forhøjelse af leverenzymer
Sjælden: Hepatitis med eller uden gulsot
Meget sjælden: Hepatisk svigt, encefalopati hos patienter med allerede eksisterende leversygdom
Hud og subkutan væv
Ikke almindelig: Dermatitis, kløe, udslæt, urticaria
Sjælden: Alopeci, lysfølsomhed
Meget sjælden: Erythema multiforme, Stevens-Johnsons syndrom, toksisk epidermal nekrolyse (TEN)
Hyppighed "ikke kendt": subakut kutan lupus erythematosus (se pkt. 4.4).
Muskuloskeletale og bindevævssygdomme
Ikke almindelig: Brud på hofte, håndled eller rygsøjle (se pkt. 4.4 Særlige advarsler og forsigtighedsregler ved brug)
Sjælden: Artralgi, myalgi
Meget sjælden: Muskelsvaghed
Nyre- og urinlidelser
Sjælden: Interstitiel nefritis
Sygdomme i reproduktive system og bryst
Meget sjælden: Gynækomasti
Generelle lidelser og tilstande på administrationsstedet
Ikke almindelig: Ubehag, perifert ødem
Sjælden: Øget svedtendens
* hypocalcæmi kan skyldes alvorlig hypomagnesæmi.
Pædiatrisk population
Sikkerheden ved omeprazol blev vurderet hos i alt 310 børn i alderen 0 til 16 år med syrerelateret sygdom. Begrænsede langtidsdata er tilgængelige om 46 børn, der modtog omeprazol-vedligeholdelsesbehandling i op til 749 dage i et klinisk studie med alvorlig erosiv esophagitis. Bivirkningsprofilen var generelt den samme som hos voksne. Både på kort og lang sigt behandling Der er ingen langsigtede data vedrørende virkningerne af omeprazolbehandling på puberteten og væksten.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det giver mulighed for løbende overvågning af fordelene / risikobalancen ved lægemidlet. Sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Adresse www. agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering -
Der findes begrænsede oplysninger om overdosering med omeprazol til mennesker.
Doser på op til 560 mg er rapporteret i litteraturen, og der har lejlighedsvis været rapporter om enkelte orale doser op til 2400 mg omeprazol (120 gange den normalt anbefalede kliniske dosis). Kvalme, opkastning, svimmelhed, mavesmerter, diarré og hovedpine er blevet rapporteret. I individuelle tilfælde blev der også observeret apati, depression og forvirring.
De beskrevne symptomer var forbigående, og der blev ikke rapporteret om alvorlige konsekvenser.
Med stigende doser ændredes eliminationshastigheden ikke (første ordens kinetik).
Behandling er om nødvendigt symptomatisk.
05.0 FARMAKOLOGISKE EGENSKABER -
05.1 "Farmakodynamiske egenskaber -
Farmakoterapeutisk gruppe: protonpumpehæmmer.
ATC -kode: A02BC01.
Handlingsmekanisme
Omeprazol, en racemisk blanding af to aktive enantiomerer, reducerer mavesyresekretion med en højt specialiseret virkningsmekanisme. Omeprazol er en specifik hæmmer af protonpumper i parietalcellerne i maven.
Det virker hurtigt og fremmer en reversibel kontrol af hæmningen af mavesyresekretion med en enkelt daglig administration.
Omeprazol er en svag base og koncentreres og omdannes til den aktive form i det meget sure miljø i de intracellulære canaliculi i parietalcellerne, hvor det hæmmer H +, K + - ATPase - protonpumpen. Denne handling på det sidste trin i saltsyredannelsesprocessen er dosisafhængig og forårsager en yderst effektiv inhibering af syresekretion, både af den basale og af den stimulerede, uanset den anvendte stimulus.
Farmakodynamiske virkninger
Alle observerede farmakodynamiske virkninger skyldes omeprazols aktivitet på syresekretion.
Virkninger på mavesyresekretion
Den orale administration af omeprazol en gang dagligt tillader en hurtig og effektiv hæmning af mavesyresekretion dag og nat, som når sit maksimum inden for de første 4 dage af behandlingen.
Hos patienter, der lider af duodenalsår, opretholdt administrationen af 20 mg omeprazol en gennemsnitlig reduktion på 80% i intragastrisk surhed over 24 timer; 24 timer efter administration af omeprazol reduceres toppen af syresekretion efter stimulering med pentagastrin i gennemsnit med ca. 70%.
Oral administration af 20 mg omeprazol fastholder den intragastriske pH ved ≥ 3 i en gennemsnitlig tid på 17 timer ud af 24 hos patienter med duodenalsår.
Som en konsekvens af nedsat syresekretion og intragastrisk surhed reducerer / normaliserer omeprazol dosisafhængig syreeksponering af spiserøret hos patienter med gastroøsofageal reflukssygdom.
Inhibering af syresekretion er relateret til plasmakoncentration / tidskurve (AUC) for omeprazol og ikke til den faktiske plasmakoncentration på et givet tidspunkt.
Der blev ikke observeret takyfylaksi under behandling med omeprazol.
Virkninger på Helicobacter pylori
Helicobacter pylori det er forbundet med mavesyresygdom, der omfatter duodenalsårssygdom og mavesårssygdom.
Helicobacter pylori det betragtes som den største synder i udviklingen af gastritis.
Helicobacter pylori sammen med mavesyresekretion repræsenterer de de vigtigste faktorer for udviklingen af mavesårssygdom.
Helicobacter pylori det er hovedfaktoren i udviklingen af atrofisk gastritis, som er forbundet med en øget risiko for at udvikle gastriske tumorer.
Udryddelsen af Helicobacter pylori med omeprazol og antimikrobielle midler er det forbundet med en "høj grad af ardannelse og langvarig remission af mavesår.
De undersøgte dobbeltterapier viste mindre effektivitet end trippelterapierne. De kan dog tages i betragtning, hvis kendt overfølsomhed udelukker brug af en tredobbelt kombination.
Andre effekter relateret til syrehæmning
Under langtidsbehandling er der observeret en stigning i hyppigheden af gastriske kirtelcyster, som repræsenterer den fysiologiske konsekvens af den udtalte hæmning af syresekretion. Disse formationer er godartede og reversible i naturen.
Faldet i mavesyren af enhver oprindelse, herunder den på grund af protonpumpehæmmere, øger den gastriske bakterielle belastning, der normalt er til stede i mave -tarmkanalen. Behandling med syrereducerende lægemidler kan forårsage en let øget risiko for gastrointestinale infektioner Salmonella og Campylobacter.
Under behandling med antisekretoriske lægemidler øges serumgastrin som reaktion på nedsat syresekretion. Chromogranin A (CgA) stiger også på grund af nedsat mavesyre. Det øgede CgA -niveau kan forstyrre undersøgelser af neuroendokrine tumorer. Rapporter fra litteraturen indikerer, at behandlingen med protonpumpehæmmeren skal stoppes mindst fem dage før starten af CgA -målinger. CgA og gastrin normaliseres ikke efter 5 dage, målinger skal gentages 14 dage efter stop af omeprazolbehandling.
En stigning i antallet af ECL-celler, muligvis relateret til en stigning i serumgastrinniveauer, er blevet observeret hos nogle patienter (både børn og voksne) under langtidsbehandling med omeprazol.
Pædiatrisk population
I en ukontrolleret undersøgelse med børn (1 til 16 år) med alvorlig refluksøsofagitis forbedrede omeprazol i doser på 0,7 til 1,4 mg / kg graden af esophagitis i 90% af tilfældene og reducerede signifikant tilbagesvalingssymptomer. I en enkeltblind undersøgelse blev børn i alderen 0-24 måneder med klinisk diagnosticeret refluksøsofagitis behandlet med 0,5, 1,0 eller 1,5 mg omeprazol / kg. Hyppigheden af opkast / opkastningsepisoder faldt med 50% efter 8 ugers behandling, uanset dosis.
Udryddelse af H. pylori hos børn
Et dobbeltblindet, randomiseret klinisk forsøg (Héliot-undersøgelse) viste, at omeprazol i kombination med to antibiotika (amoxicillin og claritromycin) er effektivt og sikkert til behandling af H. pylori-infektion hos børn i alderen 4 år og derover med gastritis: udryddelseshastighed af "H. pylori: 74,2% (23/31 patienter) med omeprazol + amoxicillin + clarithromycin mod 9,4% (3/32 patienter) med amoxicillin + clarithromycin. Imidlertid er der ikke påvist nogen klinisk fordel med hensyn til dyspeptiske symptomer. Denne undersøgelse understøtter ikke oplysninger til børn under 4 år.
05.2 "Farmakokinetiske egenskaber -
Absorption
Omeprazol og omeprazolmagnesium er følsomme over for det sure miljø og administreres derfor oralt i form af gastro-resistente granulater indeholdt i kapsler eller tabletter.
Absorptionen af omeprazol er hurtig, med maksimale plasmaniveauer synlige cirka 1-2 timer efter dosering. Absorption af omeprazol forekommer i tyndtarmen og afsluttes generelt inden for 3-6 timer. Samtidig madindtag påvirker ikke lægemidlets biotilgængelighed. Systemisk tilgængelighed (biotilgængelighed) efter en enkelt oral dosis omeprazol er cirka 40%. Efter gentagne daglige administrationer stiger biotilgængeligheden til ca. 60%.
Fordeling
Den tilsyneladende fordelingsvolumen hos raske personer er ca. 0,3 l / kg legemsvægt. 97% af omeprazol er bundet til plasmaproteiner.
Biotransformation
Omeprazol metaboliseres fuldstændigt af cytochrom P450 (CYP) -systemet. Det meste af omeprazols metabolisme er afhængig af den specifikke polymorf udtrykte CYP2C19 -isoform, der er ansvarlig for dannelsen af hydroxyomeprazol, som er den største plasmametabolit. Resten afhænger af en anden specifik isoform, CYP3A4, der er ansvarlig for dannelsen af omeprazolsulfon. Som en konsekvens af omeprazols høje affinitet for CYP2C19 er der et potentiale for konkurrencedygtig hæmning og stof-stofskifte metabolisk interaktion mellem omeprazol og andre substrater af CYP2C19. På grund af sin lave affinitet til CYP3A4 har omeprazol imidlertid ikke evnen til at hæmme metabolismen af andre CYP3A4 -substrater. Desuden har omeprazol ingen hæmmende effekt på større CYP -enzymer.
Cirka 3% af den kaukasiske befolkning og 15-20% af den asiatiske befolkning har en funktionel mangel på CYP2C19-enzymet og defineres således som dårlige metaboliserere. Hos disse individer er metabolismen af omeprazol sandsynligvis mere katalyseret af CYP3A4. Efter gentagen administration . på 20 mg omeprazol en gang dagligt var den gennemsnitlige AUC 5 til 10 gange højere hos dårlige metaboliserere end hos personer med et funktionelt CYP2C19 -enzym (omfattende metaboliserere). Maksimal plasmakoncentration var 3 til 5 gange højere. Disse resultater har ingen konsekvenser for doseringen af omeprazol.
Eliminering
Plasmaelimineringshalveringstiden for omeprazol er normalt mindre end en time efter både enkelt og gentagen oral dosering én gang dagligt. Omeprazol fjernes fuldstændigt fra plasmaet mellem doserne, og derfor er der ingen tendens til akkumulering under en gang daglig administration. Ca. 80% af en oral dosis omeprazol udskilles i urinen som metabolitter, resten findes i fæces og stammer primært fra galdeudskillelse.
AUC for omeprazol stiger efter gentagen administration. Denne stigning er dosisafhængig og resulterer i et ikke-lineært dosis-AUC-forhold efter gentagen administration. Afhængigheden af tid og dosis skyldes et fald i first-pass metabolisme og systemisk clearance. Sandsynligvis forårsaget af en inhibering af CYP2C19 -enzymet med omeprazol og / eller dets metabolitter (f.eks. sulfon).
Ingen effekt af metabolitter på mavesyresekretion blev observeret.
Særlige populationer
Nedsat leverfunktion
Hos patienter med nedsat leverfunktion er omeprazols metabolisme nedsat, hvilket resulterer i en stigning i AUC.Der var ingen tendens til at akkumulere, når omeprazol blev administreret en gang dagligt.
Nedsat nyrefunktion
Farmakokinetikken for omeprazol, herunder systemisk biotilgængelighed og eliminationshastighed, ændres ikke hos patienter med nedsat nyrefunktion.
Ældre borgere
Metabolske hastighed for omeprazol er let reduceret hos ældre (75-79 år).
Pædiatrisk population
Under behandlingen af børn fra 1 år ved anbefalede doser blev plasmakoncentrationer, der var sammenlignelige med voksne, observeret. Hos børn under 6 måneder var omeprazols clearance reduceret på grund af den dårlige metaboliske kapacitet af omeprazol.
05.3 Prækliniske sikkerhedsdata -
Gastrisk ECL -cellehyperplasi og carcinoider blev påvist i forsøg med rotter, der blev behandlet for livet med omeprazol. Disse ændringer er resultatet af høj hypergastrinæmi sekundært til syrehæmning. Lignende observationer blev opnået efter behandling med H2 -antagonister, protonpumpehæmmere og efter delvis fundusresektion. Disse ændringer kan derfor ikke tilskrives en direkte virkning af en enkelt aktiv ingrediens.
06.0 LÆGEMIDDELOPLYSNINGER -
06.1 Hjælpestoffer -
NANSEN 20 mg hårde gastro-resistente kapsler
Hver kapsel indeholder følgende hjælpestoffer:
Kerne : mikrokrystallinsk cellulose, lavsubstitueret hydroxypropylcellulose, mannitol, croscarmellosenatrium, polysorbat 80, povidon K-30, arginin, natriumlaurylsulfat, glycin, let magnesiumcarbonat.
Belægning : hypromellose, methacrylsyre-ethylacrylatcopolymer, triethylcitrat, natriumhydroxid, titandioxid, talkum.
Kapsel : gelatine, indigo karmin (E-132), titandioxid, vand.
06.2 Uforenelighed "-
Ikke anvendelig.
06.3 Gyldighedsperiode "-
I intakt emballage: 2 år.
Den angivne udløbsdato refererer til produktet i intakt og korrekt opbevaret emballage.
06.4 Særlige opbevaringsforhold -
Opbevares ved en temperatur, der ikke overstiger 30 ° C.
Opbevares i den originale emballage for at beskytte medicinen mod fugt.
06.5 Den umiddelbare emballages art og emballagens indhold -
PVC-AL-PA / AL-AL blister; æske med 14 kapsler.
06.6 Brugsanvisning og håndtering -
Ingen særlige instruktioner
07.0 INDEHAVER AF "MARKEDSFØRINGSTILLADELSEN" -
S.F. GROUP Srl - Via Tiburtina, 1143 - 00156 Rom
08.0 MARKEDSFØRINGSTILLADELSESNUMMER -
NANSEN 20 mg gastro-resistente hårde kapsler, 14 kapsler A.I.C.: 037907019
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN -
Dato for første godkendelse: 20/12/2007
10.0 DATO FOR REVISION AF TEKSTEN -
Januar 2016














.jpg)