Aktive ingredienser: Total triterpenfraktion af Centella asiatica
Centellase 30 mg tabletter
Hvorfor bruges Centellase? Hvad er det for?
Centellase er en medicin baseret på Centella asiatica, et lægemiddel, der bruges til at beskytte venerne.
Centellase er indiceret til behandling af:
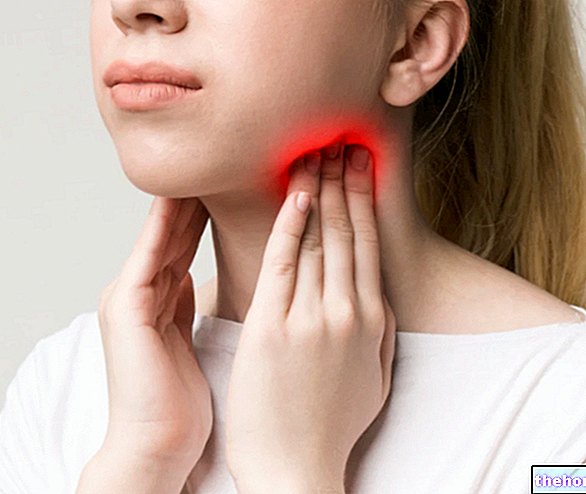
- hævelse i ankler og ben på grund af venøs insufficiens, følelse af tyngde i benene, prikken og kløe i benene, natlige kramper i benet og synlige kapillærer;
- skrøbelighed af kapillærer.
Tal med din læge, hvis du ikke har det bedre, eller hvis du har det dårligere.
Kontraindikationer Når Centellase ikke bør bruges
Tag ikke Centellase
- hvis du er allergisk over for det aktive stof eller et af de øvrige indholdsstoffer i dette lægemiddel
Forholdsregler ved brug Hvad du skal vide, før du tager Centellase
Der er ingen særlige forholdsregler for brugen af dette lægemiddel.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Centellase
Fortæl det til din læge eller apotek, hvis du tager anden medicin eller har brugt det for nylig.
Advarsler Det er vigtigt at vide, at:
Graviditet, amning og fertilitet
Brug ikke denne medicin under graviditet og amning, fordi dens virkning ikke er kendt.
hvis du er gravid eller ammer, har mistanke om, at du er gravid eller planlægger at blive gravid, skal du spørge din læge eller apotek til råds, før du tager denne medicin.
Kørsel og brug af maskiner
Centellase påvirker ikke evnen til at føre motorkøretøj eller betjene maskiner.
Dosis, metode og administrationstidspunkt Sådan bruges Centellase: Dosering
Tag altid denne medicin nøjagtigt som beskrevet i denne indlægsseddel eller som anvist af din læge eller apotek. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Den anbefalede dosis er 1 til 2 tabletter om dagen, helst ved måltider.
Sådan bruges: Tabletterne skal synkes hele med vand
Behandlingens varighed: Brug denne medicin kun i korte behandlingsperioder. Kontakt din læge, hvis lidelsen opstår gentagne gange, eller hvis du har bemærket nylige ændringer i dens egenskaber.
Bivirkninger Hvad er bivirkningerne af Centellase
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Anvendelsen af medicinen kan forårsage kløe eller forårsage fænomener med følsomhed over for solen og UV -stråler (fotosensibilisering) med udseende af rødme og røde og / eller hævede pletter (hududslæt).
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, som ikke er nævnt i denne indlægsseddel. Du kan også indberette bivirkninger direkte via webstedet: https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. Ved at rapportere bivirkninger kan du hjælpe med at give flere oplysninger om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Denne medicin kræver ingen særlige opbevaringsbetingelser.
Opbevar denne medicin utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen efter "EXP". Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Hvad Centellase indeholder
- Den aktive ingrediens er: total triterpenfraktion af Centella asiatica
- Øvrige indholdsstoffer er: dibasisk calciumphosphatdihydrat, docusatnatrium, povidon, croscarmellosenatrium, carmellosenatrium, magnesiumstearat.
Hvordan Centellase ser ud og pakningens indhold
Centellase kommer i en papæske med 30 tabletter pakket i blisterpakninger.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
CENTELLASE TABLETTER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
1 tablet indeholder: total triterpenfraktion af gotu kola (asiaticosid 40% - asiatisk syre + madecassinsyre 60%) 30 mg.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Tabletter.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Symptomer, der skyldes venøs insufficiens; tilstander af kapillær skrøbelighed.
04.2 Dosering og indgivelsesmåde
Dosering
1 til 2 tabletter om dagen, helst ved måltider.
Lægemidlet bør kun bruges i en kort behandlingsperiode.
Indgivelsesmåde: oral anvendelse.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug
Ingen særlige forholdsregler ved brug af produktet.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Der er ingen kendte interaktioner med andre lægemidler.
04.6 Graviditet og amning
Dyrestudier har ikke vist reproduktionstoksicitet. Der er ikke tilstrækkelige data om brugen af lægemidlet til gravide eller ammende kvinder. Centellase bør ikke anvendes under graviditet og amning.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Centellase påvirker ikke evnen til at føre motorkøretøj eller betjene maskiner.
04.8 Bivirkninger
Tilfælde af kløe og lysfølsomhedsreaktioner med udseende af rødme og udslæt er blevet rapporteret efter oral administration af lægemidlet.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets fordel / risiko -balance. Sundhedspersonale bedes rapportere alle formodede bivirkninger via det nationale rapporteringssystem. "Adresse: http : //www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
Der er ikke rapporteret tilfælde af overdosering.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: vasoprotektorer.
ATC -kode: C05CX.
Handlingsmekanisme
Triterpenfraktionen af Centella asiatica (FTTCA) har modulerende egenskaber på udviklingen af bindevæv, hvilket resulterer i en forbedring af tonen og elasticiteten i den venøse væg. kapillærniveauet), for med tiden at genoprette den hæmodynamiske ligevægt på niveauet af vævets mikro-vaskulære system, hvis ændring er årsagen til den symptomatologi, der ledsager varicose syndromet.
05.2 Farmakokinetiske egenskaber
Absorption
FTTCA absorberes hurtigt efter oral administration og når det maksimale plasmaniveau omkring 4 timer. Efter epikutan administration viser produktet en blodtop mellem den 6. og 12. time.
Biotransformation og eliminering
De aktive ingredienser metaboliseres ikke af kroppen og elimineres som sådan via fækal vej.
En entero-hepatisk cirkulation er blevet påvist.
05.3 Prækliniske sikkerhedsdata
Der er ingen information, der stammer fra prækliniske data, af væsentlig betydning for lægen, som ikke allerede er blevet rapporteret i de andre afsnit af produktresuméet.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Calciumdibasisk phosphatdihydrat, docusatnatrium, povidon, croscarmellosenatrium, carmellosenatrium, magnesiumstearat.
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
5 år.
06.4 Særlige opbevaringsforhold
Denne medicin kræver ingen særlige opbevaringsbetingelser.
06.5 Den umiddelbare emballages art og emballagens indhold
Tabletterne er omsluttet af plastmateriale, der er varmeforseglet med aluminium (blister) og anbragt i en papkasse sammen med indlægssedlen.
Æske med 30 tabletter.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner til bortskaffelse.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Farmaceutisk laboratorium SIT S.r.l. - Via Cavour, 70 - 27035 Mede (PV)
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
AIC: 016222073
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: november 1982.
Dato for seneste fornyelse: maj 2010.
10.0 DATO FOR REVISION AF TEKSTEN
AIFA -afgørelse af 21. juli 2014.