Aktive ingredienser: Pyridostigmin (Pyridostigminbromid)
MESTINON 60 mg tabletter
MESTINON 180 mg depottabletter
Hvorfor bruges Mestinon? Hvad er det for?
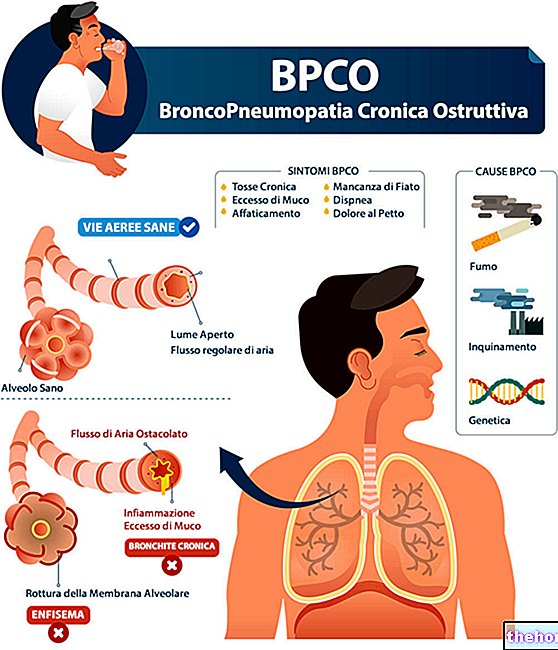
MESTINON indeholder det aktive stof pyridostigminbromid, en hæmmer af enzymet acetylcholinesterase Dette enzym inaktiverer acetylcholin, et stof, der er nødvendigt for muskelstimulering.
MESTINON er indiceret til behandlingen:
- myasthenia gravis, en alvorlig sygdom, der påvirker musklerne og viser sig som svaghed, træthed og kan føre til lammelse;
MESTINON 60 mg tabletter er også indiceret til behandlingen:
- tarmatoni (mangel på afføring, der forårsager tarmobstruktion).
Tal med din læge, hvis du ikke har det bedre, eller hvis du har det dårligere.
Kontraindikationer Når Mestinon ikke bør anvendes
Tag ikke MESTINON
- hvis du er allergisk over for pyridostigminbromid eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i afsnit 6)
- hvis du er allergisk over for medicin, der ligner pyrodostigmin;
- hvis du har en "mekanisk obstruktion af maven eller tarmene" (mave -tarmkanalen) pga. f.eks. tarmadhæsioner, tarm- eller ekstratarm-tumorer, mave- eller tarmbrok);
- hvis du lider af spastisk bronkitis (betændelse i bronkierne og luftrøret med vejrtrækningsbesvær)
- hvis du lider af bronchial astma (en luftvejssygdom manifesteret ved hoste, hvæsen, åndenød og tæthed i brystet)
- hvis du lider af mavesår (en mavesår)
- hvis du lider af thyrotoksikose (en tilstand, der forårsager en stigning i de hormoner, der produceres af skjoldbruskkirtlen i kroppen)
- hvis du lider af hjertesvigt (en alvorlig hjertesygdom)
- hvis du har haft et hjerteanfald
- hvis du lider af bradykardi (nedsat puls, dvs. antallet af hjerteslag i minuttet)
- hvis du har diabetes (en "ændring i blodsukker);
- hvis du har opereret mave eller tarm
- hvis du skal opereres med anæstesi (se "Anden medicin og MESTINON").
Tal med din læge, hvis du ikke har det bedre, eller hvis du har det dårligere.
Forholdsregler ved brug Hvad du skal vide, før du tager Mestinon
Tal med din læge eller apotek, før du tager MESTINON, hvis du har:
- en lungesygdom kaldet kronisk obstruktiv lungesygdom (KOL);
- arytmier (ændret puls, dvs. antallet af hjerteslag pr. minut;
- en nylig okklusion af kranspulsårerne (hjertets blodkar);
- hypotension (lavt blodtryk);
- vagotoni (særlig tilstand af funktionel balance i nervesystemet);
- mavesår (mavesår);
- epilepsi (anfald)
- Parkinsons (en sygdom i nervesystemet);
- Hypertyreose (øget skjoldbruskkirtelaktivitet);
- Nyresvigt (nedsat funktion af nyrerne).
Der er ingen oplysninger om administration af MESTINON til patienter med kontaktlinser.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Mestinon
Fortæl det til din læge eller apotek, hvis du tager anden medicin eller har brugt det for nylig.
Kontakt din læge eller apotek, hvis du tager følgende medicin:
- methylcellulose (et lægemiddel til behandling af forstoppelse);
- atropin og hyoscin (medicin, der ændrer muskulaturens kontraktilitet);
- pancuronium og vecuronium (medicin, der lindrer musklerne);
- morfin (smertestillende middel);
- barbiturater (medicin, der bruges til at fremkalde søvn);
- ether (et bedøvelsesmiddel).
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Hvis du er gravid eller ammer, tror at du er gravid eller planlægger at blive gravid, skal du spørge din læge eller apotek til råds, før du tager denne medicin.
Sikkerheden ved brug af MESTINON under graviditet er ikke fastslået
. Administration under graviditet bør kun overvejes, hvis den forventede fordel for moderen opvejer risikoen for fosteret, derfor i tilfælde af reelt behov og under direkte lægeligt tilsyn.
Sikkerheden ved at bruge MESTINON under amning er ikke fastslået.
Selvom kun ubetydelige mængder pyridostigmin udskilles i modermælk, skal der tages hensyn til mulige bivirkninger hos spædbørn.
Kørsel og brug af maskiner
Undgå at køre bil eller betjene maskiner, hvis du oplever uønskede virkninger såsom nedsat pupildiameter (miose) og vanskeligheder med at fokusere billeder (imødekommende defekter) under behandling med MESTINON, eller hvis du har "utilfredsstillende symptomkontrol af din sygdom (myastheni). Alvorlig).
MESTINON 60 mg tabletter indeholder lactose
Hvis din læge har fortalt dig, at du ikke tåler nogle sukkerarter, skal du kontakte din læge, inden du tager dette lægemiddel.
Dosering og anvendelsesmåde Sådan bruges Mestinon: Dosering
Tag altid dette lægemiddel nøjagtigt efter lægens eller apotekspersonalets anvisning.
Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Din læge vil finde frem til den bedst egnede dosis og hyppighed for dig.
MESTINON 60 mg tabletter
- Behandling af myasthenia gravis: den anbefalede dosis er: 1 - 3 tabletter, 2 - 4 gange om dagen. Din læge kan beslutte at øge denne dosis afhængigt af sygdommens sværhedsgrad.
- Behandling af tarmatoni: den anbefalede dosis er: 1 tablet hver 4. time.
MESTINON 180 mg depottabletter
- Behandling af myasthenia gravis: den anbefalede dosis er: 1 - 3 depottabletter 2 gange dagligt. Din læge vil beslutte den mest passende dosis for dig afhængigt af sygdommens sværhedsgrad, og om dit helbred forbedres som følge af at tage denne medicin.
Hvis du har nyresygdom, vil din læge beslutte den bedst egnede dosis. Hvis du har en alvorlig sygdom, kan din læge ordinere passende tests for at skræddersy den behandling, der er bedst for dig.
Mestinon tabletter skal tages med vand (et halvt glas eller et glas vand).
Tabletten med depottabletter kan opdeles i lige store dele, men den må ikke opdeles yderligere, da dette ville kompromittere den forsinkede frigivelse af det aktive stof.
Hvis du har glemt at tage MESTINON
Tag ikke en dobbeltdosis som erstatning for en glemt dosis.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Overdosering Hvad skal man gøre, hvis man har taget for meget Mestinon
I tilfælde af utilsigtet indtagelse / indtagelse af en overdosis MESTINON, skal du straks underrette din læge eller gå til det nærmeste hospital, da de symptomer, du kan opleve, kan ligner dem på din sygdom.
De symptomer, det kan manifestere, er:
- muskelhypotoni (muskelsvind) paradoksale symptomer (forværring af symptomer, som det behandles for)
- reduktion i antallet af hjerteslag i minuttet (bradykardi), hvilket kan gå så langt som at stoppe slagene (hjertesvigt)
- øget antal hjerteslag i minuttet (takykardi)
- nedsat blodtryk op til alvorlig nedsættelse af hjertefunktionen
- indsnævring af bronkierne, hvilket forårsager alvorlige vejrtrækningsbesvær (bronkospasme)
- overdreven spytproduktion (savlende)
- rive
- overdreven slimproduktion fra næsen (løbende næse)
- overdreven svedtendens
- rødme i huden
- mangel på styrke (adynamia)
- reduktion i pupildiameter (miose) og vanskeligheder med at fokusere billeder
- svimmelhed
- Han trak sig tilbage
- diarré
- kvalme
- inkontinens (tab af blære og anus kontrol)
- tenesmus (smertefuld krampe i anus og blære med en konstant følelse af at skulle afføring eller urinere)
- lungeødem (væske i lungerne)
- muskelkramper
- mavekramper
- fascikulationer (hurtige og ufrivillige sammentrækninger af musklerne)
- øget peristaltik (øget tarmmotilitet)
- øget bronkial sekretion
- generel svaghed op til lammelse
- apnø (standsning af vejrtrækning)
- hjerneanoxi (mangel på ilt til hjernen)
- agitation
- forvirring
- dysartri (taleforstyrrelse)
- nervøsitet
- irritation
- visuelle hallucinationer
- kramper
- koma.
Bivirkninger Hvad er bivirkningerne af Mestinon
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Følgende bivirkninger er blevet rapporteret og rapporteret med følgende frekvenser:
Sjælden (kan forekomme hos op til 1 ud af 1.000 patienter)
- Hududslæt (udslæt).
Frekvens ikke kendt (frekvens kan ikke estimeres ud fra de tilgængelige data)
- Overfølsomhed (allergi) over for lægemidlet;
- Synkope (forbigående bevidsthedstab);
- Miose (reduktion i pupillens diameter);
- Øget tåreflåd;
- Forstyrrelser i indkvartering (vanskeligheder med at fokusere billeder);
- Arytmier (ændret puls) såsom bradykardi (nedsat antal slag), takykardi (øget antal slag), atrioventrikulær blok (ledningsfejl i hjertet);
- Angina Prinzmetal (brystsmerter);
- Rødme;
- Hypotension (fald i blodtryk),
- Øget bronkial sekretion forbundet med bronkial indsnævring (indsnævring af bronkiernes kaliber);
- Kvalme;
- Han trak sig tilbage;
- Diarré;
- Øget peristaltik (tarmens motilitet);
- Sialorrhea (øget salivation);
- Ubehag i maven;
- Mavekramper
- Øget svedtendens;
- Nældefeber (hududslæt);
- Øget muskelsvaghed;
- Fascikulationer (hurtige og ufrivillige sammentrækninger af musklerne);
- Rystelser
- Muskelkramper
- Muskelhypotoni (nedsat muskeltonus);
- Blære tenesmus (trang til at tisse)
Indberetning af bivirkninger
Tal med din læge eller apotek, hvis du får bivirkninger, herunder mulige bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også indberette bivirkninger direkte via det nationale rapporteringssystem på www.agenziafarmaco.gov.it/it/responsabili. Ved at rapportere bivirkninger kan du hjælpe med at give mere information om lægemidlets sikkerhed.
Udløb og opbevaring
Opbevar denne medicin utilgængeligt for børn.
MESTINON 180 mg depottabletter
Må ikke opbevares ved temperaturer på højst 25 ° C. Beskyttes mod fugt.
MESTINON 60 mg tabletter
Dette lægemiddel kræver ingen særlige opbevaringsbetingelser.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen efter EXP. Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Smid ikke medicin i spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal bortskaffe medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Deadline "> Andre oplysninger
MESTINON indeholder
MESTINON 60 mg tabletter
- den aktive ingrediens er pyridostigminbromid 60 mg
- de høje komponenter er udfældet silica, stivelse, talkum, magnesiumstearat, lactose (se afsnittet "MESTINON tabletter indeholder lactose").
MESTINON 180 mg depottabletter
- den aktive ingrediens er pyridostigminbromid 180 mg
- de andre komponenter er carnaubavoks, udfældet silica, zein, magnesiumstearat, tribasisk calciumphosphat.
Beskrivelse af MESTINON's udseende og pakningernes indhold
MESTINON 60 mg tabletter
Den fås i hvide tabletter, pakket i ravfarvede glasflasker med en skruelåg på 20 tabletter.
MESTINON 180 mg depottabletter
Den kommer i gulgrå tabletter, pakket i ravglassflasker med skruelåg på 50 tabletter.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN -
MESTINON®
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING -
MESTINON® 60 mg tabletter.
En tablet indeholder:
Aktivt princip: pyridostigminbromid 60 mg.
MESTINON® 180 mg depottabletter.
En tablet indeholder:
Aktivt princip: pyridostigminbromid 180 mg.
03.0 LÆGEMIDDELFORM -
Tabletter. Depottabletter.
04.0 KLINISKE OPLYSNINGER -
04.1 Terapeutiske indikationer -
Myasthenia gravis. Mestinon 60 mg tabletter kan også bruges til behandling af tarmatoni.
04.2 Dosering og indgivelsesmåde -
MESTINON® 60 mg tabletter
Myasthenia gravis: doseringen skal tilpasses, både hvad angår størrelsen af enkeltdoserne og hvad angår antallet af daglige doser, til de faktiske individuelle behov Som en generel doseringsordning 1-3 tabletter på 60 mg, 2-4 gange pr. dag, forøges i de mest alvorlige former.
Tarmatoni: en 60 mg tablet hver 4. time.
MESTINON® 180 mg depottabletter
En til tre Mestinon tabletter med forlænget frigivelse to gange om dagen. Det er vigtigt at huske, at doseringen og hyppigheden af daglig administration er relateret til sygdommens sværhedsgrad og patientens reaktion på behandlingen. De anførte doser skal derfor tjene som reference og kræve individuel tilpasning til patientens individuelle behov. Den anførte dosis kan være lavere (det er muligt at tage en halv depottablet) eller i særlige tilfælde øges.
Når man skifter fra Mestinon 60 mg tabletter til Mestinon 180 mg depottabletter, skal det overvejes, at sidstnævnte ikke længere er potent, men kun langtidsvirkende (6-8 timer, i nogle tilfælde endnu længere, i stedet for 2-4 timer Antallet af tabletter taget som en enkelt dosis forbliver det samme, mens tabletterne med depottabletter tages med længere intervaller over en periode på 24 timer.
(Eksempel: En patient, der hidtil har taget tre Mestinon 60 mg tabletter af det aktive stof seks gange om dagen (6x3x60 mg = 1080 mg / dag) modtager kun tre Mestinon 180 mg depottabletter to gange dagligt (2x3x180 mg = 1080 mg / dag)).
Brug af passende diagnostiske tests er afgørende for at tilpasse doseringen af Mestinon 180 mg depottabletter til de mest alvorlige patologiske tilstande.I nogle tilfælde er det tilrådeligt at justere doseringen under stabile forhold.
Infektioner eller andre skærpende faktorer kan kræve en ændring af kravene til Mestinon 180 mg depottabletter, der er nødvendige for at kontrollere sygdommen. Den behandlende læge bør derfor straks konsulteres.
Administration og varighed af administrationen
Depottabletterne tages med en vis mængde væske og har en central rille, der gør det muligt for dem at bryde for mulig indtagelse af en halv tablet. kompromitteret med den aktive ingrediens.
For at kompensere for et for kort doseringsinterval eller for et øjeblikkeligt behov er det muligt at kombinere Mestinon 180 mg depottabletter med Mestinon 60 mg tabletter.
(Eksempel: en patient skal tage den sidste administration kl. 22.00 for at sikre uforstyrret søvn i løbet af natten. Tabletterne med depottabletter taget i løbet af dagen (8.00 - 22.00) er kun effektive til kl. 18.00. Tidsintervallet fra kl. 18.00 22.00 er den dækket med 60 mg tabletter).
04.3 Kontraindikationer -
Præparatet må ikke administreres i tilfælde af mekaniske okklusioner i mave -tarmkanalen og urinvejene og i alle patologier, der kan tilskrives hypertoni i bronkialmusklerne, såsom spastisk bronkitis, bronchial astma og kendt overfølsomhed over for antikolinesteraser, bromider eller noget af produktet komponenter.
I tilfælde af mavesår, thyrotoksikose, hjertesvigt, myokardieinfarkt skal risikoen ved behandling med Mestinon omhyggeligt overvejes.
Hos patienter med nedsat leverfunktion er periodisk kontrol af leverfunktionstest påkrævet.
Præparatet bør ikke administreres i kombination med depolariserende muskelafslappende midler, såsom suxamethonium.
Der skal udvises særlig forsigtighed ved brug af Mestinon til patienter med bradykardi, diabetes mellitus eller som har gennemgået gastrointestinal kirurgi.
Da der ikke foreligger tilfredsstillende data om anvendelse af Mestinon under graviditet, skal risikoen forbundet med ikke at behandle sygdommen vurderes omhyggeligt i forhold til risikoen ved at tage præparatet under graviditeten.
Pyridostigmin kan udskilles af brystkirtlerne og findes i modermælk. Af denne grund kan du ikke amme under behandlingen.
04.4 Særlige advarsler og passende forholdsregler ved brug -
Mestinon bør bruges med forsigtighed ved bronchial astma.
På grund af muligheden for lejlighedsvise manifestationer på grund af individuel overfølsomhed, bør antichokpræparater eller ampuller af atropin altid være let tilgængelige.
Lægemidler bør ikke opbevares inden for rækkevidde af børn
04.5 Interaktioner med andre lægemidler og andre former for interaktion -
Virkningen af morfinderivater og barbiturater kan forbedres under behandling med Mestinon. Samtidig brug af nogle antibiotika, generelt aminoglycosider eller nogle bedøvelsesmidler, især ether, kan modvirke Mestinons antagonistiske virkning mod lægemidler. Ikke-depolariserende healere.
04.6 Graviditet og amning -
Se kontraindikationer.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner -
På grund af utilfredsstillende symptomkontrol af myasthenia gravis eller parasympatomimetiske virkninger kan nedsat kørsel og brug af maskiner ikke udelukkes under overdosering af Mestinon.
04.8 Bivirkninger -
Svedende, savlende, lakrimation, bronkial hypersekretion, kvalme, opkastning, diarré, mavekramper (øget peristaltik), vandladningstrang, fascikulation, rysten og kramper eller muskelhypotoni kan forekomme under behandling med Mestinon (se kapitel overdosis), "indkvartering eller, efter at have taget høje doser, bradykardi. Da disse symptomer kan være tegn på en kolinerg krise, bør lægen straks konsulteres for at afklare diagnosen Behandling, i tilfælde af akut Mestinon -forgiftning (indtræden af parasympatomimetiske virkninger) er følgende: atropin sulfat sc, oral eller im. I sjældne tilfælde er der rapporteret om udslæt af hududslæt, som forsvinder spontant, når lægemidlet stoppes. Overfølsomhedsreaktioner kan forekomme hos disponerede forsøgspersoner. Ingen data om administration er tilgængelige. Mestinon hos patienter med kontaktlinser handling.
04.9 Overdosering -
I tilfælde af overdosering af Mestinon kan der opstå kolinerge kriser, der hovedsageligt opstår med markant muskelhypotoni (eller øget muskelhypotoni i myasthenik). Hvis denne situation ikke genkendes straks, er der en potentiel dødsfare på grund af mulig lammelse af åndedrætsmusklerne. Bradykardi, paradoksale symptomer og takykardi kan være yderligere samtidige manifestationer. Behandlingen i disse tilfælde består i øjeblikkelig afbrydelse af Mestinon eller andre kolinerge præparater og i administrationen af 1-2 mg atropinsulfat langsomt intravenøst.
Efter at have kontrolleret din puls, gentag eventuelt denne dosis efter to til fire timer.
Ligheden mellem myasthenisk symptomatologi og en kolinerge krise forårsaget af en overdosis af præparatet kræver afklaring af diagnosen med passende tests udført i et passende sundhedsmiljø.
Nødprocedurer, symptomer og modgift i tilfælde af overdosering
Symptomer
Sialorrhea, lacrimation, rhinorrhea, svedtendens, hudrødhed, adynami, myose og overnatningsforstyrrelser, svimmelhed, opkastning, inkontinens, tenesmus, ekstrem bradykardi op til hjertestop, hypotension op til kredsløbskollaps, bronkospasme, lungeødem, lejlighedsvis kramper.
Terapi
Som en specifik modgift til behandling af parasympathomimetiske virkninger, der opstår under overdosering eller forgiftning, anbefales det at bruge atropinsulfat og justere dosis til behovet i henhold til puls og pupiludvidelse.
I tilfælde af hjertestop skal du udføre hjertemassage og kunstigt åndedræt med ilt, og eventuelt bruge udstyret til assisteret kunstigt åndedræt. Kontroller omhyggeligt volumen og homeostase af plasmaelektrolytter.I tilfælde af indkvarteringskramper administreres atropinbaserede øjendråber (kontrol af intraokulært tryk).
05.0 FARMAKOLOGISKE EGENSKABER -
05.1 "Farmakodynamiske egenskaber -
Mestinon besidder kolinerge egenskaber og tilhører klassen af cholinesterasehæmmere; den er derfor en stimulans af de kolinerge nerveender og af motivpladen. Blandt disse stoffer markerer Mestinon sig ved sin gode tolerabilitet, håndterbarhed, stabile og langvarige vedligeholdelse af effektiviteten og gradvis reduktion af den terapeutiske effekt. Reduktion af hyppigheden af lægemiddeladministration letter behandlingen af myasthenia gravis.
05.2 "Farmakokinetiske egenskaber -
Efter oral administration opnås en maksimal plasmakoncentration af det aktive stof på 1,7 - 3,2 timer afhængigt af det samtidige fødeindtag. Distributionsvolumen er 1,64 ± 0,24 L / kg, plasmaclearance er 0,65 L / kg / time. Resorptionshastigheden og -hastigheden viser stor variation mellem individer. Biotilgængeligheden af pyridostigminbromid blev påvist hos raske frivillige med værdier mellem 7,6% og 18,9%. Hos patienter med myasthenia gravis kan værdien falde til 3,3%. Ved intravenøs administration er halveringstiden 1,53 timer, mens den ved oral administration kan nå op til 3,3 timer. Den dosisafhængige eliminering forekommer dels som et uændret aktivt princip (op til 50%) og dels i form af inaktive metabolitter, der følger nyrerne for 80-90%og den enteriske vej for cirka 7%.
I depottablet er den aktive ingrediens lukket i en uopløselig struktur for at opnå den forlængede frigivelse. Det inaktive stof, der bærer den aktive ingrediens, vises i fæces. Dette betyder ikke, at den aktive ingrediens ikke er blevet fuldstændigt absorberet.
05.3 Prækliniske sikkerhedsdata -
De farmakologiske egenskaber af pyridostigmin bestemmes hovedsageligt af den kolinerge virkning forårsaget af hæmning af cholinesterase og af den komplementære stimulerende virkning på den nikotiniske n-cholinoreceptor. Manglende overlevelse af blod-hjerne-barrieren forklarer fraværet af toksiske symptomer i CNS. Pyridostigmin LD50 hos rotter er 3 mg / kg efter intraperitoneal administration, mens det er 115 mg / kg til oral vej. Oral indtagelse af 0,25, 1 og 4 mg / kg hos rotter i over 100 dage gav ikke anledning til histologiske ændringer, hæmatologiske ændringer, adfærdsændringer eller forstyrrede væksten eller var relateret til dødsfald Resultaterne af toksikologiske eller reproduktive undersøgelser hos kaniner og rotter viser ingen negative virkninger på reproduktiv adfærd og fosterudvikling.
Selv med administration af 0,25, 1, 4, 12 og 32 mg / kg til aber i perioder på 115 til 146 dage, skete der ingen toksiske ændringer. Nogle aber modtog lægemidlet i mere end 6 dage i en dosis på 64 mg / kg uden at opleve nogen bivirkninger. Dosen på 128 mg / kg forårsagede i stedet opkastning.
06.0 LÆGEMIDDELOPLYSNINGER -
06.1 Hjælpestoffer -
MESTINON® 60 mg tabletter
En tablet indeholder:
udfældet silica, 51 mg; stivelse, 183,5 mg; talkum, 7 mg; magnesiumstearat, 0,5 mg; lactose, efter smag til 350 mg.
MESTINON® 180 mg depottabletter.
En tablet indeholder:
Carnaubavoks, 150 mg; udfældet silica, 40 mg; zein, 115 mg; magnesiumstearat, 15 mg; tribasisk calciumphosphat, 100 mg.
06.2 Uforenelighed "-
Ingen kendte uforligeligheder.
06.3 Gyldighedsperiode "-
MESTINON® 60 mg tabletter: 60 måneder
MESTINON® 180 mg depottabletter: 24 måneder.
06.4 Særlige opbevaringsforhold -
MESTINON® 180 mg depottabletter: opbevares ved en temperatur på højst 25 ° C. Beskyttes mod fugt.
06.5 Den umiddelbare emballages art og emballagens indhold -
MESTINON® 60 mg tabletter: glasflaske indeholdende 20 tabletter
MESTINON® 180 mg depottabletter: glasflaske indeholdende 50 tabletter.
06.6 Brugsanvisning og håndtering -
Der er ingen særlige brugsanvisninger.
07.0 INDEHAVER AF "MARKEDSFØRINGSTILLADELSEN" -
Meda Pharma SpA - Viale Brenta 18 - 20139 Milano
08.0 MARKEDSFØRINGSTILLADELSESNUMMER -
MESTINON® 60 mg tabletter, 20 tabletter - AIC: 009286016
MESTINON® 180 mg depottabletter, 50 tabletter - AIC: 009286042
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN -
Fornyelse juni 2010
10.0 DATO FOR REVISION AF TEKSTEN -
April 2010