Aktive ingredienser: Levonorgestrel
Jaydess 13,5 mg intrauterint leveringssystem
Indikationer Hvorfor bruges Jaydess? Hvad er det for?
Jaydess er indiceret til forebyggelse af graviditet (prævention) i op til tre år.
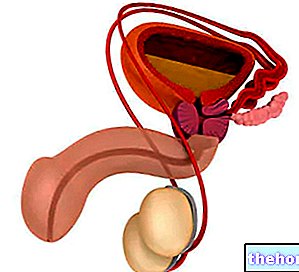
Jaydess er et T-formet intrauterint leveringssystem (IUS), der, når det indsættes i livmoderen, langsomt frigiver en lille mængde af hormonet levonorgestrel.
Jaydess reducerer den månedlige vækst af livmoderens indre slimhinde og gør livmoderhalsslimet tættere.På denne måde forhindrer det kontakten mellem sædcellen og oocytten og dermed befrugtningen af oocytten med spermatozoer.
Kontraindikationer Når Jaydess ikke bør bruges
Generel overvejelse
Inden du kan begynde at bruge Jaydess, vil din læge stille dig et par spørgsmål om din sygehistorie.
Denne indlægsseddel beskriver flere situationer, hvor Jaydess skal fjernes, eller hvor pålideligheden af Jaydess kan reduceres. Under sådanne omstændigheder skal hun opgive samleje eller bruge kondom eller anden barriere som prævention.
Jaydess beskytter, ligesom andre hormonelle præventionsmidler, ikke mod HIV -infektion (AIDS) eller andre seksuelt overførte sygdomme.
Jaydess er ikke indiceret som et nødprævention (postcoital prævention).
Brug IKKE Jaydess
- hvis du er gravid (se afsnittet "Graviditet, amning og fertilitet")
- hvis du har bækkenbetændelse (PID; infektion i de kvindelige kønsorganer), eller hvis du tidligere har lidt af det flere gange
- hvis du lider af lidelser forbundet med øget modtagelighed for bækkeninfektioner
- hvis du har en "infektion i nedre kønsorganer (en" infektion i skeden eller livmoderhalsen [livmoderhalsen])
- hvis du har haft en "livmoderinfektion" efter fødslen, efter et graviditetstab eller efter en abort inden for de sidste 3 måneder.
- hvis du i øjeblikket har abnormiteter i livmoderhalsen
- hvis du har kendt eller mistanke om malignitet i livmoderhalsen eller livmoderen
- hvis du har tumorer, der er følsomme over for progestogenhormoner til at vokse (f.eks. brystkræft)
- hvis du har vaginal blødning af ukendt oprindelse
- hvis du har abnormiteter i livmoderhalsen eller livmoderen, herunder fibroider, som deformerer livmoderhulen
- hvis du har en aktiv leversygdom eller leverkræft
- hvis du er allergisk over for levonorgestrel eller et af de øvrige indholdsstoffer i dette lægemiddel (angivet i afsnit 6).
Forholdsregler ved brug Det, du skal vide, før du tager Jaydess
Tal med din læge, før du bruger Jaydess, hvis:
- har diabetes. Det er generelt ikke nødvendigt at ændre den antidiabetiske behandling, mens du bruger Jaydess, men sundhedspersonalet kan være nødvendigt at overvåge behandlingen.
- lider af epilepsi. Et anfald kan forekomme under isætning eller fjernelse af enheden.
- tidligere har haft en ektopisk eller ekstrauterin graviditet (en graviditet uden for livmoderen).
Tal også med din læge, hvis noget af det følgende gælder for dig, før du begynder at bruge Jaydess, eller hvis det først opstår, mens du bruger Jaydess:
- migræne med synsforstyrrelser eller andre symptomer, der kan være tegn på forbigående cerebral iskæmi (midlertidig blokering af blodtilførslen til hjernen)
- usædvanlig alvorlig hovedpine
- gulsot (gulfarvning af huden, det hvide i øjnene og / eller neglene)
- markant stigning i blodtrykket
- alvorlig arteriesygdom såsom slagtilfælde eller hjerteanfald.
Følgende tegn og symptomer kan være tegn på en ektopisk graviditet, og derfor skal du straks kontakte din læge:
- Menstruationen er stoppet, og vedvarende blødning eller smerter vises efterfølgende
- Du har svære eller vedvarende smerter i underlivet
- Hun har de normale tegn på graviditet, men også blødning og svimmelhed
- Graviditetstesten er positiv
Kontakt straks din læge, hvis du har en af følgende betingelser:
- svær smerte (ligner menstruationskramper) eller kraftig blødning efter placering, eller hvis du har smerter / blødninger, der vedvarer i mere end et par uger. For eksempel kan dette være et tegn på infektion, perforering eller det kan betyde, at Jaydess ikke er i den rigtige position.
- hun mærker ikke længere trådene i skeden. Dette kan være et tegn på udvisning eller perforering. Du kan kontrollere forsigtigt ved at indsætte en finger i skeden og mærke trådene for enden af skeden nær livmoderåbningen (livmoderhalsen). Træk ikke i trådene, da du ved et uheld kan trække Jaydess ud. Undgå samleje eller brug barrierer til prævention (f.eks. Kondomer), så længe din læge har kontrolleret, at spiralen stadig er på plads.
- du eller din partner føler Jaydess 'underekstremitet Undgå samleje, indtil din læge har kontrolleret, at det intrauterine system stadig er på plads.
- hendes partner føler fjernelsestrådene under samleje
- tror hun kan være gravid
- har vedvarende mavesmerter, feber eller usædvanlig vaginal udledning, som kan være tegn på infektion. Infektioner skal behandles med det samme.
- du oplever smerter eller ubehag under samleje, som f.eks. kan være tegn på infektion, ovariecyste eller som kan betyde, at Jaydess ikke er i den korrekte position.
- menstruationskarakteristika ændrer sig pludseligt (for eksempel hvis menstruationen er lav eller fraværende og vedvarende blødning eller smerter eller meget kraftig blødning efterfølgende vises), hvilket kan indikere, at Jaydess ikke er i den korrekte position, eller at hun er blevet udvist.
Det anbefales at bruge sanitetspuder. Hvis du bruger tamponer, skal du ændre dem og være særlig opmærksom på ikke at trække Jaydess's tråde ud.
Børn og unge
Brug af Jaydess er ikke indiceret før begyndelsen af den første menstruation (menarche).
Interaktioner Hvilke lægemidler eller fødevarer kan ændre effekten af Jaydess
Fortæl det til din læge, hvis du tager anden medicin eller har brugt det for nylig
Advarsler Det er vigtigt at vide, at:
Graviditet, amning og fertilitet
Graviditet
Jaydess bør ikke bruges under graviditet.
Mens de bruger Jaydess, kan nogle kvinder stoppe med at menstruere helt.Mangel på menstruation er ikke nødvendigvis et tegn på graviditet. Hvis du ikke har menstruation og har andre graviditetssymptomer, skal du få en lægeundersøgelse og en graviditetstest.
Hvis du ikke har haft menstruation i seks uger og er bekymret, kan du overveje at tage en graviditetstest. Hvis testen er negativ, behøver den ikke at blive gentaget, medmindre der er andre tegn på graviditet.
Hvis du bliver gravid, mens du bruger Jaydess, skal du straks kontakte din læge for at få enheden fjernet. Hvis Jaydess fjernes under graviditeten, er der risiko for abort. Hvis Jaydess forbliver på plads under graviditeten, risiko for abort, infektion eller øget for tidlig fødsel. Diskuter risici forbundet med fortsat graviditet med din læge. Hvis du ønsker at blive gravid, skal du kontakte din læge for at fjerne Jaydess.
Ekstrauterin graviditet (graviditet uden for livmoderen)
Det er ikke almindeligt, at en kvinde bliver gravid, mens hun bruger Jaydess, men hvis hun bliver gravid, mens hun bruger Jaydess, øges risikoen for graviditet uden for livmoderen (ektopisk eller ektopisk graviditet). Kvinder, der allerede har haft en ektopisk graviditet, æggelederoperation eller "bækkeninfektion er mest udsatte. Ektopisk graviditet er en alvorlig tilstand, der kræver øjeblikkelig lægehjælp (se afsnittet" Advarsler og forsigtighedsregler "for tegn og symptomer) og kan påvirke fremtiden frugtbarhed.
Fodringstid
Du kan bruge Jaydess, hvis du ammer. Levonorgestrel (det aktive stof i Jaydess) er fundet i små mængder i modermælk, men der er ikke observeret nogen negative virkninger på den ammende barns vækst eller udvikling eller på mængden eller kvaliteten af modermælk ..
Fertilitet
Fertiliteten vender tilbage til det normale, efter at Jaydess er blevet fjernet.
Kørsel og brug af maskiner
Jaydess påvirker ikke evnen til at føre motorkøretøj eller betjene maskiner.
Dosis, metode og administrationstidspunkt Sådan bruges Jaydess: Dosering
Jaydess indsættelse Jaydess kan indsættes:
- inden for syv dage efter menstruationens begyndelse (månedlig cyklus)
- umiddelbart efter en første trimester abort, forudsat at du ikke har en "genital infektion".
- efter fødslen, kun når livmoderen har genvundet sin normale størrelse og ikke før 6 uger efter fødslen (se afsnittet "Mulige bivirkninger - Perforering").
Besøget foretaget af sundhedspersonale før indsættelse kan omfatte:
- en cervikal smear (Pap smear)
- bryst eksamen
- andre tests, for eksempel for at diagnosticere eventuelle infektioner, herunder seksuelt overførte sygdomme, hvis det er nødvendigt. Lægen vil også foretage et gynækologisk besøg for at bestemme livmoderens position og størrelse.
Efter den gynækologiske undersøgelse:
- Et instrument kaldet et spekulum indsættes i skeden, og livmoderhalsen kan rengøres med en antiseptisk opløsning Jaydess indsættes i livmoderen ved hjælp af et tyndt, fleksibelt plastrør (indsættelsesrør). Lokalbedøvelse af livmoderhalsen kan udføres før indsættelse.
- Nogle kvinder føler sig svimmel eller besvimede under eller efter indsættelse af Jaydess eller efter fjernelse.
- Smerter og blødninger kan forekomme under eller kort tid efter indsættelse
Opfølgende besøg:
Jaydess skal overvåges 4-6 uger efter indsættelse og mindst årligt derefter. Lægen kan bestemme hyppigheden og typen af kontroller, der er nødvendige i dit særlige tilfælde.
Fjernelse af Jaydess
Jaydess skal fjernes senest i slutningen af det tredje brugsår.
Jaydess kan til enhver tid fjernes af din læge; efter fjernelsen er det muligt at blive gravid. Nogle kvinder føler sig svimmel eller besvimede under eller efter fjernelsen af Jaydess. Du kan føle smerter og blødninger, mens du fjerner Jaydess. Ønsker ikke for at blive gravid, bør Jaydess ikke fjernes efter den syvende dag i din menstruationscyklus, medmindre du bruger andre præventionsmetoder (f.eks. kondomer) i mindst syv dage, før IUS fjernes.
Hvis du ikke har menstruation, skal du bruge et præventionsmiddel i syv dage før fjernelse.
En ny Jaydess -enhed kan indsættes umiddelbart efter fjernelse af den forrige; i dette tilfælde er det ikke nødvendigt at anvende yderligere beskyttelsesmetoder.
Bivirkninger Hvad er bivirkningerne af Jaydess
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Følgende liste viser de mulige bivirkninger efter deres hyppighed:
Meget almindelige bivirkninger: kan forekomme hos mere end 1 ud af 10 personer
- hovedpine
- mavesmerter / bækken
- acne / fedtet hud
- menstruationsændringer såsom forøget og nedsat menstruation, pletblødning, sjælden menstruation og fraværende menstruation (se også afsnit nedenfor om uregelmæssig og sjælden blødning)
- ovariecyste (se også det følgende afsnit om ovariecyster)
- betændelse i de ydre kønsorganer og vagina (vulvovaginitis)
Almindelige bivirkninger: kan forekomme hos op til 1 ud af 10 personer
- deprimeret humør / depression
- migræne
- kvalme
- infektion i øvre kønsorganer
- smertefuld menstruation
- brystsmerter / ubehag
- udstødning af enheden (fuldstændig og delvis) - (se det følgende afsnit om "udstødning)
- hårtab
- kønsudladning
Ikke almindelige bivirkninger: kan forekomme hos op til 1 ud af 100 personer
- øget kropshår
Sjældne bivirkninger: kan forekomme hos op til 1 ud af 1.000 mennesker
- perforering 1 af livmoderen (se også afsnit nedenfor om perforering)
1 Risikoen for perforering er højere (op til 1 ud af 100 patienter) hos kvinder, der ammer på tidspunktet for indsætning af den intrauterine enhed, og når den intrauterine enhed indsættes op til 36 uger efter fødslen.
Beskrivelse af nogle mulige bivirkninger
- Allergiske reaktioner, herunder udslæt, urticaria og angioødem (karakteriseret ved pludselig hævelse, for eksempel i øjne, mund, hals) er blevet rapporteret med lignende produkter.
Uregelmæssig eller sjælden blødning
Jaydess vil sandsynligvis ændre menstruationscyklussen. Menstruation kan opstå som pletblødning (let blødning), blødning af kortere eller længere varighed eller mindre eller større intensitet eller endda fuldstændig fravær af menstruation.
Blødning og pletblødning kan forekomme mellem menstruation, især i de første 3-6 måneder. Nogle gange er menstruationen i begyndelsen mere rigelig end normalt.
Samlet set vil mængden og varigheden i menstruationsdage sandsynligvis falde gradvist hver måned. Hos nogle kvinder kan menstruation stoppe helt.
Livmoderslimhinden kan ikke blive tykkere månedligt på grund af hormonelle virkninger, og derfor er der ikke noget materiale, der skal udvises med menstruation. Dette betyder ikke nødvendigvis, at du er i overgangsalderen eller gravid. Dine hormonniveauer forbliver. Generelt normale.
Efter fjernelse af systemet skulle menstruationen snart vende tilbage til det normale.
Bekkeninfektion
Jaydess Inserter og Jaydess Device er sterile, men risikoen for bækkeninfektion (infektioner i slimhinden i livmoderen eller æggelederne) øges ved indsættelse og i de første 3 uger derefter.
Bekkeninfektioner hos SUI -brugere skyldes ofte seksuelt overførte sygdomme. Risikoen for infektion er højere, hvis du eller din partner har flere seksuelle partnere, eller hvis du tidligere har haft bækkenbetændelsessygdom (PID).
Bekkeninfektioner skal behandles hurtigt.
Bekkeninfektioner som PID kan have alvorlige konsekvenser, forringe fertiliteten og øge risikoen for en fremtidig ektopisk graviditet (graviditet uden for livmoderen). I ekstremt sjældne tilfælde kan alvorlige infektioner eller sepsis forekomme kort tid efter indsættelsen. Alvorlig kan være dødelig).
Jaydess bør fjernes for tilbagevendende PID'er, eller hvis infektionen er alvorlig eller ikke reagerer på behandlingen.
Bortvisning
Muskelkontraktioner i livmoderen under menstruation kan nogle gange bevæge sig eller skubbe IUS -enheden ud.
Det er en sjælden, men mulig forekomst, at Jaydess bliver bortvist i løbet af sin periode, uden at hun har bemærket det.
Det er også muligt for Jaydess at blive delvist udvist af livmoderen og derefter flyttet, men ikke helt udvist (du og din partner kan bemærke dette under samleje). Hvis Jaydess er helt eller delvist udvist, er hun ikke længere beskyttet mod graviditet..
Boring
Under indsættelsen af Jaydess kan penetration eller perforering af livmodervæggen forekomme, men det er muligt, at perforeringen først vil blive fundet efter et stykke tid. Hvis Jaydess findes uden for livmoderhulen, er det ikke effektivt til at forhindre graviditet. Kirurgi kan være påkrævet for at fjerne Jaydess.
Risikoen for perforering stiger under amning og hos kvinder, hvor den indsættes op til 36 uger efter fødslen, og kan øges:
- hos kvinder, der har livmoderen vendt tilbage (fast retroverteret livmoder)
Ovariecyste
Da Jaydess prævention hovedsageligt skyldes lokale virkninger i livmoderen, fortsætter ægløsning (frigivelse af et æg) normalt, mens du bruger Jaydess. Nogle gange kan en æggestokkecyste udvikle sig. I de fleste tilfælde oplever kvinden ingen symptomer.
En ovariecyste kan kræve lægehjælp, mere sjældent kirurgi, men den forsvinder generelt af sig selv
Indberetning af bivirkninger
Tal med din læge eller sygeplejerske, hvis du får mulige bivirkninger. Dette inkluderer eventuelle bivirkninger, der ikke er anført i denne indlægsseddel. Du kan også rapportere bivirkninger direkte via det nationale rapporteringssystem på https: //www.aifa. .Gov .it / indhold / bivirkningsrapporter
Ved at rapportere bivirkninger kan du hjælpe med at give flere oplysninger om sikkerheden ved dette lægemiddel.
Udløb og opbevaring
Denne medicin kræver ingen særlige opbevaringsbetingelser.
Opbevar denne medicin utilgængeligt for børn.
Åbn ikke blisterpakningen. Kun lægen eller sygeplejersken er autoriseret til at gøre dette.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen og blisteren efter EXP. Udløbsdatoen refererer til den sidste dag i den pågældende måned.
Hvad Jaydess indeholder
Den aktive ingrediens er levonorgestrel. Det intrauterine leveringssystem indeholder 13,5 mg levonorgestrel.
Øvrige indholdsstoffer er:
- polydimethylsiloxan elastomer
- vandfri kolloid silica
- polyethylen
- bariumsulfat
- sort jernoxid (E172)
- sølv
Hvordan Jaydess ser ud og pakningens indhold
Jaydess er et T-formet intrauterint leveringssystem (IUS). Den lodrette arm på T-kroppen indeholder et reservoir, der indeholder lægemidlet levonorgestrel. To ledninger beregnet til fjernelse af enheden er fastgjort til øjet i den nedre ende af den lodrette arm. Derudover indeholder den lodrette støtte en sølvring placeret nær de vandrette arme, synlig på ultralyd.
Emballage:
- 1x1 intrauterint leveringssystem.
- 5x1 intrauterint leveringssystem.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Følgende oplysninger er kun beregnet til sundhedspersonale
INSTRUKTIONER TIL INSÆTNING
Jaydess 13,5 mg intrauterint leveringssystem
Indsættelse af en sundhedsperson under aseptiske forhold.
Jaydess leveres med en indsætter i en steril emballage, der ikke må åbnes, før den er klar til indsættelse. Må ikke resteriliseres. Jaydess er kun til engangsbrug. Må ikke bruges, hvis blisterpakningen er beskadiget eller åbnet. Indsæt ikke efter den angivne udløbsdato på kartonen. og på blisterpakningen efter EXP.
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler
Forberedelse til indsættelse
- Besøg patienten for at bestemme livmoderens størrelse og position og for at opdage tegn på akut genital infektion eller andre kontraindikationer for Jaydess -indsætning. Hvis der er tvivl om en graviditet, bør der foretages en graviditetstest.
- Indsæt et spekulum, visualiser livmoderhalsen og rengør forsigtigt livmoderhalsen og skeden med en passende antiseptisk opløsning.
- Brug om nødvendigt en assistent.
- Tag fat i livmoderhalsens forreste læbe med tenaculum pincet eller anden pincet for at stabilisere livmoderen. Hvis livmoderen er tilbageført, kan det være hensigtsmæssigt at gribe fat i livmoderhalsens bageste læbe. Der kan påføres en let trækkraft på pincetten for at rette livmoderhalskanalen mod. Modsætning på livmoderhalsen.
- Før en livmoderprobe gennem livmoderhalskanalen til fundus for at måle dybden, bekræfte livmoderhulets retning og udelukke tilstedeværelsen af intrauterine abnormiteter (f.eks. Septum, submukosale fibroider) eller et tidligere indsat intrauterint præventionsmiddel og ikke fjernet. Hvis du har svært ved at overveje at udvide kanalen. Hvis udvidelse af livmoderhalskanalen er nødvendig, skal du overveje muligheden for at bruge smertestillende midler og / eller en paracervikal blok
Indskud
1) Åbn først den sterile emballage helt. Arbejd under aseptiske forhold ved hjælp af sterile handsker.
2) Skub skyderen fremad i pilens retning til den længste position for at indlæse Jaydess i indsættelsesrøret
VIGTIG! Træk ikke skyderen ned, da dette vil medføre, at Jaydess frigives for tidligt. Når Jaydess er frigivet, kan den ikke genindlæses.
3) Hold markøren i den længste position, indstil den øverste kant af flangen i overensstemmelse med livmoderdybden målt med sonden.
4) Mens skyderen holdes i den længste position, føres indsætteren ind i livmoderhalsen, indtil flangen er cirka 1,5 til 2,0 cm fra livmoderhalsen.
VIGTIG! Undlad at tvinge indføreren i. Udvid om nødvendigt cervikal kanalen.
5) Mens du holder indføringsenheden, skal du trække skyderen op til mærket for at åbne Jaydess's vandrette arme. Vent 5-10 sekunder, indtil de vandrette arme er fuldt udplaceret.
6) Fremfør forsigtigt insertereren mod fundus, indtil flangen rører livmoderhalsen. Jaydess er nu placeret ved fundus.
7) Hold indsætteren på plads, slip Jaydess ved at trække skyderen helt ned. Hold skyderen nede, fjern forsigtigt indsætter ved at trække i den.Klip trådene og efterlad ca. 2-3 cm, der stikker ud af livmoderhalsen.
VIGTIG! Hvis du har mistanke om, at systemet ikke er i den korrekte position, skal du kontrollere stedet (f.eks. Ved ultralyd). Fjern systemet, hvis det ikke sidder korrekt i livmoderen. Når et ansigt er fjernet, behøver systemet ikke at blive indtastet igen.
Fjernelse / udskiftning
For fjernelse / udskiftning se Jaydess Resumé af produktkarakteristika.
For at fjerne Jaydess skal du trække i ledningerne med en tang.
Et nyt Jaydess -system kan indsættes umiddelbart efter fjernelse.
Efter at Jaydess er blevet fjernet, bør systemet undersøges for at sikre, at det er sundt.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
JAYDESS 13,5 MG INTRAUTERINE RELEASE SYSTEM
▼ Lægemiddel underlagt yderligere overvågning. Dette vil muliggøre hurtig identifikation af nye sikkerhedsoplysninger. Sundhedspersonale bedes rapportere alle formodede bivirkninger. Se afsnit 4.8 for information om, hvordan du rapporterer bivirkninger.
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Det intrauterine leveringssystem indeholder 13,5 mg levonorgestrel.
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
For detaljer om frigivelseshastigheder, se afsnit 5.2.
03.0 LÆGEMIDDELFORM
Intrauterint leveringssystem (intrauterint leveringssystem, IUS).
Produktet består af en hvidlig eller lysegul lægemiddelkerne dækket af en semi-uigennemsigtig membran, monteret på den lodrette understøtning af et T-formet legeme. Desuden indeholder den lodrette understøtning en sølvring placeret nær de vandrette arme. T-kroppen har et øje i den ene ende af den lodrette støtte og to vandrette arme i den anden ende. Fjernelse af ledninger er fastgjort til øjet. Den vertikale understøtning af IUS er indeholdt i indsættelsesrøret, ved spidsen af indsættelsesmaskinen. IUS og indsætter er i det væsentlige fri for synlige urenheder.
Dimensioner på Jaydess: 28 x 30 x 1,55 mm
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Prævention op til 3 år.
04.2 Dosering og indgivelsesmåde
Dosering
Jaydess indsættes i livmoderhulen og er effektiv i op til tre år.
Indsætning og fjernelse / udskiftning
Jaydess bør kun indsættes af læger / sundhedspersonale med erfaring i indsættelse af IUS -enheder og / eller som er blevet uddannet i Jaydess -indsættelsesproceduren.
Jaydess skal indsættes i livmoderhulen inden for syv dage efter menstruationens start. Jaydess kan når som helst under din cyklus udskiftes med et nyt system. Jaydess kan også indsættes umiddelbart efter en første trimesterabort.
Efter fødslen skal indsættelsen udskydes, indtil livmoderen er fuldstændig involveret, og under alle omstændigheder må den først finde sted seks uger efter fødslen. Hvis involution forsinkes betydeligt, kan du overveje at vente op til 12 uger efter levering.
I tilfælde af vanskeligheder ved indsættelse og / eller usædvanlig smerte eller blødning under eller efter indsættelse, bør der straks træffes passende foranstaltninger for at udelukke perforering, såsom en lægeundersøgelse og ultralyd. Den gynækologiske undersøgelse er muligvis ikke tilstrækkelig til at udelukke delvis perforering.
Jaydess skiller sig ud fra andre IUS’er takket være sølvringen, synlig på ultralyd. Jaydess T-krop indeholder bariumsulfat, som gør det synligt på røntgen.
For at fjerne Jaydess skal du let trække i ledningerne med en tang. Hvis ledningerne ikke kan findes, og systemet er synligt i livmoderen ved ultralyd, kan det fjernes med fin pincet, i hvilket tilfælde livmoderhalskanalen skal udvides eller opereres.
Systemet skal fjernes senest ved udgangen af det tredje år. Hvis kvinden ønsker at fortsætte med at bruge den samme metode, kan et nyt system indsættes umiddelbart efter fjernelse af den tidligere enhed.
Hvis kvinden ikke ønsker at blive gravid, skal enheden fjernes inden for 7 dage efter menstruationens start, så længe menstruationen stadig er normal. Hvis systemet fjernes på et andet tidspunkt i cyklussen, og kvinden har haft sex inden for om ugen, er der risiko for graviditet, medmindre der indsættes et nyt system umiddelbart efter, at det forrige er fjernet.
Efter fjernelse skal Jaydess -systemet undersøges for integritet.
Ældre patienter
Jaydess er ikke undersøgt hos kvinder over 65 år. Der er ingen indikation for brugen af Jaydess til postmenopausale kvinder.
Patienter med nedsat leverfunktion
Jaydess er ikke undersøgt hos kvinder med nedsat leverfunktion. Jaydess er kontraindiceret hos kvinder med akut leversygdom eller leverkræft (se pkt.4.3).
Patienter med nedsat nyrefunktion
Jaydess er ikke undersøgt hos kvinder med nedsat nyrefunktion.
Pædiatrisk population
Anvendelse af produktet er ikke angivet før menarchen. For oplysninger om sikkerhed og effekt hos unge, se pkt. 5.1.
Indgivelsesmåde
Indsættelse af en sundhedsperson under aseptiske forhold.
Jaydess leveres med en indsætter i en steril emballage, der ikke må åbnes, før den er klar til indsættelse. Må ikke resteriliseres. Jaydess er kun til engangsbrug. Må ikke bruges, hvis blæren er beskadiget eller åbnet. Indsæt ikke enheden efter den angivne udløbsdato. på kartonen og blisteren efter EXP.
Ubrugt medicin og affald fra denne medicin skal bortskaffes i overensstemmelse med lokale regler.
Forberedelse til indsættelse
• Besøg patienten for at bestemme livmoderens størrelse og position og for at opdage tegn på akut genital infektion eller andre kontraindikationer for Jaydess -indsættelse. Hvis der er tvivl om den aktuelle graviditet, bør der foretages en graviditetstest.
• Indsæt et spekulum, visualiser livmoderhalsen og rengør forsigtigt livmoderhalsen og skeden med en passende antiseptisk opløsning.
• Brug om nødvendigt en assistent.
• Tag fat i livmoderhalsens forreste læbe med tenaculum pincet eller anden pincet for at stabilisere livmoderen. Hvis livmoderen er tilbageført, kan det være hensigtsmæssigt at gribe fat i livmoderhalsens bageste læbe. Skånsom trækkraft på pincet kan påføres for at rette livmoderhalskanalen modtræk på livmoderhalsen.
• Før en livmoderprobe gennem livmoderhalskanalen til fundus for at måle dybden, bekræfte livmoderhulets retning og udelukke tilstedeværelsen af intrauterine abnormiteter (f.eks. Septum, submukosale fibroider) eller et tidligere indsat intrauterint prævention og ikke fjernet. Hvis du har svært ved at overveje at udvide kanalen. Hvis udvidelse af livmoderhalskanalen er nødvendig, bør du overveje at bruge smertestillende midler og / eller en paracervikal blok.
Indskud
1. Åbn først den sterile emballage helt. Arbejd under aseptiske forhold ved hjælp af sterile handsker.
2. Skub skyderen fremad i pilens retning til den længste position for at indlæse Jaydess i indsættelsesrøret.
VIGTIG! Træk ikke skyderen ned, da dette vil medføre, at Jaydess frigives for tidligt. Når den er frigivet, kan Jaydess ikke genindlæses
3. Hold markøren i den længste position, og indstil den øverste kant af flangen til at svare til livmoderdybden målt med sonden.
4. Mens skyderen holdes i den længste position, føres indsætningsmaskinen ind i livmoderhalsen, indtil flangen er cirka 1,5-2,0 cm fra livmoderhalsen.
VIGTIG! Undlad at tvinge indføreren i. Udvid om nødvendigt cervikal kanalen
5. Mens du holder indføringsenheden, skal du trække skyderen op til mærket for at åbne Jaydess vandrette arme. Vent 5-10 sekunder, indtil de vandrette arme er fuldt udplaceret.
6. Fremfør forsigtigt indføringsmaskinen mod fundus, indtil flangen rører ved livmoderhalsen. Jaydess er nu placeret ved fundus
7. Mens du holder indsætteren på plads, skal du slippe Jaydess ved at trække skyderen helt ned. Hold skyderen nede, og fjern forsigtigt indsættelsesmaskinen ved at trække i den. Klip trådene og efterlad ca. 2-3 cm, der stikker ud af livmoderhalsen.
VIGTIG! Hvis du har mistanke om, at systemet ikke er i den korrekte position, skal du kontrollere stedet (f.eks. Ved ultralyd). Fjern systemet, hvis det ikke sidder korrekt i livmoderen. Når systemet er fjernet, behøver det ikke at genaktiveres
Fjernelse / udskiftning
Se afsnit 4.2 for fjernelse / udskiftning Indsætning og fjernelse / udskiftning.
For at fjerne Jaydess skal du trække i ledningerne med en tang.
Et nyt Jaydess -system kan indsættes umiddelbart efter fjernelse.
Efter at Jaydess er blevet fjernet, bør systemet undersøges for at sikre, at det er sundt.
04.3 Kontraindikationer
• Graviditet (se afsnit 4.6);
• Akut eller tilbagevendende bækkenbetændelse eller tilstande forbundet med en øget risiko for bækkeninfektion;
• Akut cervicitis eller vaginitis;
• Postpartum endometritis eller inficeret abort inden for de sidste tre måneder;
• Cervikal intraepitelial neoplasi indtil opløsning;
• Uterin eller cervikal malign neoplasma;
• Progestinfølsomme tumorer, f.eks. brystkræft;
• Unormal vaginal blødning af ukendt ætiologi;
• Medfødt eller erhvervet uterin abnormitet, herunder fibroider, som kan forstyrre indsættelsen og / eller varigheden af det intrauterine system (dvs. hvis de deformerer livmoderhulen);
• Akut leversygdom eller leverkræft;
• Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt. 6.1.
04.4 Særlige advarsler og passende forholdsregler ved brug
Hvis nogen af følgende betingelser eksisterer eller opstår for første gang, skal Jaydess bruges med forsigtighed efter samråd med en specialist, eller fjernelse af systemet bør overvejes:
• migræne, fokal migræne med asymmetrisk synstab eller andre symptomer, der tyder på forbigående cerebral iskæmi
• hovedpine af exceptionel intensitet
• gulsot
• markant stigning i blodtrykket
• alvorlig arteriel sygdom såsom slagtilfælde eller myokardieinfarkt
Lave doser levonorgestrel kan forringe glukosetolerancen, og blodglukose bør overvåges hos diabetiske Jaydess -brugere. Det er imidlertid generelt ikke nødvendigt at ændre behandlingsregimet hos diabetikere, der bruger levonorgestrel-baseret IUS.
Lægeundersøgelse / konsultation
Inden indsættelse skal kvinden informeres om fordele og risici ved Jaydess, herunder tegn og symptomer på perforering og risiko for ektopisk graviditet, se nedenfor. En igangværende graviditet og tilstedeværelsen af seksuelt overførte sygdomme skal udelukkes.Kønsinfektioner skal behandles med succes før indsættelse. Livmoders position og livmoderhulets størrelse skal bestemmes. For at opnå maksimal effekt og reducere risikoen for udvisning er det vigtigt, at Jaydess er placeret ved fundus. Instruktionerne for indsættelse skal følges nøje.
Særligt vigtigt er træningen i den korrekte indsættelsesteknik.
Indsætning og fjernelse kan være forbundet med en vis grad af smerte og blødning.Proceduren kan udløse en vasovagal reaktion (f.eks. Synkope eller anfald hos patienter med epilepsi).
Kvinden bør undersøges igen 4-6 uger efter indsættelse for at kontrollere ledningerne og kontrollere systemets korrekte position. Derefter anbefales årlige kontroller eller hyppigere, hvis det er klinisk indiceret.
Jaydess er ikke beregnet til brug som post-coital prævention.
Brugen af Jaydess til behandling af tunge menstruationsstrømme eller til beskyttelse mod endometrial hyperplasi under østrogenerstatningsterapi er ikke bevist. Derfor bør Jaydess ikke bruges under disse forhold.
Ektopisk graviditet
I kliniske undersøgelser var den samlede forekomst af ektopisk graviditet med Jaydess cirka 0,11 pr. 100 kvindeår. Cirka halvdelen af de graviditeter, der opstår under brug af Jaydess, kan være ektopiske.
Kvinder, der overvejer at bruge Jaydess, bør informeres om tegn, symptomer og risiko for ektopisk graviditet. For kvinder, der bliver gravide, mens de bruger Jaydess, bør muligheden for en ektopisk graviditet overvejes og evalueres.
Kvinder med en ektopisk graviditet, tubal kirurgi eller bækkeninfektion har en forhøjet risiko for ektopisk graviditet. Muligheden for en ektopisk graviditet bør overvejes i tilfælde af smerter i underlivet, især hvis det er forbundet med fraværende menstruation, eller hvis der opstår "blødning" hos en amenorøsk kvinde.
Da en ektopisk graviditet kan påvirke fremtidig fertilitet, bør fordele og risici ved at bruge Jaydess afvejes omhyggeligt, især for nulliparøse kvinder.
Anvendelse til nulliparøse kvinder: Da klinisk erfaring er begrænset, er Jaydess ikke førstevalgsbehandlingen til prævention hos nulliparøse kvinder.
Virkninger på menstruationscyklussen
Virkninger på menstruationscyklussen forventes hos de fleste brugere af Jaydess. Disse virkninger skyldes levonorgestrels direkte virkning på endometriet og er muligvis ikke relateret til ovarial aktivitet.
Uregelmæssig blødning og pletblødning er almindelig i de første par måneders brug. Efterfølgende resulterer markant undertrykkelse af endometriet i en reduktion i varigheden og volumenet af menstruationsblodtab. Dårlig strømning udvikler sig ofte til oligomenoré eller amenoré.
I kliniske undersøgelser udviklede sjældne blødninger og / eller amenoré gradvist hos henholdsvis ca. 22,3% og 11,6% af brugerne. Hvis menstruation ikke forekommer inden for seks uger efter begyndelsen af den forrige menstruation, bør muligheden for graviditet overvejes. Det er ikke nødvendigt at gentage graviditetstesten hos kvinder med vedvarende amenoré, medmindre der er andre tegn på graviditet.
Hvis blodtabet med tiden bliver mere rigeligt og / eller uregelmæssigt, bør der træffes passende diagnostiske foranstaltninger, fordi uregelmæssigt blodtab kan være et symptom på endometrielle polypper, hyperplasi eller karcinom, og kraftig blødning kan være tegn på en ubevidst udvisning af IUS .
Bekkeninfektion
Selvom Jaydess og inserter er sterile, kan de efter bakteriekontaminering under indsættelse blive et redskab til transport af bakterier ind i det øvre kønsorgan. Bækkeninfektion er blevet rapporteret ved brug af enhver IUS eller IUD. I kliniske forsøg har bækkenbetændelsessygdom (bækkenbetændelse, PID) blev observeret oftere i begyndelsen af brugen af Jaydess, svarende til det, der er blevet offentliggjort for kobberspiral, hvorved den højeste frekvens af PID findes i de første 3 uger efter indsættelse, for derefter at falde.
Inden Jaydess bruges, skal alle risikofaktorer forbundet med bækkeninfektion (f.eks. Flere seksuelle partnere, seksuelt overførte infektioner, PID -historie) evalueres hos patienter. Bekkeninfektioner som PID kan have alvorlige konsekvenser, forringe fertiliteten og øge risikoen for ektopisk graviditet.
Som med andre gynækologiske eller kirurgiske procedurer, og selvom det er ekstremt sjældent, kan alvorlig infektion eller sepsis (herunder gruppe A streptokok -sepsis) forekomme efter indsættelse af lUD.
Hos kvinder med tilbagefaldende endometritis eller bækkenbetændelse eller med alvorlig akut infektion eller reagerer ikke på behandling, skal Jaydess fjernes.
Bakteriologisk undersøgelse er indiceret, og overvågning anbefales, selvom symptomer, der tyder på infektion, er moderate.
Bortvisning
I kliniske forsøg med Jaydess var forekomsten af udvisning lav og inden for samme område som set med andre IUD'er og IUS. Symptomer på delvis eller fuldstændig udvisning af Jaydess kan omfatte blødning eller smerter. En "delvis eller fuldstændig udvisning kan dog forekomme uden at kvinden bemærker det, hvilket resulterer i en reduktion eller tab af præventionsbeskyttelse. Da Jaydess reducerer menstruationsblødning over tid, kan en stigning i sådanne tab være tegn på en" udvisning.
I tilfælde af delvis udvisning skal Jaydess fjernes. Ved denne lejlighed kan der indsættes et nyt system, forudsat at en graviditet er blevet udelukket.
Kvinden skal instrueres i, hvordan hun kontrollerer Jaydess -ledninger, og opfordres til at kontakte sundhedspersonalet, hvis hun ikke kan mærke ledningerne.
Boring
Perforering eller indtrængning af kroppen eller livmoderhalsen med et intrauterint præventionsmiddel kan forekomme, især under indsættelse, selvom det måske ikke opdages før senere, hvilket reducerer Jaydess 'effektivitet. I tilfælde af vanskeligheder ved indsættelse og / eller ekstraordinær smerte eller blødning under eller efter indsættelse, bør der straks træffes passende foranstaltninger for at udelukke perforering, såsom fysisk undersøgelse og ultralyd. Systemet skal fjernes; operation kan være påkrævet.
I en stor prospektiv sammenlignende ikke-interventionel kohorteundersøgelse foretaget hos intrauterine enhedsbrugere (N = 61.448 kvinder) var forekomsten af perforering 1,3 (95% CI: 1,1-1,6) pr. 1000 indsættelser. I hele undersøgelseskohorten; 1,4 (95% CI: 1,1-1,8) for hver 1000 indsættelse i kohorten af en anden levonorgestrel-baseret intrauterin enhed og 1,1 (95% CI: 0,7-1,6) for hver 1000 indsættelser i kohorten med intrauterine kobberanordninger.
Undersøgelsen viste, at både amning ved indsættelse og indsættelse op til 36 uger efter fødslen var forbundet med en øget risiko for perforering (se tabel 1) Disse risikofaktorer var uafhængige af apparattype intrauterin indsat.
Tabel 1: Forekomst af perforering pr. 1000 indsættelser for hele kohorteundersøgelsen, lagdelt efter amning og indsættelsestid efter fødslen (kvinder, der har født)
Risikoen for perforering kan øges hos kvinder med en fast retroverteret livmoder.
Efterindsættelse skal følge instruktionerne i afsnittet "Lægeundersøgelse / konsultation", som kan tilpasses klinisk angivet hos kvinder med risikofaktorer for perforering.
Tab af tråde
Hvis trådene ikke er synlige i livmoderhalsen under opfølgende besøg, skal en bevidstløs bortvisning og en igangværende graviditet udelukkes. Trådene kan have trukket sig tilbage i livmoderen eller livmoderhalskanalen og kan dukke op igen i den næste menstruationscyklus. Hvis graviditet er blevet udelukket, findes trådene normalt ved forsigtigt at udforske livmoderhalskanalen med et egnet instrument. Hvis ikke, skal det overvejes muligheden for udvisning eller perforering. Ultralyd kan bruges til at verificere systemets position. Hvis en ultralyd ikke er tilgængelig, eller hvis ultralydet ikke giver resultater, kan Jaydess lokaliseres ved røntgen.
Ovariecyster / forstørrelse af ovarie follikler
Da Jaydess 'prævention hovedsageligt skyldes dens lokale virkninger på livmoderen, er der generelt ingen ændring i ægløsningsfunktionen, herunder regelmæssig follikeludvikling, oocytfrigivelse og follikulær atresi hos kvinder i den fødedygtige alder. Nogle gange forsinkes follikulær atresi og folliculogenese kan fortsætte. Disse forstørrede follikler kan ikke klinisk skelnes fra ovariecyster og er blevet rapporteret som bivirkninger i kliniske forsøg hos 13,2% af Jaydess -brugere, herunder ovariecyster, hæmoragiske ovariecyster og brud på ovariecyster. De fleste cyster er asymptomatiske, men nogle kan ledsages af bækkenpine eller dyspareuni.
I de fleste tilfælde forsvinder dilaterede follikler spontant inden for to til tre måneders observation. Hvis en udvidet follikel ikke går spontant tilbage, kan ultralydsovervågning og andre diagnostiske eller terapeutiske foranstaltninger indikeres. Kirurgi er sjældent nødvendig.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Interaktioner med lægemidler, der fremkalder mikrosomale leverenzymer, især cytochrom P450 -enzymer, kan forekomme, hvilket resulterer i øget metabolisme af levonorgestrel og øget clearance af kønshormoner (f.eks. Phenytoin, barbiturater, primidon, carbamazepin, rifampicin, rifabutin, nevirapin, efavirenz, bosentan og evt. oxcarbazepin, topiramat, felbamat, griseofulvin og produkter, der indeholder naturlægemidlet perikon).
På den anden side kan stoffer, der hæmmer de enzymer, der er ansvarlige for lægemiddelmetabolisme (f.eks. Itraconazol, ketoconazol), øge serumkoncentrationerne af levonorgestrel.
Virkningen af disse lægemidler på Jaydess 'virkning kendes ikke, men menes ikke at have særlig relevans på grund af den lokale virkningsmekanisme.
Magnetic Resonance Imaging (MRI) erhvervelse
Ikke-kliniske analyser har vist, at patienter sikkert kan undersøges efter Jaydess-indsættelse med følgende indstillinger: statisk magnetfelt lig med eller mindre end 3 tesla, maksimalt rumligt gradientmagnetfelt lig med eller mindre end 720 gauss / cm. Under disse forhold, med en 15 minutters scanning, var den maksimale temperaturstigning ved Jaydess 1,8 ° C. Små artefakter kan forekomme, hvis interesseområdet nøjagtigt matcher eller er relativt tæt på Jaydess position.
04.6 Graviditet og amning
Fertilitet
Anvendelse af et intrauterint system, der frigiver levonorgestrel, kompromitterer ikke fremtidig fertilitet.Efter fjernelse af det intrauterine system genvinder kvinden normal fertilitet (se afsnit 5.1).
Graviditet
Indsættelse af Jaydess er kontraindiceret til gravide (se pkt. 4.3).
Hvis en kvinde bliver gravid, mens hun bruger Jaydess, bør graviditet uden for livmoderen udelukkes, og hurtig fjernelse af systemet anbefales, da enhver intrauterin prævention, der sidder på plads, kan øge risikoen for abort og for tidlig fødsel. Fjernelse af Jaydess eller brug af livmoderprober kan også forårsage abort.Hvis kvinden ønsker at fortsætte graviditeten, og systemet ikke kan fjernes, skal hun informeres om risici og mulige konsekvenser af for tidlig fødsel af barnet. kvinden bør uddannes om behovet for at rapportere alle symptomer, der tyder på komplikationer, såsom krampe mavesmerter med feber.
På grund af intrauterin administration og lokal eksponering for levonorgestrel bør de mulige viriliserende virkninger hos kvindelige fostre overvejes.Klinisk erfaring med graviditetsresultater under brug af Jaydess er begrænset på grund af den høje præventionsevne. Kvinder bør informeres om, at der i øjeblikket ikke er tegn på fosterskader på grund af brugen af et levonorgestrelfrigivende intrauterint system i tilfælde, hvor graviditeten er fortsat, mens den levonorgestrelfrigivende IUS forbliver på plads.
Fodringstid
Generelt ser det ud til, at der ikke er nogen skadelig virkning på spædbarnets vækst eller udvikling, hvis der kun bruges en gestagen-metode seks uger efter fødslen. Et levonorgestrel-frigivende intrauterint system kompromitterer ikke mængden eller kvaliteten af modermælk. Små mængder gestagen (ca. 0,1% af levonorgestrel -dosis) passerer i modermælken.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Jaydess påvirker ikke evnen til at føre motorkøretøj eller betjene maskiner.
04.8 Bivirkninger
Resumé af sikkerhedsprofilen
De fleste kvinder oplever ændringer i deres menstruationscyklus efter indsættelse af Jaydess. Over tid øges hyppigheden af amenoré og sjældne blødninger, og hyppigheden af langvarig og hyppig menstruation falder.I kliniske undersøgelser er menstruationscyklusser blevet observeret hos kvinder. Følgende funktioner:
Tabel 2: Menstruationscyklusegenskaber observeret med Jaydess i kliniske undersøgelser
* Kvinder med langvarig blødning kan også falde ind i en af de andre kategorier (undtagen amenoré)
Oversigtstabel over bivirkninger
Hyppigheden af bivirkninger (Bivirkninger, ADR) rapporteret med Jaydess er opsummeret i nedenstående tabel. Inden for hver frekvensklasse er uønskede virkninger opført efter faldende sværhedsgrad.Frekvenserne er defineret som følger:
meget almindelig (≥ 1/10),
almindelig (≥ 1/100,
ikke almindelig (≥ 1 / 1.000,
sjælden (≥ 1 / 10.000,
meget sjælden (
* I kliniske forsøg skulle ovariecyster rapporteres som AE i tilfælde af unormale, ikke-funktionelle og / eller> 3 cm diameter cyster på ultralyd.
** Denne hyppighed er baseret på kliniske undersøgelser, der udelukker ammende kvinder. I en stor prospektiv sammenlignende ikke-interventionel kohorteundersøgelse foretaget hos brugere af en anden levonorgestrelbaseret intrauterin enhed og intrauterine kobberanordninger var hyppigheden af perforering hos kvinder, der ammede eller havde indsættelse i op til 36 uger efter fødslen, "ualmindelig" (se pkt.4.4 "Perforering")
Beskrivelse af udvalgte bivirkninger
Tilfælde af overfølsomhed inklusive udslæt, urticaria og angioødem er blevet observeret ved brug af en anden levonorgestrel-baseret IUS.
Hos kvinder, der bliver gravide, mens de bruger Jaydess, øges den relative sandsynlighed for en ektopisk graviditet (se pkt. 4.4 under Ektopisk graviditet).
Ledningerne, der bruges til at fjerne enheden, kan mærkes af partneren under samleje.
Følgende bivirkninger er blevet rapporteret i forbindelse med Jaydess indsættelses- eller fjernelsesprocedure:
smerter på grund af proceduren, blødning under proceduren, indsættelsesrelateret vasovagal reaktion med svimmelhed eller synkope.Proceduren kan udløse et anfald hos patienter med epilepsi.
For andre IUD'er er der rapporteret tilfælde af sepsis (herunder gruppe A streptokok -sepsis) efter indsættelse (se pkt. 4.4 Bækkeninfektion).
Pædiatrisk population
Sikkerhedsprofilen for Jaydess fra en undersøgelse af 304 unge stemmer overens med den, der blev observeret hos den voksne befolkning
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet er
vigtigt, da det muliggør kontinuerlig overvågning af fordel -risiko -forholdet for medicinen.
Sundhedspersonale bedes rapportere alle formodede bivirkninger via systemet
national rapportering på adressen https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Overdosering
Ikke relevant.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: Plastic IUD med gestagen, ATC -kode: G02BA03
Farmakodynamiske virkninger
Jaydess er hovedsageligt udstyret med lokale progestin -virkninger i livmoderhulen.
Den høje endometriekoncentration af levonorgestrel forårsager et fald i endometriale østrogen- og progesteronreceptorer. Endometriet bliver relativt ufølsomt for cirkulerende østradiol og en markant antiproliferativ virkning observeres. Under brug, morfologiske ændringer i endometriet og en let fremmedlegemsreaktion. Den tættere livmoderhals slim forhindrer transit af spermatozoer ind i livmoderhalskanalen. Det lokale miljø i livmoderen og æggelederne hæmmer mobilitet og funktion af spermatozoer og derfor befrugtning. I de kliniske undersøgelser udført med Jaydess blev der observeret ægløsning i størstedelen af subpopulationen af mennesker studerede. Der blev fundet tegn på ægløsning hos 34 ud af 35 kvinder i det første år, hos 26 ud af 27 kvinder i det andet år og hos alle 27 kvinder i det tredje år.
Klinisk effekt og sikkerhed
Jaydess 'præventionsmåde blev undersøgt i et klinisk studie med 1.432 kvinder i alderen 18 til 35 år, omfattende 38,8% af nulliparous, hvoraf 83,6% var nulligravid under brug af Jaydess .. 1-årige Pearl Index var 0,41 (95% konfidensinterval 0,13 - 0,96) og det 3 -årige Pearl Index var 0,33 (95% konfidensinterval 95% svarende til 0,16 - 0,60). Fejlfrekvensen var ca. 0,4% efter 1 år, og den kumulative fejlfrekvens var ca. 0,9% efter 3 år . svigt omfatter også graviditet på grund af udiagnosticerede udvisninger og perforeringer Brug af et intrauterint system, der frigiver levonorgestrel, kompromitterer ikke fremtidig fertilitet. Baseret på data indhentet med en højere dosis levonorgestrel-baseret IUS, blev cirka 80% af de kvinder, der planlægger graviditet, undfanget inden for 12 måneder efter fjernelse af systemet.
Sikkerhedsprofilen for Jaydess fra en undersøgelse af 304 unge stemmer overens med den observerede hos den voksne befolkning. Den forventede effekt er den samme for unge under 18 år som for brugere i alderen 18 og derover.
Hos Jaydess skyldes ændringer i menstruationscyklussen den direkte virkning af levonorgestrel på endometriet og afspejler muligvis ikke æggestokkens cyklus. Der er ingen tydelige forskelle i follikeludvikling, ægløsning eller østradiol og progesteronproduktion hos kvinder med forskellige menstruationsegenskaber. I processen med at hæmme spredning af endometrium kan der forekomme en indledende stigning i pletdannelse i de første måneders brug. Efterfølgende resulterer den markante undertrykkelse af endometriet i en reduktion i varigheden og volumenet af menstruationsblodtab under brug af Jaydess. Dårlig strømning udvikler sig ofte til oligomenoré eller amenoré Ovariefunktionen forbliver normal, og østradiolniveauerne forbliver konstante, selv hos brugere af amenorroisk Jaydess.
05.2 "Farmakokinetiske egenskaber
Levonorgestrel frigives lokalt i livmoderhulen. Udgivelseskurven in vivo det er kendetegnet ved en stor indledende reduktion, der gradvist falmer, hvilket giver anledning til en minimumsvariation efter 1 år indtil udgangen af den forventede brugsperiode på 3 år. Anslåede procentdele af frigivelse in vivo på forskellige tidspunkter er vist i tabel 3.
Tabel 3: Estimerede frigivelseshastigheder in vivo baseret på data ex vivo på restindholdet
Absorption
Efter indsættelse frigives levonorgestrel øjeblikkeligt fra IUS i livmoderhulen, som det fremgår af bestemmelsen af serumkoncentrationer.Maksimal serumkoncentration af levonorgestrel opnås i de første to uger efter Jaydess indsættelse. Syv dage efter indsættelse blev en gennemsnitlig levonorgestrel-koncentration på 162 pg / ml bestemt. Efterfølgende falder serumkoncentrationerne af levonorgestrel over tid og når gennemsnitlige koncentrationer på 59 pg / ml efter 3 år. Af et levonorgestrel-frigivende intrauterint system, den høje lokal eksponering for lægemidlet i livmoderhulen resulterer i en markant koncentrationsgradient mellem endometrium og myometrium (endometriumgradient: myometrium> 100) og lave koncentrationer af levonorgestrel i serum (endometriumgradient: serum> 1.000).
Fordeling
Levonorgestrel binder ikke-specifikt til serumalbumin og specifik binding til kønshormontransportproteiner (SHBG). Mindre end 2% af cirkulerende levonorgestrel er til stede i fri form. Levonorgestrel binder SHBG med høj affinitet. Som følge heraf vil ændringer i serum SHBG-koncentration resultere i en stigning (ved højere SHBG -koncentrationer) eller fald (ved lavere SHBG -koncentrationer) i total serum levonorgestrel -koncentration. Inden for en måned efter Jaydess -indsættelse falder SHBG -koncentrationen. ca. 30%. Koncentrationer af SHBG observeres efterfølgende a plateau, med en tendens til at stige til baseline niveauer med tiden.Det gennemsnitlige tilsyneladende fordelingsvolumen for levonorgestrel er cirka 106 liter.
Biotransformation
Levonorgestrel metaboliseres i vid udstrækning. De vigtigste plasmametabolitter er de konjugerede og ukonjugerede former af 3a, 5b-tetrahydrolevonorgestrel. Baseret på undersøgelserne in vitro Og in vivo, CYP3A4 er det vigtigste enzym, der er involveret i metabolismen af levonorgestrel.
Eliminering
Total clearance af levonorgestrel fra plasma er ca. 1,0 ml / min / kg. Kun spor af levonorgestrel udskilles i uændret form. Metabolitterne udskilles i fæces og urin med et udskillelsesforhold på ca. 1. Halveringstiden for udskillelse er ca. 1 dag.
Linearitet / ikke-linearitet
Levonorgestrels farmakokinetik afhænger af koncentrationen af SHBG, som igen påvirkes af østrogener og androgener. En gennemsnitlig reduktion i SHBG på ca. 30% observeres i den første måned, Jaydess blev brugt, med deraf følgende reduktion i serum levonorgestrel, et tegn på ikke-lineær farmakokinetik af levonorgestrel med hensyn til tid. På grund af den hovedsageligt lokale handling fra Jaydess forventes der ingen konsekvenser for Jaydess 'effekt.
Pædiatrisk population
I et etårigt fase 3-studie hos postmenarche-unge (middelalder 16,2 i intervallet 12-18 år) viste den farmakokinetiske analyse af 283 forsøgspersoner lidt højere (10%) estimerede LNG-koncentrationer hos unge versus voksne Dette resultat korrelerer med de generelt lavere ungdoms kropsvægt.De estimerede intervaller for unge ligger dog inden for dem, der er estimeret for voksne, hvilket viser en høj grad af lighed.
05.3 Prækliniske sikkerhedsdata
Ikke-kliniske data afslører ingen særlig fare for mennesker baseret på konventionelle undersøgelser af sikkerhedsfarmakologi, farmakokinetik og toksicitet, herunder gentoksicitet og carcinogent potentiale for levonorgestrel. Undersøgelser udført på aber med intrauterin frigivelse af levonorgestrel i 9-12 måneder bekræftede lokal farmakologisk aktivitet med god tolerabilitet og fravær af tegn på systemisk toksicitet. Hos kaniner blev der ikke fundet embryonal toksicitet efter intrauterin administration af levonorgestrel. Sikkerhedsvurderinger af de elastomere komponenter i hormonreservoiret, produktets polyethylenmateriale, sølvprofilen og kombinationen af elastomer og levonorgestrel, baseret på evaluering af gentoksicitet i standardtest in vitro Og in vivo og biokompatibilitetstest hos mus, rotter, marsvin, kaniner og i test in vitroviste ikke tilstedeværelse af biologisk uforenelighed.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Polydimethylsiloxan elastomer
Vandfri kolloid silica
Polyethylen
Bariumsulfat
Sort jernoxid (E172)
Sølv
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
3 år.
06.4 Særlige opbevaringsforhold
Denne medicin kræver ingen særlige opbevaringsbetingelser.
06.5 Den umiddelbare emballages art og emballagens indhold
Produktet leveres enkeltvis i en termoformet blister (PETG) med åbning (PE).
Emballage: 1x1 og 5x1.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
06.6 Brugsanvisning og håndtering
Produktet leveres i en steril emballage, der ikke må åbnes, før det indsættes. Hvert system skal håndteres under aseptiske forhold. Hvis tætningen af den sterile emballage brydes, skal det indeholdte system bortskaffes i overensstemmelse med lokale bestemmelser om farligt medicinsk affald. På samme måde skal det fjernede Jaydess -system og indføreren bortskaffes. Den ydre emballage og den indre blister kan bortskaffes som husholdningsaffald.
Indsættelse af en sundhedsperson under aseptiske forhold (se afsnit 4.2).
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Bayer S.p.A - Viale Certosa 130 - 20156 Milano
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
042522019 - "13,5 MG INTRAUTERINE RELEASE SYSTEM", 1 PTEG / PE BLISTER
042522021 - "13,5 MG INTRAUTERINE RELEASE SYSTEM", 5 x 1 PTEG / PE BLISTER
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 13.12.2013
10.0 DATO FOR REVISION AF TEKSTEN
07/2015