I organisk kemi, med udtrykket raceme - eller racemisk blanding - s "betyder en 1: 1 (dermed ækvimolær) blanding af to enantiomerer. Enantiomerer defineres som spejlbilleder af det samme molekyle, der ikke kan overlejres hinanden.
Organiske molekyler, der ikke kan overlejres på deres eget spejlbillede, kaldes molekyler chiral; præcis som vores venstre hånd ikke er overlejret på vores højre hånd (fra græsk jubel "hånd", hvorfra udtrykket chiral blev født).

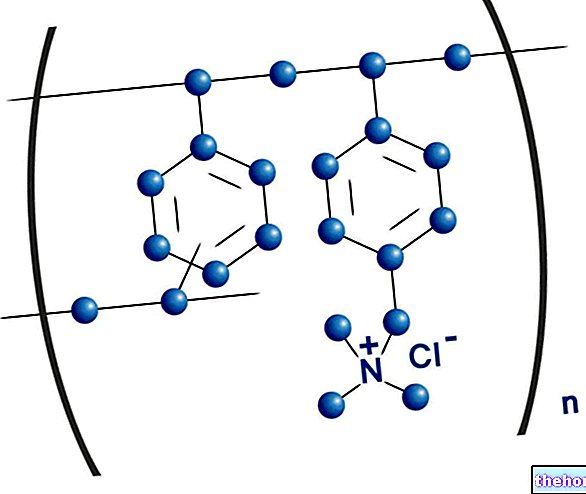
Eksempel på de to enantiomerer af et raceme
Et organisk molekyle er chiralt, hvis det - inden for sin struktur - har et tetraedert atom (normalt et carbonatom, men kan også være et andet atom) bundet til fire forskellige atomer eller grupper. Et carbonatom, der binder fire atomer eller grupper, der er forskellige fra hinanden og blottet for elementer af symmetri siges chiralt center eller chiralitetens centrum.
For bedre at forstå chiralitetsbegrebet er følgende et eksempel på enantiomererne af 2-butanol:
Som du kan se, er de to molekyler det ene spejlbillede af det andet. De har de samme atomer - forbundet på samme måde - men orienteret på en anden måde i rummet, og det gør dem ikke overlejrede.
Enantiomerer skelnes fra hinanden baseret på absolut konfiguration af det chirale center. Det system, der stadig bruges i dag til at tildele den absolutte konfiguration til de kirale centre, er defineret Cahn-Ingold-Prelog-stævne eller konvention R, S, opkaldt efter forskerne, der opfandt det i slutningen af 1950'erne.
Endvidere kan enantiomerer skelnes på grundlag af deres optiske rotationseffekt. Faktisk besidder molekyler med kirale centre i deres struktur evnen til at rotere planet for polariseret lys; de siges at være sammensat optisk aktiv. Der er imidlertid også chirale molekyler, der ikke er i stand til at rotere polariseret lys.
Hvis et molekyle roterer planet for polariseret lys med uret - så fra venstre mod højre - kaldes det højrehåndet eller dextrorotatorisk. Hvis molekylet derimod roterer lyset mod uret - derfor fra højre til venstre - er det defineret venstrehåndet eller levorotatorisk.
Et højrehåndet molekyle er normalt angivet ved at præfiksere sit navn med tegnet "+"eller brevet"d", mens et venstrehåndet molekyle er angivet ved at præfiksere sit navn med tegnet"-"eller brevet"L'.
For hvert par enantiomerer er den ene dextrorotatorisk og den anden venstrehåndet, men den absolutte værdi af den optiske rotationseffekt er den samme. Derfor et raceme - hvori der er en ækvimolær blanding af enantiomerer og derfor indeholder det samme tal af dextrorotatoriske og levorotatoriske molekyler - besidder ingen optisk rotationseffekt og defineres som optisk inaktiv.