Definition af osmose
Osmose er spontan passage af et opløsningsmiddel (som i biologiske systemer normalt er vand), fra opløsningen, hvor de opløste stoffer er mere fortyndet til det, hvori de er mere koncentrerede; denne bevægelse - der sker gennem en semipermeabel membran - fortsætter, indtil der er nået en ligevægtssituation, hvor begge løsninger opnår og opretholder den samme koncentration.
Praktisk eksempel

For bedre at tydeliggøre begrebet osmose, lad os forestille os, at vi har en beholder opdelt i to rum med samme volumen (A og B) af en semipermeabel membran (det vil sige kun permeabel for opløsningsmidlet - i dette tilfælde vand - og ikke for rum A. der er en vandig opløsning, hvori en spiseskefuld glucose er opløst, mens vi i del B har en vandig opløsning med samme volumen, hvor tre spiseskefulde glucose er opløst (det er derfor mere koncentreret). Dette forskel skaber en koncentrationsgradient for glukose på siderne af membranen, og da dette sukker ikke kan krydse det, opnås ligevægt med vandets passage fra rum A (hvor glukose er mere fortyndet) mod rum B (hvor det er mere rigeligt ). Hvis du foretrækker det, kan det også siges, at vandet passerer osmose fra opløsningen, hvor det er mere koncentreret (A) til det, hvor det er mindre koncentreret (B).
Efter denne strømning stiger og falder vandstanden i B i A, hvilket skaber en vis niveauforskel mellem de to. Dette fænomen slutter, når de to løsninger når den samme koncentration og derefter holder den konstant.
Hypotoniske, isotoniske og hypertoniske løsninger
Ved at tage to opløsninger med forskellig molkoncentration (forskelligt antal partikler opløst i dem) defineres opløsningen med den laveste molkoncentration som hypotonisk, og den mere koncentrerede er hypertonisk. To løsninger er i stedet isotoniske (eller ækvimolære), når de har samme koncentration.
I det netop fremstillede eksempel er løsning B hypertonisk (derfor indeholder den flere opløste stoffer) end den anden (defineret som hypotonisk); derfor flytter opløsningsmidlet under normale betingelser ved osmose fra den hypotoniske til den hypertoniske opløsning. Vi talte om standardbetingelser, fordi det ved at lege med fysikkens love er muligt at vælte selve begrebet osmose og favorisere passage af opløsningsmidlet fra den mest fortyndede koncentration til den mest koncentrerede (omvendt osmose).
Osmotisk tryk og omvendt osmose
Som udtrykt hidtil fortsætter nettostrømmen af opløsningsmidlet - genereret af osmose - indtil de to opløsninger har nået den samme koncentration. Nå, denne bevægelse kan modvirkes, stoppes eller endda vendes ved at lægge pres på rummet med den højeste koncentration.

I det foregående eksempel er det tilstrækkeligt at placere et stempel i rum B (som vi husker at have en højere koncentration) og skubbe det ned med en bestemt kraft for at favorisere vandets passage mod A; i dette tilfælde taler vi omvendt osmose.
Osmotisk tryk er det tryk, der præcist modsætter sig opløsningsmidlets passage gennem den semipermeable membran; derfor er det det nødvendige tryk for at modvirke osmose.
For hvad der er blevet sagt indtil videre, har to isotoniske løsninger det samme osmotiske tryk; det bør derfor understreges, at det osmotiske tryk udelukkende afhænger af antallet af partikler, der er til stede i opløsningen og ikke af deres art.
Osmose og menneskekroppen
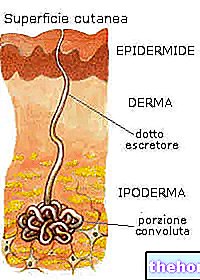
Plasmamembraner, der omgiver cellerne i menneskekroppen, er faktisk halvgennemtrængelige membraner, som tillader direkte passage gennem osmose af små molekyler (såsom vand og urinstof), men ikke af dem med større molekylvægt ( såsom proteiner, aminosyrer og sukkerarter). Osmotiske balancer i kropsvæsker er derfor afgørende for at sikre cellerne et optimalt miljø at leve i.
Hvis vi tager en celle som en rød blodlegeme og nedsænker den i en hypotonisk opløsning, undergår denne - ved osmose - en hævelse (forårsaget af indtrængen af vand), som endda kan få den til at eksplodere. Tværtimod, hvis den er nedsænket i en hypertonisk opløsning cellen, den gennemgår på grund af vandets passage mod ydersiden, en alvorlig dehydrering, der får den til at rynke. Heldigvis er celler i den menneskelige organisme nedsænket i isotoniske løsninger med hensyn til deres indre miljø, og der er forskellige systemer til at holde disse væsker i osmotisk ligevægt.
Osmotisk tryk og opbevaring af mad
Lad os tænke et øjeblik over en hjemmelavet marmelade ... sukker tilsættes i overflod ikke kun for at forbedre dens smag, men også og frem for alt for at øge holdbarheden. Alligevel er sukker et vigtigt element i livet for mange mikroorganismer, der er involveret i nedbrydningen af produktet. Denne tilsyneladende modsætning er demonteret af selve begrebet osmose.