Aktive ingredienser: Apripitant
EMEND 125 mg hårde kapsler
EMEND 80 mg hårde kapsler
Emend indlægssedler er tilgængelige til pakningsstørrelser: - EMEND 125 mg hårde kapsler, EMEND 80 mg hårde kapsler
- EMEND 125 mg pulver til oral suspension
Hvorfor bruges Emend? Hvad er det for?
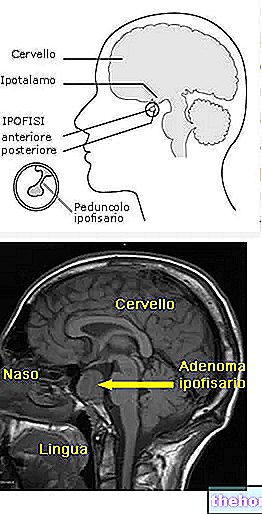
EMEND indeholder det aktive stof aprepitant og tilhører en gruppe lægemidler kaldet 'neurokinin 1 (NK1) receptorantagonister'. Hjernen har et specifikt "område, der styrer kvalme og opkastning. EMEND virker ved at blokere de signaler, der sendes til dette område, og reducerer derved kvalme og opkastning. EMEND -kapsler bruges til voksne og unge i alderen 12 og derover sammen med andre. Medicin til forebyggelse af kvalme og opkastning forårsaget af kemoterapibehandlinger (kræftbehandlinger), som er stærke og moderate inducere af kvalme og opkastning (f.eks. cisplatin, cyclophosphamid, doxorubicin eller epirubicin).
Kontraindikationer Når Emend ikke bør bruges
Tag ikke EMEND:
- hvis du eller barnet er allergisk over for aprepitant eller et af de øvrige indholdsstoffer i denne medicin
- med medicin, der indeholder pimozid (et stof, der bruges til behandling af psykiatriske sygdomme), terfenadin og astemizol (bruges til høfeber og andre allergier), cisaprid (bruges til behandling af fordøjelsesproblemer). Fortæl det til lægen, hvis du eller barnet tager disse lægemidler, da behandlingen skal ændres, før du eller barnet begynder at tage EMEND.
Forholdsregler ved brug Hvad du skal vide, før du tager Emend
Tal med din læge, apotek eller sygeplejerske, før du tager EMEND eller giver denne medicin til dit barn.
Inden behandling med denne medicin, skal du fortælle det til din læge, hvis du eller barnet har en leversygdom, fordi leveren er vigtig for at nedbryde medicinen i kroppen. Din læge kan derfor have brug for at kontrollere leverens eller barnets tilstand.
Børn og unge
Giv ikke EMEND 80 mg kapsler til børn under 12 år, da 80 mg kapslerne ikke er blevet undersøgt i denne population.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre effekten af Emend
EMEND kan påvirke andre lægemidler både under og efter behandling med EMEND. Der er nogle lægemidler, der ikke bør tages sammen med EMEND (såsom pimozid, terfenadin, astemizol og cisaprid) eller som kræver dosisjustering (se også: "Tag ikke EMEND").
Virkningerne af EMEND eller andre lægemidler kan påvirkes, hvis du eller dit barn tager EMEND sammen med andre lægemidler, herunder dem, der er anført nedenfor. Fortæl det til din læge eller apotek, hvis du eller dit barn tager nogen af følgende lægemidler:
- p-piller, der kan omfatte p-piller, hudplastre, implantater og nogle hormonfrigivende intrauterine enheder (IUD'er) virker muligvis ikke korrekt, når de tages sammen med EMEND. En anden eller yderligere ikke-hormonel prævention bør anvendes under behandling med EMEND og i op til 2 måneder efter brug af EMEND.
- cyclosporin, tacrolimus, sirolimus, everolimus (immunsuppressiva)
- alfentanil, fentanyl (bruges til behandling af smerter)
- kinidin (bruges til behandling af uregelmæssig hjerterytme)
- irinotecan, etoposid, vinorelbin, ifosfamid (medicin mod kræft)
- medicin, der indeholder ergot-afledte alkaloider, såsom ergotamin og diergotamin (bruges til behandling af migræne)
- warfarin, acenocoumarol (antikoagulantia; blodprøver kan være nødvendige)
- rifampicin, clarithromycin, telithromycin (antibiotika til behandling af infektioner)
- phenytoin (en medicin, der bruges til at behandle anfald)
- carbamazepin (bruges til behandling af depression og epilepsi)
- midazolam, triazolam, phenobarbital (medicin, der bruges til at berolige eller hjælpe dig med at sove)
- Perikon (et naturlægemiddel til behandling af depression)
- proteasehæmmere (bruges til behandling af HIV -infektioner)
- ketoconazol undtagen shampoo (bruges til behandling af Cushings syndrom, som er karakteriseret ved, at kroppen laver for meget cortisol)
- itraconazol, voriconazol, posaconazol (svampemidler)
- nefazodon (bruges til behandling af depression)
- kortikosteroider (såsom dexamethason og methylprednisolon)
- medicin mod angst (f.eks. alprazolam)
- tolbutamid (et lægemiddel til behandling af diabetes) Fortæl det til din læge eller apotek, hvis du eller dit barn tager, for nylig har taget eller måske tager anden medicin.
Fortæl det til din læge eller apoteket, hvis du eller dit barn tager, for nylig har taget eller måske tager anden medicin.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Denne medicin bør ikke bruges under graviditet, medmindre det er klart nødvendigt. Hvis du eller barnet er gravid, tror at du er gravid eller planlægger at blive gravid eller ammer, skal du spørge din læge til råds, før du tager denne medicin.
For information om prævention, se "Andre lægemidler og EMEND".
Det vides ikke, om EMEND udskilles i modermælk; Amning anbefales derfor ikke under behandling med denne medicin. Inden du tager denne medicin er det vigtigt at fortælle det til din læge, hvis du eller barnet ammer eller tænker på at amme.
Kørsel og brug af maskiner
Det skal tages i betragtning, at nogle mennesker føler sig svimmel og søvnige efter at have taget EMEND. Hvis du eller dit barn føler sig svimmel eller søvnig, skal du undgå at køre, cykle eller bruge maskiner eller værktøjer efter at have taget denne medicin. (Se "Mulige bivirkninger").
EMEND indeholder saccharose
EMEND kapsler indeholder saccharose. Hvis din læge har fortalt dig, at du eller barnet ikke tåler visse sukkerarter, skal du kontakte din læge, før du tager denne medicin.
Dosis, metode og administrationstidspunkt Sådan bruges Emend: Dosering
Tag altid denne medicin eller giv denne medicin til dit barn nøjagtigt som din læge, apotek eller sygeplejerske har fortalt dig. Spørg din læge, apotek eller sygeplejerske, hvis du er i tvivl. Tag altid EMEND sammen med andre lægemidler for at forhindre kvalme og opkastning. Efter behandling med EMEND kan din læge bede dig eller dit barn om at fortsætte med at tage anden medicin, herunder et kortikosteroid (f.eks. Dexamethason) og en "5-HT3-antagonist" (f.eks. "Ondansetron) for at forhindre kvalme og opkastning. Kontakt din læge, apotek eller sygeplejerske, hvis du ikke er sikker.
Den anbefalede orale dosis EMEND er:
- Dag 1:
- en kapsel på 125 mg 1 time før kemoterapisessionen påbegyndes
- Dag 2 og 3:
- en 80 mg kapsel hver dag.
- Hvis der ikke gives kemoterapi, skal du tage EMEND om morgenen.
- Hvis der gives kemoterapi, skal du tage
EMEND 1 time før du starter kemoterapisessionen. EMEND kan tages med eller uden mad.
Synk kapslen hel med væske.
Hvis du har glemt at tage EMEND
Spørg din læge til råds, hvis du eller barnet savner en dosis.
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af dette lægemiddel.
Overdosering Hvad skal man gøre, hvis man har taget for meget Emend
Tag ikke flere kapsler end anbefalet af din læge. Hvis du eller barnet har taget for mange kapsler, skal du straks kontakte din læge.
Bivirkninger Hvad er bivirkningerne af Emend
Ligesom al anden medicin kan denne medicin forårsage bivirkninger, men ikke alle får bivirkninger.
Stop med at tage EMEND og kontakt straks en læge, hvis du eller dit barn bemærker nogen af følgende bivirkninger, som kan være alvorlige, og som du eller dit barn kan få brug for akut lægehjælp til:
- nældefeber, udslæt, kløe, vejrtræknings- eller synkebesvær (frekvens ikke kendt, kan ikke estimeres ud fra tilgængelige data) disse er tegn på en allergisk reaktion.
Andre bivirkninger, der er blevet rapporteret, er angivet nedenfor.
Almindelige bivirkninger (kan forekomme hos op til 1 ud af 10 personer) er:
- forstoppelse, fordøjelsesbesvær
- hovedpine
- træthed
- mistet appetiten
- hikke
- stigning i mængden af leverenzymer i blodet.
Ikke almindelige bivirkninger (kan forekomme hos op til 1 ud af 100 personer) er:
- svimmelhed, søvnighed,
- acne, udslæt
- angst,
- rapning
- kvalme, opkastning, halsbrand, mavesmerter, mundtørhed, vind
- øget smerte eller forbrænding ved vandladning
- svaghed, generel følelse af at være utilpas
- rødme i ansigtet eller huden
- hurtige eller uregelmæssige hjerteslag
- feber med øget risiko for infektion, sænkning af røde blodlegemer.
Sjældne bivirkninger (kan forekomme hos op til 1 ud af 1.000 mennesker) er:
- problemer med at tænke, mangel på energi, ændret smag
- hudens følsomhed over for solen, overdreven svedtendens, fedtet hud, hudlæsioner, kløende udslæt, Stevens-Johnsons syndrom / toksisk epidermal nekrolyse (en sjælden alvorlig hudreaktion)
- eufori (følelse af ekstrem lykke), desorientering
- bakteriel infektion, svampeinfektion
- alvorlig forstoppelse, mavesår, betændelse i tyndtarmen og tyktarmen, læsioner i munden, tarmgas
- hyppig vandladning, mere urin end normalt, sukker eller blod i urinen
- ubehag i brystet, hævelse, ændringer i din måde at gå på
- hoste, slimudledning bag i halsen, irritation i halsen, nysen, ondt i halsen
- okulær udledning og kløe
- ringer i ørerne
- muskelspasmer, muskelsvaghed
- overdreven tørst
- langsom puls, hjerte- og blodkar sygdom
- sænkning af hvide blodlegemer, sænkning af natriumniveauer i blodet, vægttab.
Indberetning af bivirkninger
Tal med din læge, apotek eller sygeplejerske, hvis du eller barnet får bivirkninger. Du kan også rapportere bivirkninger direkte via det nationale rapporteringssystem.
Ved at rapportere bivirkninger kan du hjælpe med at give flere oplysninger om sikkerheden ved dette lægemiddel.
<Andre oplysninger
Opbevar denne medicin utilgængeligt for børn.
Brug ikke dette lægemiddel efter den udløbsdato, der står på kartonen efter EXP. Udløbsdatoen refererer til den sidste dag i måneden.
Opbevares i den originale emballage for at holde den væk fra fugt.
Fjern ikke kapslen fra blisterpakningen, før du er ved at tage den.
Smid ikke medicin via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Andet "> Andre oplysninger
Hvad EMEND indeholder
EMED 80 mg hårde kapsler:
- Den aktive ingrediens er aprepitant. Hver kapsel indeholder 80 mg aprepitant.
- Øvrige indholdsstoffer er: saccharose, mikrokrystallinsk cellulose (E 460), hydroxypropylcellulose (E 463), natriumlaurylsulfat, gelatine, titandioxid (E 171), shellak, kaliumhydroxid og sort jernoxid (E 172).
EMED 125 mg hårde kapsler:
- Den aktive ingrediens er aprepitant. Hver 125 mg hård kapsel indeholder 125 mg aprepitant.
- Øvrige indholdsstoffer er: saccharose, mikrokrystallinsk cellulose (E 460), hydroxypropylcellulose (E 463), natriumlaurylsulfat, gelatine, titandioxid (E 171), shellak, kaliumhydroxid, sort jernoxid (E 172), rødt jernoxid ( E 172) og gult jernoxid (E 172).
Beskrivelse af hvordan EMEND ser ud og pakningens indhold
EMED 80 mg hårde kapsler:
Den 80 mg hårde kapsel er uigennemsigtig med hvid hætte og krop med "461" og "80 mg" trykt radialt på kroppen i sort blæk.
EMEND 80 mg hårde kapsler fås i følgende pakningsstørrelser:
- Aluminiumsblister indeholdende en 80 mg kapsel
- 2-dages behandlingspakke indeholdende to 80 mg kapsler
- 5 aluminiumsblister, der hver indeholder en 80 mg kapsel
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
EMED 125 mg hårde kapsler:
Den 125 mg hårde kapsel er uigennemsigtig med en hvid krop og pink hætte med "462" og "125 mg" trykt radialt på kroppen i sort blæk.
EMEND 125 mg hårde kapsler fås i følgende pakningsstørrelser:
- Aluminium blisterpakning indeholdende en 125 mg kapsel
- 5 aluminiumsblister, der hver indeholder en 125 mg kapsel
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
EMEND HARDE KAPULER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver 125 mg kapsel indeholder 125 mg aprepitant. Hver 80 mg kapsel indeholder 80 mg aprepitant.
Hjælpestof med kendt effekt
Hver kapsel indeholder 125 mg saccharose (i 125 mg kapslen).
Hjælpestof med kendt effekt
Hver kapsel indeholder 80 mg saccharose (i 80 mg kapslen).
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Hård kapsel.
125 mg kapslerne er uigennemsigtige med en hvid krop og pink hætte med "462" og "125 mg" trykt radialt på kroppen med sort blæk. 80 mg kapslerne er uigennemsigtige med en hvid krop og hætte med "461" og "80 mg" trykt radialt på kroppen i sort blæk.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Forebyggelse af kvalme og opkastning forbundet med stærkt og moderat emetogen kræftkemoterapi hos voksne og unge fra 12 år.
EMEND 125 mg / 80 mg gives som en del af en kombinationsbehandling (se pkt.4.2).
04.2 Dosering og indgivelsesmåde
Dosering
Voksne
EMEND gives i 3 dage som en del af et regime, der indeholder et kortikosteroid og en 5-HT3-antagonist. Den anbefalede dosis er 125 mg oralt en gang dagligt en time før kemoterapi påbegyndes på dag 1 og 80 mg oralt en gang dagligt på dag 2 og 3 om morgenen.
Følgende behandlinger anbefales til voksne til forebyggelse af kvalme og opkastning i forbindelse med emetogen kræftkemoterapi:
Meget emetogent kemoterapiregime
Dexamethason bør administreres 30 minutter før kemoterapibehandling på dag 1 og om morgenen på dag 2 til 4. Dexamethason -dosis tager hensyn til lægemiddelinteraktioner.
Moderat emetogen kemoterapibehandling
Dexamethason bør administreres 30 minutter før kemoterapibehandling på dag 1. Dosis af dexamethason tager hensyn til lægemiddelinteraktioner.
Pædiatrisk population
Teenagere (12 til 17 år)
EMEND gives i 3 dage som en del af et regime, der indeholder en 5-HT3-antagonist. Den anbefalede dosis for EMEND kapsler er 125 mg oralt på dag 1 og 80 mg oralt på dag 2 og 3. EMEND gives oralt 1 time før kemoterapi på dag 1, 2 og 3. Hvis kemoterapi ikke gives på dag 2 og 3 , EMEND bør gives om morgenen. Se produktresuméet (SmPC) for den valgte 5-HT3-antagonist for information om den passende dosis.Hvis et kortikosteroid, såsom dexamethason, administreres samtidigt med EMEND, bør kortikosteroiddosis administreres med 50% af den sædvanlige dosis (se pkt. 4.5 og 5.1).
Sikkerheden og effekten af 80 mg kapsel og 125 mg kapsel er ikke påvist hos børn under 12. Der er ingen data tilgængelige.For information om passende dosering til spædbørn, småbørn og børn fra 6 måneder til under 12 år alder, se produktresuméet for pulveret til oral suspension.
Generel
Effektdata for kombination med andre kortikosteroider og 5-HT3-antagonister er begrænsede. For mere information om samtidig administration med kortikosteroider, se afsnit 4.5. Se produktresuméet for 5-HT3-antagonistlægemidler. Administreret.
Særlige populationer
Ældre (≥ 65 år)
Ingen dosisjustering er nødvendig for ældre (se pkt. 5.2).
Køn
Det er ikke nødvendigt at justere dosis baseret på køn (se pkt. 5.2).
Nedsat nyrefunktion
Ingen dosisjustering er nødvendig for patienter med nedsat nyrefunktion eller for patienter med nyresygdom i slutstadiet, der gennemgår hæmodialyse (se pkt. 5.2).
Nedsat leverfunktion
Ingen dosisjustering er nødvendig for patienter med let nedsat leverfunktion. Der er begrænsede data om patienter med moderat nedsat leverfunktion, og der er ingen data om patienter med svært nedsat leverfunktion. Apripitant bør anvendes med forsigtighed til disse patienter (se pkt. 4.4 og 5.2).
Indgivelsesmåde
De hårde kapsler skal sluges hele.
EMEND kan tages med eller uden mad.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne anført i pkt.6.1.
Samtidig administration med pimozid, terfenadin, astemizol eller cisaprid (se pkt. 4.5).
04.4 Særlige advarsler og passende forholdsregler ved brug
Patienter med moderat til svær leverinsufficiens
Der er begrænsede data om patienter med moderat nedsat leverfunktion og ingen data om patienter med svært nedsat leverfunktion. EMEND bør anvendes med forsigtighed til disse patienter (se pkt. 5.2).
Interaktioner med CYP3A4
EMEND bør anvendes med forsigtighed til patienter i samtidig oral behandling med aktive stoffer, der primært metaboliseres af CYP3A4 og med et snævert terapeutisk område, såsom cyclosporin, tacrolimus, sirolimus, everolimus, alfentanil, ergotafledte alkaloider, fentanyl og kinidin (se pkt.4.5 Desuden skal samtidig administration med irinotecan tages med stor forsigtighed, da kombinationen kan resultere i øget toksicitet.
Samtidig administration med warfarin (et CYP2C9 -substrat)
Hos patienter i kronisk warfarinbehandling bør International Normalized Ratio (INR) overvåges nøje under behandling med EMEND og i 14 dage efter hvert 3-dages forløb af EMEND (se afsnit 4.5).
Samtidig administration med hormonelle præventionsmidler
Effekten af hormonelle præventionsmidler kan reduceres i løbet af og 28 dage efter administration af EMEND. Under behandling med EMEND og i 2 måneder efter administrationen af den sidste dosis EMEND bør alternative ikke-hormonelle substitutionsmetoder anvendes (se afsnit 4.5 ).
Hjælpestoffer
EMEND kapsler indeholder saccharose. Patienter med sjældne arvelige problemer med fructoseintolerance, glucose-galactose malabsorption eller sucrase-isomaltase-insufficiens bør ikke tage denne medicin.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
L "aprepitant (125 mg / 80 mg) er et substrat, moderat inhibitor og inducer af CYP3A4. L" aprepitant er også en inducer af CYP2C9. Der er hæmning af CYP3A4 under behandling med EMEND. Ved afslutning af behandlingen forårsager EMEND en forbigående mild induktion af CYP2C9, CYP3A4 og glucuronidering. Aperpitant ser ikke ud til at interagere med transport P-glycoprotein, hvilket antydes af den manglende interaktion mellem aprepitant og digoxin.
Virkning af aprepitant på andre aktive stoffers farmakokinetik
CYP3A4 -hæmning
Som en moderat hæmmer af CYP3A4 kan aprepitant (125 mg / 80 mg) øge plasmakoncentrationerne af samtidig administrerede CYP3A4-metaboliserede aktive stoffer.Den samlede eksponering af samtidig administrerede CYP3A4-substrater kan stige til cirka 3 gange i løbet af den 3-dages behandling med EMEND; den forventede effekt af aprepitant på plasmakoncentrationer af CYP3A4 -substrater administreret intravenøst forventes at være lavere. EMEND må ikke anvendes samtidigt med pimozid, terfenadin, astemizol eller cisaprid (se afsnit 4.3). Hæmning af CYP3A4 af aprepitant kan resultere i forhøjede plasmakoncentrationer af disse aktive stoffer, hvilket potentielt kan forårsage alvorlige og livstruende reaktioner. Der udvises forsigtighed ved samtidig administration af EMEND og oralt administrerede aktive stoffer, der primært metaboliseres af CYP3A4 og med et snævert terapeutisk område, såsom cyclosporin, tacrolimus, sirolimus, everolimus, alfentanil, diergotamin, ergotamin, fentanyl og kinidin (se pkt. 4.4).
Kortikosteroider
Dexamethason: Den sædvanlige orale dosis dexamethason bør reduceres med cirka 50%, når det administreres samtidigt med et terapeutisk regime med EMEND 125 mg / 80 mg. Dosis af dexamethason i kemoterapi -inducerede kvalme og opkastning blev valgt under hensyntagen til lægemiddelinteraktioner (se pkt.4.2). EMEND, givet som et regime på 125 mg med 20 mg dexamethason i kombination oralt på dag 1, og EMEND givet i en dosis på 80 mg / dag med 8 mg dexamethason i kombination oralt på dag 2 til 5, øgede AUC for dexamethason, et CYP3A4-substrat, 2,2 gange på dag 1 og 5.
Methylprednisolon: Den sædvanlige intravenøse methylprednisolondosis bør reduceres med cirka 25%, og den sædvanlige orale methylprednisolondosis bør reduceres med cirka 50%, når den administreres samtidigt med et terapeutisk regime med EMEND 125 mg / 80 mg. Ved indgivelse som en del af et 125 mg -regime på dag 1 og 80 mg / dag på dag 2 og 3 øgede EMEND AUC for methylprednisolon, et CYP3A4 -substrat, med 1,3 gange på dag 1 og 2,5 gange på dag 3, hvor methylprednisolon blev administreres samtidigt intravenøst i doser på 125 mg på dag 1 og oralt i doser på 40 mg på dag 2 og 3.
Under fortsat behandling med methylprednisolon kan AUC for methylprednisolon falde sent inden for 2 uger efter påbegyndelse af EMEND -dosis på grund af den inducerende effekt af aprepitant på CYP3A4. Denne effekt forventes at være mere udtalt ved administration af oral methylprednisolon.
Kemoterapi medicin
I de farmakokinetiske undersøgelser ændrede EMEND, når det blev administreret med et regime på 125 mg / dag på dag 1 og 80 mg / dag på dag 2 og 3, ikke farmakokinetikken for docetaxel administreret intravenøst på dag 1 eller vinorelbin administreret intravenøst på dag 1 eller dag 8. Fordi effekten af EMEND på farmakokinetikken af oralt administrerede CYP3A4 -substrater er bedre end effekten af EMEND på farmakokinetikken af intravenøse CYP3A4 -substrater, en interaktion med kemoterapiprodukter administreret til oralt metaboliseret hovedsageligt eller delvist af CYP3A4 (f.eks. etoposid Forsigtighed tilrådes, og yderligere overvågning er påkrævet hos patienter, der modtager lægemidler, der hovedsageligt eller delvist metaboliseres af CYP3A4 (se pkt. 4.4) Efter markedsføring af neurotoksicitet, en potentiel bivirkning af ifosfamid, er blevet rapporteret dop eller samtidig administration af aprepitant og ifosfamid.
Immunsuppressive midler
Under det 3-dages regime til behandling af CINV forventes en moderat forbigående stigning efterfulgt af et let fald i eksponeringen af CYP3A4-metaboliserede immunsuppressiva (f.eks. Cyclosporin, tacrolimus, everolimus og sirolimus). Varighed af 3-dages behandling og begrænset tid -afhængige ændringer i eksponeringen, ingen dosisreduktion af immunsuppressiva anbefales under 3-dages samtidig administration med EMEND.
Midazolam
De potentielle virkninger af øgede koncentrationer af midazolam eller andre benzodiazepiner, der metaboliseres via CYP3A4 (alprazolam, triazolam), bør overvejes, når disse lægemidler administreres samtidigt med EMEND (125 mg / 80 mg).
EMEND øgede AUC for midazolam, et følsomt substrat for CYP3A4, med 2,3 gange på dag 1 og 3,3 gange på dag 5, da en enkelt 2 mg dosis midazolam blev administreret på dag 1 og dag 5 i et behandlingsforløb med EMEND 125 mg på dag 1 og 80 mg / dag på dag 2 til 5.
I en anden undersøgelse med intravenøs administration af midazolam blev EMEND administreret i en dosis på 125 mg på dag 1 og 80 mg / dag på dag 2 og 3, og 2 mg midazolam blev administreret intravenøst inden administration af den 3-dages terapeutiske cyklus med EMEND og på dag 4, 8 og 15. EMEND øgede AUC for midazolam med 25% på dag 4 og reducerede AUC for midazolam med 19% på dag 8 og 4% på dag 15 Disse virkninger blev ikke anset for klinisk vigtige.
I en tredje undersøgelse med intravenøs og oral midazolam -administration blev EMEND administreret i en dosis på 125 mg på dag 1 og 80 mg / dag på dag 2 og 3 sammen med ondansetron 32 mg på dag 1, dexamethason 12 mg på dag 1 og 8 mg på dag 2-4. Denne kombination (EMEND, ondansetron og dexamethason) reducerede AUC for oral midazolam med 16% på dag 6, 9% på dag 8, 7% på dag 15 og 17% på dag 22. Disse virkninger blev ikke anset for klinisk vigtige.
En yderligere undersøgelse blev afsluttet med intravenøs administration af midazolam og EMEND.
2 mg intravenøs midazolam blev administreret 1 time efter oral administration af en enkelt dosis EMEND 125 mg. Plasma-AUC for midazolam steg 1,5 gange. Denne effekt blev ikke betragtet som klinisk vigtig.
Induktion
Som en mild inducer af CYP2C9, CYP3A4 og glucuronidering kan aprepitant reducere plasmakoncentrationen af substrater, der ryddes af disse metaboliske veje inden for to uger efter behandlingsstart. Denne effekt bliver først tydelig efter afslutningen af den 3 -dages behandling med EMEND. For CYP2C9 og CYP3A4-substrater er induktion forbigående med maksimal effekt 3-5 dage efter, at 3-dages behandling med EMEND er afsluttet.Effekten opretholdes i et par dage, formindskes derefter langsomt og er klinisk ubetydelig. Efter to uger efter behandlingens ophør. med EMEND. En let induktion af glucuronidering observeres også med 80 mg oralt aprepitant administreret i 7 dage. Der mangler data om virkningerne på CYP2C8 og CYP2C19. Der udvises forsigtighed ved administration af warfarin, acenocoumarol, tolbutamid, phenytoin eller andre aktive stoffer, der vides at blive metaboliseret af CYP2C9 inden for dette tidsinterval.
Warfarin
Hos patienter i kronisk warfarinbehandling bør protrombintid (INR) overvåges nøje under behandling med EMEND og i 2 uger efter hvert 3-dages EMEND-forløb for kemoterapi-induceret kvalme og opkastning (se pkt. 4.4). Når en enkelt 125 mg EMEND -dosis blev givet på dag 1, og en dosis på 80 mg / dag blev givet på dag 2 og 3 til raske mennesker stabiliseret på kronisk warfarinbehandling, var der ingen effekt af EMEND på plasma -AUC for R (+ ) eller "(S-) warfarin bestemt på dag 3; c" var imidlertid et fald på 34% i lavkoncentrationen af S (-) warfarin (et CYP2C9-substrat) ledsaget af et fald på 14% i INR 5 dage efter behandlingens ophør med EMEND.
Tolbutamid
Ved indgivelse i en dosis på 125 mg på dag 1 og 80 mg / dag på dag 2 og 3 reducerede EMEND AUC for tolbutamid (et CYP2C9 -substrat) med 23% på dag 4, med 28% på dag 8 og 15% på dag 15, hvor en enkelt dosis på 500 mg tolbutamid blev administreret oralt før administration af det 3-dages forløb af EMEND og på dag 4, 8 og 15.
Hormonale præventionsmidler
Effekten af hormonelle præventionsmidler kan reduceres i løbet af og i 28 dage efter administration af EMEND. Alternative ikke-hormonelle substitutionsmetoder bør anvendes under behandling med EMEND og i 2 måneder efter administration af den sidste dosis EMEND.
I et klinisk studie blev enkeltdoser af et oralt præventionsmiddel indeholdende ethinylestradiol og norethindron administreret på dag 1 til dag 21 med EMEND, i et regime på 125 mg på dag 8 og 80 mg / dag på dage 9 og 10 med ondansetron 32. intravenøst mg på dag 8 og oral dexamethason givet i doser på 12 mg på dag 8 og 8 mg / dag på dag 9, 10 og 11. I løbet af dag 9 til og med 21 i denne undersøgelse var der et fald op til 64 % af lavkoncentrationerne af ethinylestradiol og fald med op til 60% af lavkoncentrationerne af norethindron.
5-HT3 antagonister
I kliniske interaktionsundersøgelser havde aprepitant ingen klinisk relevant effekt på ondansetrons, granisetrons eller hydrodolasetrons farmakokinetik (dolasetrons aktive metabolit).
Virkninger af andre lægemidler på aprepitants farmakokinetik
Samtidig administration af EMEND med aktive stoffer, der hæmmer CYP3A4-aktivitet (f.eks. Ketoconazol, itraconazol, voriconazol, posaconazol, clarithromycin, telithromycin, nefazodon og proteasehæmmere) bør overvejes med forsigtighed, da kombinationen forventes at resultere i en flere gange stigning i plasmakoncentrationer af aprepitant (se pkt. 4.4).
Samtidig administration af EMEND med aktive stoffer stærke inducere af CYP3A4 -aktivitet (f.eks. Rifampicin, phenytoin, carbamazepin, phenobarbital) bør undgås, da kombinationen resulterer i reduktioner i plasmakoncentrationer af aprepitant, hvilket kan resultere i nedsat effekt af EMEND. EMEND med naturlægemidler, der indeholder perikon (Hypericum perforatum) anbefales ikke.
Ketoconazol
Ved administration som en enkelt dosis på 125 mg aprepitant på dag 5 i et 10-dages behandlingsforløb med ketoconazol, en stærk CYP3A4-hæmmer, ved en dosis på 400 mg / dag, steg AUC for aprepitant med cirka 5. og middelværdien terminal halveringstid for aprepitant steg ca. 3 gange.
Rifampicin
Ved administration af en enkelt dosis på 375 mg aprepitant på dag 9 i et 14-dages behandlingsforløb med 600 mg rifampicin / dag, en stærk CYP3A4-inducer, faldt "aprepitant AUC med 91% og" gennemsnitlig terminal halveringstid faldt med 68%.
Pædiatrisk population
Interaktionsundersøgelser er kun blevet udført hos voksne.
04.6 Graviditet og amning
Prævention hos mænd og kvinder
Effekten af hormonelle præventionsmidler kan reduceres under og i 28 dage efter administration af EMEND. Under behandling med EMEND og i 2 måneder efter administration af den sidste dosis EMEND bør alternative ikke-hormonelle substitutionsmetoder anvendes (se afsnit 4.4 og 4.5).
Graviditet
Der foreligger ingen kliniske data om brug af aprepitant under graviditet Potentialet for reproduktionstoksicitet af aprepitant er ikke fuldt ud blevet karakteriseret, da eksponeringsniveauer over terapeutisk eksponering ved 125 mg -dosis ikke kunne opnås i dyreforsøg. / 80 mg hos mennesker. Disse undersøgelser indikerede ikke direkte eller indirekte skadelige virkninger med hensyn til graviditet, embryoføtal udvikling, fødsel eller postnatal udvikling (se pkt. 5.3). De potentielle virkninger på reproduktion af ændringer i neurokinregulering er ukendte. EMEND bør ikke anvendes under graviditet, medmindre det er klart nødvendigt.
Fodringstid
Aperpitant udskilles i mælken hos rotter under amning Det vides ikke, om aprepitant udskilles i modermælk; amning anbefales derfor ikke under behandling med EMEND.
Fertilitet
Potentialet for aprepitants virkning på fertiliteten blev ikke fuldt ud karakteriseret som højere end terapeutiske eksponeringsniveauer hos mennesker ikke kunne opnås i dyreforsøg Disse fertilitetsstudier indikerede ikke direkte eller indirekte skadelige virkninger i forhold til parringsevne, fertilitet, embryo / fosterudvikling eller sædtal og motilitet (se pkt. 5.3).
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
EMEND kan påvirke evnen til at køre bil, cykle eller betjene maskiner en smule. Svimmelhed og træthed kan forekomme efter administration af EMEND (se pkt.4.8).
04.8 Bivirkninger
Resumé af sikkerhedsprofilen
Sikkerhedsprofilen for aprepitant blev evalueret hos cirka 6.500 voksne i mere end 50 undersøgelser og 184 børn og unge i 2 pilotpædiatriske kliniske undersøgelser.
De mest almindelige bivirkninger rapporteret med en højere forekomst hos voksne behandlet med aprepitant end med standardterapi hos patienter, der modtog stærkt emetogen kemoterapi (HEC) var: hikke (4,6% versus 2,9%), øget alaninaminotransferase (ALAT) (2,8% versus 1,1%), dyspepsi (2,6%mod 2,0%), forstoppelse (2,4%mod 2,0%), hovedpine (2,0%mod 1,8%) og nedsat appetit (2,0%mod 0,5%). Den hyppigste bivirkning rapporteret med højere forekomsten hos patienter behandlet med aprepitant end med standardterapi hos patienter, der fik moderat emetogen kemoterapi (MEC), var træthed (1,4% versus 0,9%).
De mest almindelige bivirkninger rapporteret med en højere forekomst hos pædiatriske patienter, der blev behandlet med aprepitant end i kontrolplanen samtidigt med administration af emetogen kræftkemoterapi, var hikke (3,3%vs. 0,0%) og rødme (1,1%). Vs. 0,0% ).
Tabel med liste over bivirkninger
Følgende bivirkninger blev observeret i en analyse fra HEC- og MEC-undersøgelser med en højere forekomst af aprepitant end den, der blev rapporteret ved standardterapi hos voksne eller pædiatriske patienter eller efter markedsføring. Hyppighedskategorierne i tabellen er baseret på undersøgelser og udført hos voksne; frekvenser observeret i pædiatriske undersøgelser var ens eller lavere, medmindre det er angivet i tabellen. Nogle mindre almindelige bivirkninger i den voksne befolkning blev ikke observeret i pædiatriske undersøgelser.
Frekvenser defineres som: meget almindelig (≥ 1/10); almindelig (≥ 1/100,
† Kvalme og opkastning var effektparametre i de første 5 dage efter kemoterapibehandling og blev derefter kun rapporteret som bivirkninger.
Beskrivelse af udvalgte bivirkninger
Bivirkningsprofilen hos voksne i multiple-cycle-forlængelsen af undersøgelser med HEC og MEC op til 6 yderligere cyklusser af kemoterapi lignede generelt den, der blev observeret i cyklus 1.
I et yderligere aktivt kontrolleret klinisk studie med 1169 voksne patienter, der fik aprepitant og HEC, var bivirkningsprofilen generelt den samme som i andre HEC-undersøgelser med aprepitant.
Yderligere bivirkninger blev observeret hos voksne patienter, der blev behandlet med aprepitant for postoperativ kvalme og opkastning (PONV) ved en forekomst højere end den, der blev rapporteret med ondansetron: smerter i øvre del af maven, abdominal auskultatorisk abnormitet, forstoppelse *, dysartri, dyspnø, hypoestesi, søvnløshed, miosis, kvalme, sanseforstyrrelser, ubehag i maven, suboklusion *, nedsat synsstyrke, hvæsen.
* Rapporteret hos patienter, der tager en højere dosis aprepitant.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det muliggør løbende overvågning af lægemidlets nytte / risiko -forhold.Professionelle sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det italienske lægemiddelagentur. , websted: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Overdosering
I tilfælde af overdosering bør behandlingen med EMEND afbrydes, patienten overvåges og der træffes generelle støttende foranstaltninger. På grund af de antiemetiske virkninger af aprepitant er lægemiddelinduceret emese muligvis ikke effektiv.
Apripitant kan ikke fjernes ved hæmodialyse.
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk klassifikation: antiemetika og kvalme, ATC -kode: A04AD12
Aperpitant er en selektiv menneskelig substans P -antagonist med høj affinitet for neurokinin 1 (NK1) -receptorer.
3-dages behandling med aprepitant hos voksne
I 2 randomiserede, dobbeltblinde undersøgelser med i alt 1.094 voksne patienter behandlet med kemoterapi inklusive cisplatin ≥ 70 mg / m2 blev aprepitant i kombination med ondansetron / dexamethasonbehandling (se pkt. 4.2) sammenlignet med standard (placebo plus ondansetron 32 mg intravenøst givet på dag 1 plus dexamethason 20 mg oralt på dag 1 og 8 mg to gange dagligt på dag 2 og 4). Selvom en 32 mg intravenøs dosis ondansetron blev brugt i kliniske forsøg, er dette ikke længere den anbefalede dosis. Se produktinformation for den valgte 5-HT3-antagonist for passende dosisinformation.
Effektiviteten var baseret på vurdering af følgende sammensatte mål: fuldstændig respons (defineret som ingen episoder med opkastning og ingen brug af redningsterapi) hovedsageligt under cyklus 1.Resultaterne blev evalueret for hver enkelt undersøgelse og for de 2 samlede undersøgelser.
En oversigt over de vigtigste undersøgelsesresultater baseret på den kombinerede analyse er vist i tabel 1.
tabel 1
Procentdel af voksne patienter, der modtager stærkt emetogen kemoterapibehandling
og som reagerede på behandling efter behandlingsgruppe og fase - cyklus 1
* Konfidensintervaller blev beregnet uden justeringer for køn og samtidig kemoterapi, der tidligere var inkluderet i den primære analyse af oddsforhold og logistiske modeller.
† En patient i Apripitant -behandlingsgruppen havde kun data i den akutte fase og blev ekskluderet fra de samlede og forsinkede faseanalyser; en patient i standardbehandlingsgruppen havde kun data i den forsinkede fase og blev ekskluderet. Fra den globale analyse og fra den akutte fase analyse.
Statistisk signifikante forskelle i effekt blev også observeret i hver af de 2 individuelle undersøgelser.
I de samme 2 kliniske undersøgelser fortsatte 851 voksne patienter i forlængelsen med flere cyklusser i op til 5 yderligere kemoterapiforløb. Effekten af aprepitant behandling blev tilsyneladende opretholdt gennem alle forløb.
I en dobbeltblind, randomiseret undersøgelse af i alt 866 voksne patienter (864 kvinder og 2 mænd), der fik kemoterapibehandling med cyclophosphamid 750-1.500 mg / m2 eller cyclophosphamid 500-1.500 mg / m2 og doxorubicin (≤ 60 mg / m2 ) eller epirubicin (≤ 100 mg / m2), aprepitant i kombination med ondansetron / dexamethason (se afsnit 4.2) blev sammenlignet med standardterapi [placebo plus ondansetron 8 mg oralt (to gange på dag 1 og hver 12. time på dag 2 og 3) plus dexamethason 20 mg oralt på dag 1].
Effektiviteten blev vurderet på grundlag af et sammensat mål: fuldstændig respons (defineret som ingen episoder med opkastning og ingen brug af redningsterapi) hovedsageligt under cyklus 1.
En oversigt over de vigtigste undersøgelsesresultater er vist i tabel 2.
Tabel 2
Procentdel af voksne patienter, der modtager moderat emetogen kemoterapibehandling og reagerer på behandling efter behandlingsgruppe og fase - Cyklus 1
* Konfidensintervaller blev beregnet uden alderskategorijusteringer (
† En patient i Apripitant -behandlingsgruppen havde kun data om akutte faser og blev ekskluderet fra de samlede og forsinkede faseanalyser.
I det samme kliniske studie fortsatte 744 voksne patienter forlængelsen med flere cyklusser i op til 3 yderligere kemoterapiforløb. Effekten af aprepitant behandling blev tilsyneladende opretholdt i alle forløb.
I et andet multicenter, randomiseret, dobbeltblindet, parallelt klinisk forsøg blev behandling med aprepitant sammenlignet med standardterapi hos 848 voksne patienter (652 kvinder, 196 mænd), der fik kemoterapibehandling med enhver intravenøs dosis oxaliplatin., Carboplatin, epirubicin , idarubicin, ifosfamid, irinotecan, daunorubicin, doxorubicin; intravenøs cyclophosphamid; eller intravenøs cytarabin (> 1 g / m2). Patienter behandlet med aprepitant modtog kemoterapi for forskellige former for kræft omfattende 52% af patienterne med brystkræft, 21% med forskellige former for mave -tarmkræft, herunder kolorektal cancer, 13% med lungekræft og 6%. Med forskellige former for gynækologisk kræft. Aperpitant i kombination med ondansetron / dexamethason (se pkt. 4.2) blev sammenlignet med standardterapi [placebo med oral ondansetron 8 mg (to gange på dag 1 og hver 12. time på dag 2 og 3) plus dexamethason 20 mg oralt på dag 1].
Effekten var baseret på vurdering af følgende primære og centrale sekundære endepunkter: fravær af opkastning i den samlede periode (0 til 120 timer efter kemoterapi), vurdering af sikkerhed og tolerabilitet ved behandling af kemoterapi-induceret kvalme og opkastning (CINV) med aprepitant og fuldstændig respons (defineret som fravær af opkastning og redningsterapi) i den samlede periode (0 til 120 timer efter kemoterapi). Desuden var fraværet af betydelig kvalme i den samlede periode (0 til 120 timer efter kemoterapi) evalueret som et undersøgende endepunkt, både i den akutte og i den forsinkede fase som en post-hoc analyse.
En oversigt over de vigtigste undersøgelsesresultater er vist i tabel 3.
Tabel 3
Procentdel af voksne patienter, der reagerer efter behandlingsgruppe og fase for undersøgelse 2 - Cyklus 1 Moderat emetogen kemoterapi
* Konfidensintervaller blev beregnet uden justeringer for køn og region, som blev inkluderet i den primære analyse ved hjælp af logistiske modeller.
Fordelen ved kombinationsbehandling med aprepitant i hele undersøgelsespopulationen var hovedsageligt drevet af resultaterne observeret hos patienter med dårlig kontrol med standardterapi såvel som hos kvinder, selvom resultaterne var numerisk overlegne uanset alder, tumortype eller køn. Komplet respons på aprepitant og standardterapibehandling blev opnået hos henholdsvis 209 af 324 (65%) og 161 af 320 (50%) kvinder og 83 af 101 (82%) og 68 af 87 (78%).
Pædiatrisk population
I et randomiseret, dobbeltblindet, aktivt kontrolleret klinisk forsøg med 302 børn og unge (i alderen 6 måneder til 17 år) behandlet med moderat eller stærkt emetogen kemoterapi blev aprepitant-regimet sammenlignet med et kontrolregime til forebyggelse af CINV. Effekten af aprepitant-regimet blev vurderet i en enkelt cyklus (cyklus 1). Patienterne havde mulighed for at modtage open-label aprepitant i efterfølgende cyklusser (valgfri cyklus 2-6); i disse valgfrie cykler er effekten imidlertid ikke blevet evalueret. Aprepitant-regimet for unge i alderen 12-17 år (n = 47) involverede administration af EMEND 125 mg kapsler oralt på dag 1 og administration af 80 mg / dag på dag 2 og 3 i kombination med ondansetron på dag 1. Aprepitant -regimet for børn fra 6 måneder til under 12 år (n = 105) bestod i administration af EMEND -pulver til suspension oral 3,0 mg / kg (op til 125 mg) oralt den dag 1 og 2,0 mg / kg (op til 80 mg) oralt på dag 2 og 3 i kombination med ondansetron på dag 1. Regimekontrollen hos unge i alderen 12-17 år (n = 48) og børn i alderen 6 måneder til mindre end 12 år (n = 102) bestod af administration af placebo i stedet for aprepitant på dag 1, 2 og 3 i kombination med ondansetron på dag 1. EMEND eller placebo og ondansetron blev givet henholdsvis 1 time og 30 minutter før ved kemoterapiens start. Intravenøs administration af dexamethason var tilladt i forbindelse med det antiemetiske regime til pædiatriske patienter i begge aldersgrupper efter lægens skøn. En reduktion (50%) af dexamethason -dosis var påkrævet for pædiatriske patienter behandlet med aprepitant. Der var ikke planlagt dosisreduktioner for pædiatriske patienter, der blev behandlet med kontrolregimet. Af pædiatriske patienter brugte 29% i aprepitantregimet og 28% i kontrolregime dexamethason som en komponent i cyklus 1 -regimet.
Den antiemetiske aktivitet af EMEND blev vurderet i en periode på 5 dage (120 timer) efter initiering af kemoterapi på dag 1. Det primære endepunkt var fuldstændig respons i den forsinkede fase (25-120 timer efter initiering). Af kemoterapi) i cyklus 1 En oversigt over undersøgelsens hovedresultater er vist i tabel 4.
Tabel 4
Antal (%) pædiatriske patienter med komplet respons og ingen opkastning efter behandlingsgruppe og fase-Cyklus 1 (hensigt-til-behandling-population)
Estimeret tid til første opkastningsepisode efter initiering af kemoterapi var længere med aprepitant (estimeret mediantid til første opkastningsepisode på 94,5 timer) end i kontrolgruppen (estimeret mediantid til første opkastningsepisode på 26, 0 timer).
En "effektanalyse i delpopulationer i cyklus 1 viste, at uanset alderskategori, køn, brug af dexamethason til antiemetisk profylakse og" kemoterapiens emetogenicitet, gav aprepitantregimet mulighed for bedre kontrol. Sammenlignet med kontrolregimet for komplette responsendepunkter.
05.2 Farmakokinetiske egenskaber
Aperpitant udviser ikke-lineær farmakokinetik. Både clearance og absolut biotilgængelighed falder med stigende dosis.
Absorption
Den gennemsnitlige absolutte orale biotilgængelighed af aprepitant er 67% for 80 mg kapsel og 59% for kapsel 125 mg. Den gennemsnitlige maksimal plasmakoncentration (Cmax) for aprepitant forekom efter ca. 4 timer (tmax). Oral administration af kapslen med en standard morgenmad på ca. 800 Kcal resulterede i en stigning på op til 40% i AUC for aprepitant. Denne stigning anses ikke for klinisk relevant.
Farmakokinetikken for aprepitant er ikke-lineær over hele det kliniske dosisinterval. Hos raske unge voksne er stigningen i AUC0-? mellem 80 mg og 125 mg i enkeltdoser administreret til fodrede personer var det 26% højere end dosisproportionaliteten.
Efter oral administration af en enkelt 125 mg dosis EMEND på dag 1 og 80 mg én gang dagligt på dag 2 og 3 var AUC0-24h (middelværdi ± SD) 19,6 ± 2, 5 mcg • time / ml og 21,2 ± 6,3 mcg • h / ml på henholdsvis dag 1 og 3. Cmax var henholdsvis 1,6 ± 0,36 mcg / ml og 1,4 ± 0, 22 mcg / ml på dag 1 og 3.
Fordeling
Aperpitant er stærkt proteinbundet, i gennemsnit 97%. Det geometriske gennemsnitlige tilsyneladende steady-state distributionsvolumen (Vdss) er cirka 66 L hos mennesker.
Biotransformation
Aperpitant metaboliseres i udstrakt grad. Hos raske unge voksne kan cirka 19% af radioaktiviteten i plasma tilskrives aprepitant inden for 72 timer efter administration af en 100 mg dosis [14C] -fosaprepitant, et prodrug af aprepitant., Hvilket indikerer en betydelig tilstedeværelse metabolitter i plasma. Tolv metabolitter af aprepitant er blevet identificeret i human plasma. kun svage tegn på aktivitet in vitro med humane levermikrosomer indikerer, at aprepitant primært metaboliseres via CYP3A4 med potentielle mindre bidrag fra CYP1A2 og CYP2C19.
Eliminering
Aperpitant udskilles ikke uændret i urinen Metabolitterne udskilles i urinen og fæces via galdeudskillelse. Efter en enkelt 100 mg intravenøs dosis [14C] -fosaprepitant, et prodrug af aprepitant, til raske mennesker, blev 57% af radioaktiviteten genfundet i urinen og 45% i fæces.
Plasmaclearance for aprepitant er dosisafhængig, falder med stigende dosis og varierer fra cirka 60 til 72 ml / min inden for det terapeutiske vindue Den terminale halveringstid er cirka 9 til 13 timer.
Farmakokinetik i særlige populationer
Ældre borgere: Efter oral administration af 125 mg enkeltdosis aprepitant på dag 1 og 80 mg én gang dagligt på dag 2 til 5 var AUC0-24h for aprepitant 21% højere på dag 1 og 36% på dag 5 hos ældre (≥ 65 år) Cmax var 10% højere på dag 1 og 24% højere på dag 5 hos ældre end hos unge voksne Disse forskelle anses ikke for at være klinisk signifikante. Ingen dosisjustering af EMEND er påkrævet hos ældre patienter.
Køn: Efter oral administration af en enkelt dosis på 125 mg aprepitant var Cmax for aprepitant 16% højere hos kvinder end hos mænd. Halveringstiden for aprepitant er 25% kortere hos kvinder end hos mænd, og dens tmax nås på omtrent samme tid. Disse forskelle betragtes ikke som klinisk signifikante. Ingen dosisjustering af EMEND er nødvendig baseret på køn.
Nedsat leverfunktion: Let nedsat leverfunktion (Child-Pugh klasse A) påvirker ikke aprepitants farmakokinetik i klinisk relevant omfang. Ingen dosisjustering er nødvendig for patienter med let nedsat leverfunktion. Baseret på tilgængelige data er det ikke muligt at konkludere om effekten af moderat nedsat leverfunktion (Child-Pugh klasse B) på aprepitants farmakokinetik. Der er ingen kliniske eller farmakokinetiske data fra patienter med svært nedsat leverfunktion (Child-Pugh klasse C ).).
Nedsat nyrefunktion: En enkelt dosis på 240 mg aprepitant blev administreret til patienter med svært nedsat nyrefunktion (CrCl
Hos patienter med svært nedsat nyrefunktion faldt AUC for total aprepitant (ubundet og proteinbundet) med 21% og Cmax faldt med 32% sammenlignet med raske mennesker. Hos patienter med ESRD, der gennemgår hæmodialyse, faldt AUC0-? Af total aprepitant med 42%, og Cmax faldt med 32%. På grund af beskedent fald i proteinbinding af aprepitant hos patienter med nyresygdom, blev AUC for det ubundne farmakologisk aktive lægemiddel ikke signifikant ændret hos patienter med nedsat nyrefunktion sammenlignet med raske mennesker Hæmodialysebehandling udført 4 eller 48 timer efter administration havde ingen signifikant effekt på aprepitants farmakokinetik; mindre end 0,2% af dosis blev genfundet i dialysatet.
Ingen dosisjustering af EMEND er nødvendig for patienter med nedsat nyrefunktion eller for patienter med ESRD, der gennemgår hæmodialyse.
Pædiatrisk population: I forbindelse med et 3-dages kursus resulterede administration af aprepitant kapsler (125/80/80 mg) til unge patienter (i alderen 12-17 år) i en AUC0-24 timer større end 17 mcg • h/ml på dag 1 med koncentrationer (Cmin) ved slutningen af dag 2 og 3 over 0,4 mcg / ml hos de fleste patienter. Den mediane maksimale plasmakoncentration (Cmax) var ca. 1,3 mcg / ml på dag 1 og nås efter ca. 4 timer. I forbindelse med et 3-dages kursus resulterede administration af aprepitant pulver til oral suspension (3/2/2 mg/kg) hos patienter fra 6 måneder til under 12 år i en højere AUC0-24 timer ved 17 mcg • h / ml på dag 1 med koncentrationer (Cmin) ved slutningen af dag 2 og 3 over 0,1 mcg / ml hos de fleste patienter. Den mediane maksimale plasmakoncentration (Cmax) var ca. 1,2 mcg / ml på dag 1 og nås mellem 5 og 7 timer.
En populationsfarmakokinetisk analyse af administrationen af aprepitant til pædiatriske patienter (i alderen 6 måneder til 17 år) tyder på, at køn og race ikke har nogen klinisk signifikant effekt på aprepitants farmakokinetik.
Forholdet mellem koncentration og effekt
Positronemissionstomografi (PET) -undersøgelser hos raske unge mænd, der anvender meget specifikke sporstoffer til NK1-receptorer, har vist, at aprepitant trænger ind i hjernen og optager NK1-receptorerne i en dosis og koncentrationsafhængigt omfang i plasma. Beregner, at plasmakoncentrationerne af aprepitant opnået med det 3-dages terapeutiske forløb med EMEND hos voksne resulterer i en belægning af hjernens NK1-receptorer større end 95%.
05.3 Prækliniske sikkerhedsdata
Ikke-kliniske data afslører ingen fare for mennesker baseret på konventionelle undersøgelser af enkelt- og gentagen dosetoksicitet, gentoksicitet, kræftfremkaldende potentiale, reproduktionstoksicitet og udviklingstoksicitet. Det skal dog bemærkes, at systemisk eksponering hos gnavere var ens eller endda lavere end den terapeutiske eksponering hos mennesker i en dosis på 125 mg / 80 mg. Selv om der ikke blev observeret negative virkninger på menneskelige eksponeringsniveauer i reproduktive undersøgelser, er dyreeksponering ikke tilstrækkelig til at foretage en tilstrækkelig menneskelig risikovurdering.
I et ungtoksicitetsstudie hos rotter behandlet fra postnatal dag 10 til dag 63 inducerede aprepitant "tidlig vaginal åbning hos hunner, der startede med 250 mg / kg to gange og forsinket adskillelse af forhud hos hundyr. Hannkøn startede med 10 mg / kg to gange Der var ingen margen for klinisk relevant eksponering. Der var ingen tegn på behandlingsrelaterede virkninger på parring, fertilitet eller embryoføtal overlevelse, og der var heller ingen patologiske ændringer i reproduktionsorganerne. I et ungtoksicitetsstudie hos hunde behandlet fra postnatal dag 14 til dag 42 blev der observeret en reduktion i testikelvægt og Leydig -cellestørrelse hos mænd i en dosis på 6 mg / kg / dag og vægtforøgelse i livmoderen, hypertrofi af livmoderen og livmoderhals og ødem i vaginale væv blev observeret hos hunprøver fra 4 mg / kg / dag. Der var ingen "margin for" klinisk relevant eksponering af aprepitant. For kortvarig behandling i henhold til det anbefalede doseringsregime anses disse data for usandsynligt at have klinisk relevans.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Kapselindhold
Saccharose
Mikrokrystallinsk cellulose (E 460)
Hydroxypropylcellulose (E 463)
Natriumlaurylsulfat
Kapselskal (125 mg)
Gele
Titandioxid (E 171)
Rødt jernoxid (E 172)
Gul jernoxid (E 172)
Kapselskal (80 mg)
Gele
Titandioxid (E 171)
Trykfarve
Shellac
Kaliumhydroxid
Sort jernoxid (E 172)
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
4 år.
06.4 Særlige opbevaringsforhold
Opbevares i den originale emballage for at beskytte mod fugt.
06.5 Den umiddelbare emballages art og emballagens indhold
Der findes forskellige typer emballage, herunder forskellige formuleringer.
Aluminiumsblister med en 80 mg kapsel.
Aluminiumsblister med to 80 mg kapsler.
5 aluminiumsblister hver med en 80 mg kapsel.
Aluminiumsblister med en 125 mg kapsel.
5 aluminiumsblister hver med en 125 mg kapsel.
Aluminiumsblister med en 125 mg kapsel og to 80 mg kapsler.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner til bortskaffelse.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Merck Sharp & Dohme Ltd.
Hertford Road, Hoddesdon
Hertfordshire EN11 9BU
Storbritannien
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU/1/03/262/001
EU/1/03/262/002
EU/1/03/262/003
EU/1/03/262/004
EU/1/03/262/005
EU/1/03/262/006
036167043
036167068
036167017
036167029
036167056
036167031
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 11. november 2003
Dato for seneste fornyelse: 22. september 2008
10.0 DATO FOR REVISION AF TEKSTEN
23. marts 2016