Aktive ingredienser: Rasagiline
AZILECT 1 mg tabletter
Indikationer Hvorfor bruges Azilect? Hvad er det for?
AZILECT bruges til behandling af Parkinsons sygdom. Det kan bruges med eller uden Levodopa (en anden medicin til behandling af Parkinsons sygdom).
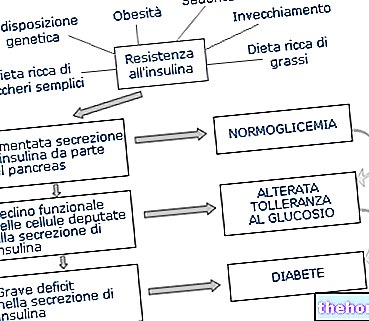
Med Parkinsons sygdom forekommer tab af dopaminerge celler i visse områder af hjernen. Dopamin er et hjernestof, der er ansvarligt for at kontrollere bevægelse. AZILECT hjælper med at øge og vedligeholde dopaminniveauer i hjernen.
Kontraindikationer Når Azilect ikke bør bruges
Tag ikke AZILECT:
- hvis du er allergisk (overfølsom) over for rasagilin eller et af de øvrige indholdsstoffer i AZILECT.
- hvis du lider af alvorlig leverinsufficiens.
Tag ikke følgende medicin i kombination med AZILECT:
- monoaminoxidase (MAO) -hæmmere (bruges som antidepressiva, til behandling af Parkinsins sygdom eller til enhver anden indikation), herunder ikke-receptpligtig medicin og naturlige produkter, såsom perikon.
- pethidin (et stærkt smertestillende middel).
Vent mindst 14 dage efter at behandlingen med AZILECT er stoppet, før du starter behandling med MAO -hæmmere eller pethidin.
Forholdsregler ved brug Hvad du skal vide, før du tager Azilect
Vær særlig forsigtig med AZILECT
- Ved let til moderat nedsat leverfunktion.
- Kontakt din læge ved mistanke om hudforandringer.
Børn
Brug af AZILECT til patienter under 18 år anbefales ikke.
Interaktioner Hvilke lægemidler eller fødevarer kan ændre virkningen af Azilect
Fortæl det til din læge eller apotek, hvis du tager eller for nylig har taget anden medicin, herunder medicin, der er købt uden recept, og hvis du er ryger eller har til hensigt at stoppe med at ryge.
Spørg din læge til råds, før du tager nogen af følgende lægemidler i kombination med AZILECT:
- nogle antidepressiva (selektive serotonin genoptagelseshæmmere, selektive serotonin og noradrenalin genoptagelseshæmmere, tricykliske eller tetracykliske antidepressiva)
- antibiotikumet ciprofloxacin, der bruges til behandling af infektioner
- dextromethorphan, en medicin, der bruges til hoste
- sympatomimetika, såsom dem, der findes i øjendråber, nasale og orale decongestanter og kolde lægemidler, der indeholder efedrin eller pseudoephedrin.
Undgå samtidig brug af AZILECT og antidepressiva, der indeholder fluoxetin eller fluvoxamin. Inden behandling påbegyndes med AZILECT, skal du vente mindst fem uger efter, at behandlingen med fluoxetin er stoppet.
Inden behandlingen påbegyndes med fluoxetin eller fluvoxamin, skal du vente mindst 14 dage efter at behandlingen med AZILECT er stoppet.
Fortæl det til din læge, hvis du, din familie eller omsorgspersoner bemærker, at du udvikler usædvanlig adfærd, der gør, at du ikke kan modstå trangen, trangen eller ønsket om at deltage i visse aktiviteter, der er farlige eller skadelige for dig eller dem. Andre. Denne adfærd kaldes impulskontrolforstyrrelser Adfærd som tvang, tvangstanker, spilafhængighed, overforbrug er blevet observeret hos patienter, der tager AZILECT og / eller anden medicin, der bruges til behandling af Parkinsons sygdom. impulsiv adfærd og unormalt højt seksuelt begær eller en stigning i seksuelle tanker eller ønsker. . Din læge skal muligvis ændre din dosis eller stoppe behandlingen
Brug af AZILECT sammen med mad og drikke
AZILECT kan tages med eller uden mad.
Advarsler Det er vigtigt at vide, at:
Graviditet og amning
Spørg din læge eller apotek til råds, før du tager medicin.
Kørsel og brug af maskiner
Der er ikke udført undersøgelser af virkningerne på evnen til at føre motorkøretøj eller betjene maskiner. Spørg din læge til råds, før du kører bil og bruger maskiner.
Dosis, metode og administrationstidspunkt Sådan bruges Azilect: Dosering
Tag altid AZILECT nøjagtigt efter lægens anvisning. Hvis du er i tvivl, skal du kontakte din læge eller apotek.
Den sædvanlige dosis AZILECT er 1 tablet på 1 mg taget gennem munden, en gang dagligt. AZILECT kan tages med eller uden mad.
Overdosering Hvad skal man gøre, hvis man har taget for meget Azilect
Hvis du har taget for meget AZILECT, end du burde
Hvis du tror, at du har taget flere AZILECT -tabletter, end du burde, skal du straks kontakte din læge eller apotek. Tag AZILECT -blisteren / flasken med dig for at vise lægen eller apoteket.
Hvis du har glemt at tage AZILECT
Tag ikke en dobbeltdosis som erstatning for en glemt tablet. Tag din næste dosis som normalt, når det er tid til at tage den.
Hvis du holder op med at tage AZILECT
Spørg din læge eller apotek, hvis du har yderligere spørgsmål om brugen af AZILECT.
Bivirkninger Hvad er bivirkningerne af Azilect
Som al anden medicin kan AZILECT forårsage bivirkninger, men ikke alle får bivirkninger.
Følgende bivirkninger er blevet rapporteret i placebokontrollerede kliniske forsøg.
Hyppigheden af mulige bivirkninger anført nedenfor er defineret ved hjælp af følgende konventioner:
- Meget almindelig (hos mere end 1 ud af 10 patienter)
- Almindelig (1 til 10 ud af 100 patienter)
- Ikke almindelig (1 til 10 ud af 1.000 patienter)
- Sjælden (1 til 10 ud af 10.000 patienter)
- Meget sjælden (færre end 1 ud af 10.000 patienter)
- Ikke kendt (hyppigheden kan ikke estimeres ud fra de tilgængelige data).
Meget normal:
- Unormale bevægelser (dyskinesi)
- hovedpine.
Almindelige:
- mavesmerter
- falder
- allergi,
- feber
- influenzasyndrom (influenza)
- generel følelse af ubehag (utilpashed)
- nakke smerter
- brystsmerter (angina pectoris)
- fald i blodtrykket ved oprejst ledsaget af symptomer som svimmelhed / svimmelhed (ortostatisk hypotension)
- nedsat appetit
- forstoppelse
- tør mund
- kvalme og opkast
- luft i maven
- abnormitet i blodprøveresultater (leukopeni)
- ledsmerter (artralgi)
- muskuloskeletale smerter
- ledbetændelse (gigt)
- følelsesløshed og svaghed i håndmusklen (karpaltunnelsyndrom)
- tab af kropsvægt
- unormale drømme
- besvær med at koordinere muskler (balanceforstyrrelser)
- depression
- svimmelhed
- forlængede muskelsammentrækninger (dystoni)
- løbende næse (rhinitis)
- hudirritation (dermatitis)
- erytem
- røde øjne (konjunktivitis)
- urinhastighed.
Ualmindelig:
- slagtilfælde (cerebrovaskulært slagtilfælde)
- Hjerteanfald (myokardieinfarkt)
- hudblærer (vesiculobullous erythema).
Derudover blev hudkræft rapporteret hos cirka 1% af patienterne i placebokontrollerede kliniske forsøg.Videnskabelige beviser tyder på, at Parkinsons sygdom, og ikke et bestemt lægemiddel, er forbundet med en højere risiko for hudkræft (ikke kun melanom) Rapporter enhver mistanke hudforandringer til din læge.
Parkinsons sygdom er forbundet med symptomer såsom hallucinationer og forvirring. Efter markedsføringserfaring er disse symptomer også blevet observeret hos patienter med Parkinsons sygdom behandlet med AZILECT.
Der har været tilfælde af patienter, der, mens de tog et eller flere lægemidler til behandling af Parkinsons sygdom, ikke var i stand til at modstå trangen, lysten eller fristelsen til at udføre en handling, der kunne have været skadelig for dem selv eller andre. Denne adfærd kaldes impuls Følgende adfærd er observeret hos patienter, der tager AZILECT og / eller anden medicin, der bruges til behandling af Parkinsons sygdom:
- Tvangstanker eller impulsiv adfærd.
- Stærk impuls til at spille overdrevent på trods af alvorlige personlige eller familiemæssige konsekvenser.
- Ændret eller øget seksuel interesse og adfærd af væsentlig bekymring for dig selv eller andre, for eksempel en stigning i seksuel lyst. - Ukontrollerbare og overdrevne udgifter eller køb.
Fortæl din læge, hvis nogen af disse adfærd forekommer; du vil diskutere måder at håndtere eller reducere symptomer.
Fortæl det til din læge eller apoteket, hvis nogen af bivirkningerne bliver alvorlige, eller du bemærker nogen bivirkninger, der ikke er angivet i denne indlægsseddel.
Udløb og opbevaring
Opbevar AZILECT utilgængeligt for børn.
Brug ikke AZILECT efter den udløbsdato, der står på kartonen, flasken eller kartonen. Udløbsdatoen refererer til den sidste dag i måneden.
Må ikke opbevares over 25 ° C.
Lægemidler bør ikke bortskaffes via spildevand eller husholdningsaffald. Spørg din apotek om, hvordan du skal smide medicin, du ikke længere bruger. Dette vil hjælpe med at beskytte miljøet.
Hvad indeholder AZILECT
- Den aktive ingrediens er rasagilin.Hver tablet indeholder 1 mg rasagilin (som mesylat).
- Øvrige indholdsstoffer er mannitol, vandfri kolloid silica, majsstivelse, prægelatiniseret majsstivelse, stearinsyre, talkum.
Hvordan AZILECT ser ud og pakningens indhold
AZILECT fås i form af hvidhvide tabletter, runde, flade og affasede i kanterne, glatte på den ene side og præget med "GIL" og "1" på den anden.
Tabletterne fås i pakninger med 7, 10, 28, 30, 100 og 112 tabletter eller i flasker med 30 tabletter.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
AZILECT 1 MG TABLETTER
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
Hver tablet indeholder 1 mg rasagilin (mesylat).
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Tablet.
Hvide til råhvide tabletter, runde, flade og skrå i kanterne, glatte på den ene side og præget med "GIL" og "1" på den anden.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
AZILECT er indiceret til behandling af Parkinsons sygdom både som monoterapi (uden levodopa) og som kombinationsbehandling (med levodopa) hos patienter med svingninger ved afslutningen af dosis.
04.2 Dosering og indgivelsesmåde
Dosering
Rasagilin administreres oralt i en dosis på 1 mg, en gang dagligt, med eller uden levodopa.
Det kan tages enten på tom mave eller på fuld mave.
Ældre: Ingen dosisjustering er nødvendig hos ældre patienter.
Pædiatrisk population: Brug af Azilect til børn og unge anbefales ikke på grund af manglende data om sikkerhed og effekt.
Patienter med leverinsufficiens: Anvendelse af rasagilin til patienter med svær leverinsufficiens er kontraindiceret (se pkt. 4.3) Anvendelse af rasagilin til patienter med moderat leverinsufficiens bør undgås. Vær forsigtig, når behandling med rasagilin påbegyndes hos patienter med let leversvigt.
Patienter med nyreinsufficiens: Ingen dosisjustering er nødvendig hos patienter med nyreinsufficiens.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof eller over for et eller flere af hjælpestofferne (se pkt.6.1).
Samtidig behandling med andre monoaminoxidase (MAO) -hæmmere (herunder ikke-receptpligtige lægemidler og naturprodukter, såsom perikon) eller pethidin (se afsnit 4.5) Vent mindst 14 dage mellem behandlingens ophør. Med rasagilin og initiering af behandlingen med MAO -hæmmere eller pethidin.
Anvendelse af rasagilin er kontraindiceret hos patienter med alvorlig leverinsufficiens.
04.4 Særlige advarsler og passende forholdsregler ved brug
Undgå samtidig brug af rasagilin og fluoxetin eller fluvoxamin (se afsnit 4.5) Vent mindst fem uger, efter du har stoppet behandlingen med fluoxetin, før du starter behandling med rasagilin. Vent mindst 14 dage mellem behandlingen med rasagilin stoppes og behandlingen med fluoxetin eller fluvoxamin startes.
Impulskontrolforstyrrelser (ICD'er) kan forekomme hos patienter behandlet med dopaminagonister og / eller dopaminerge behandlinger. Lignende rapporter om impulskontrolforstyrrelser (ICD'er) er blevet modtaget efter markedsføring hos patienter behandlet med rasagilin. Patienter bør overvåges regelmæssigt for udvikling af impulskontrolforstyrrelser. Patienter og pårørende skal være opmærksom på adfærdsmæssige symptomer på impulskontrolforstyrrelser, der er blevet observeret hos patienter behandlet med rasagilin, som omfatter tilfælde af tvang, tvangstanker, patologisk spil, øget libido, hyperseksualitet, impulsiv adfærd og tvangsmæssige udgifter eller køb.
Da rasagilin forstærker virkningerne af levodopa, kan bivirkningerne af levodopa øges, og allerede eksisterende dyskinesi forværres. Reduktion af dosis af levodopa kan forbedre denne bivirkning.
Der har været rapporter om hypotensive virkninger, når rasagilin tages samtidigt med levodopa. Patienter med Parkinsons sygdom er særlig sårbare over for bivirkninger af hypotension på grund af tilstedeværelsen af gangproblemer.
Samtidig brug af rasagilin og dextromethorphan eller sympatomimetika, herunder nasale og orale decongestanter og lægemidler indeholdende efedrin eller psudoephedrin, der anvendes til behandling af forkølelse, anbefales ikke (se pkt. 4.5).
Under det kliniske udviklingsprogram for rasagilin blev der observeret et par tilfælde af melanom, som kunne tyde på en mulig forbindelse med rasagilin. De indsamlede data indikerer, at Parkinsons sygdom, og ikke et bestemt lægemiddel, er forbundet med en højere risiko for hudkræft (ikke kun melanom). Kontakt en specialist i tilfælde af mistanke om hudlæsion.
Vær forsigtig, når du starter behandling med rasagilin hos patienter med let leverinsufficiens.
Undgå brug af rasagilin til patienter med moderat leverinsufficiens Afbryd behandling med rasagilin, hvis mild til moderat leverinsufficiens udvikler sig (se pkt. 5.2).
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Der er en række kendte interaktioner mellem ikke-selektive MAO-hæmmere og andre lægemidler.
Rasagilin bør ikke administreres i kombination med andre MAO-hæmmere (herunder ikke-receptpligtige lægemidler og naturprodukter, såsom "perikon), da der er risiko for" ikke-selektiv MAO-hæmning med mulig anfald af anfald. Hypertensiv (se afsnit 4.3).
Alvorlige bivirkninger er blevet rapporteret ved samtidig brug af pethidin og MAO-hæmmere samt en anden selektiv MAO-B-hæmmer. Samtidig administration af rasagilin og pethidin er kontraindiceret (se pkt. 4.3).
Den samtidige anvendelse af MAO -hæmmere og sympatomimetiske lægemidler har resulteret i fænomener af interaktion mellem lægemidler. Derfor, i betragtning af MAO -hæmmende aktivitet af rasagilin, samtidig administration af rasagilin og sympatomimetika, såsom dem, der findes i nasale decongestanter og orale og kolde lægemidler, der indeholder efedrin eller psudoephedrin ( se afsnit 4.4).
Lægemiddelinteraktioner er blevet rapporteret ved samtidig brug af dextromethorphan og ikke-selektive MAO-hæmmere. På grund af den MAO -hæmmende aktivitet af rasagilin anbefales det derfor ikke samtidig brug af rasagilin og dextromethorphan (se pkt. 4.4).
Undgå samtidig brug af rasagilin og fluoxetin eller fluvoxamin (se pkt. 4.4).
For samtidig brug af rasagilin og selektive serotonin -genoptagelseshæmmere (SSRI'er) / selektive serotonin- og noradrenalin -genoptagelseshæmmere (SNRI'er) i kliniske forsøg, se pkt.4.8.
Alvorlige bivirkninger er blevet rapporteret ved samtidig brug af SSRI'er, SNRI'er, tricykliske og tetracykliske antidepressiva og MAO -hæmmere.Givet rasogilins MAO -hæmmende aktivitet anbefales det derfor at være forsigtig i tilfælde af behandling med antidepressiva.
Der er ikke rapporteret klinisk signifikant effekt af levodopa på rasagilinclearance hos patienter med Parkinsons sygdom på kronisk behandling med levodopa som kombinationslægemiddel.
Uddannelse in vitro på metabolisme viste, at cytochrom P4501A2 (CYP1A2) er det vigtigste enzym, der er ansvarligt for metabolismen af rasagilin. Samtidig administration af rasagilin og ciprofloxacin (en CYP1A2 -hæmmer) resulterede i en stigning på 83% i rasagilin AUC. Samtidig administration af rasagilin og theophyllin (et substrat for CYP1A2) havde ingen effekt på farmakokinetikken af de to produkter. Derfor kan potente CYP1A2 -hæmmere ændre plasmaniveauerne af rasagilin og bør administreres med forsigtighed.
Hos rygepatienter er der risiko for nedsatte plasmaniveauer af rasagilin på grund af induktion af det metaboliserende enzym CYP1A2.
Uddannelse in vitro viste, at rasagilinkoncentrationer på 1 mcg / ml (svarende til et niveau 160 gange den gennemsnitlige Cmax på ~ 5,9-8,5 ng / ml hos Parkinsons sygdomspatienter efter flere doser på 1 mg rasagilin), ikke hæmmede cytochrom P450-isoenzymerne CYP1A2, CYP2A6 , CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4 og CYP4A. Disse resultater viser, at terapeutiske koncentrationer af rasagilin sandsynligvis ikke signifikant forstyrrer substrater af disse enzymer.
Samtidig administration af rasagilin og entacapon resulterede i en stigning på 28% i den orale clearance af rasagilin.
Tyramin / rasagilin interaktion: resultaterne af fem tyraminstimuleringsstudier (hos frivillige og patienter med Parkinsons sygdom) sammen med data fra daglig blodtryksovervågning efter måltider (hos 464 patienter behandlet med 0,5 mg / dag eller 1 mg / dag rasagilin eller placebo som kombinationsbehandling med levodopa i seks måneder uden tyraminrestriktioner), og fraværet af rapporter om en interaktion mellem tyramin og rasagilin i ubegrænsede kliniske forsøg med tyramin indikerer, at rasagilin kan bruges sikkert og uden kostbegrænsninger for tyramin.
04.6 Graviditet og amning
Der foreligger ingen kliniske data om brugen af rasagilin under graviditet. Dyrestudier viser ikke direkte eller indirekte skadelige virkninger med hensyn til graviditet, embryonal / fosterudvikling, fødsel og postnatal udvikling (se pkt. 5.3.). Forsigtighed er nødvendig, når medicinen ordineres til gravide.
Eksperimentelle data indikerer, at rasagilin hæmmer prolaktinsekretion og dermed kan hæmme amning.
Det vides ikke, om rasagilin udskilles i modermælk. Der bør lægges særlig vægt på administration af lægemidlet til ammende kvinder.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Der er ikke udført undersøgelser af evnen til at føre motorkøretøj eller betjene maskiner.
Patienter bør advares om risikoen ved brug af maskiner, herunder motorkøretøjer, indtil de er sikre på, at Azilect ikke har nogen indflydelse på deres evner.
04.8 Bivirkninger
I rasagilins kliniske udviklingsprogram modtog i alt 1.361 patienter 3.076,4 patientår med rasagilin. I dobbeltblinde placebokontrollerede undersøgelser blev 529 patienter svarende til 212 patientår behandlet med rasagilin 1 mg / dag, og 539 patienter svarende til 213 patientår fik placebo.
Monoterapi
Bivirkninger rapporteret med en højere forekomst i placebokontrollerede undersøgelser hos patienter behandlet med rasagilin 1 mg / dag (rasagilin gruppe n = 149, placebogruppe n = 151) er anført nedenfor.
Bivirkninger med mindst 2% forskel fra placebo er rapporteret i kursiv
Antallet i parentes (% af patienterne) angiver forekomsten af bivirkningen i henholdsvis rasagilin vs. placebogruppen.
Bivirkninger er blevet rangeret efter hyppighed ved hjælp af følgende konventioner: meget almindelig (> 1/10), almindelig (> 1/100 til 1 / 1.000 til 1 / 10.000 til
Infektioner og angreb
Almindelige: influenza (4,7% vs. 0,7%)
Godartede, ondartede og uspecificerede neoplasmer (herunder cyster og polypper)
Almindelig: hudkræft (1,3% vs. 0,7%)
Forstyrrelser i blod og lymfesystem
Almindelig: leukopeni (1,3% vs. 0%)
Forstyrrelser i immunsystemet
Almindelige: allergiske reaktioner (1,3% vs. 0,7%)
Metabolisme og ernæringsforstyrrelser
Ikke almindelig: nedsat appetit (0,7% vs. 0%)
Psykiatriske lidelser
Almindelige: depression (5,4% vs. 2%), hallucinationer (1,3% vs. 0,7%)
Nervesystemet lidelser
Meget normal: migræne (14,1% vs. 11,9%)
Ikke almindelig: cerebrovaskulært slagtilfælde (0,7% vs. 0%)
Øjenlidelser
Almindelige: konjunktivitis (2,7% vs. 0,7%)
Øre- og labyrintforstyrrelser
Almindelig: svimmelhed (2,7% vs. 1,3%)
Hjertepatologier
Almindelig: angina pectoris (1,3% vs. 0%)
Ikke almindelig: myokardieinfarkt (0,7% vs. 0%)
Åndedræts-, thorax- og mediastinumforstyrrelser
Almindelige: rhinitis (3,4% vs. 0,7%)
Gastrointestinale lidelser
Almindelig: flatulens (1,3% vs. 0%)
Hud og subkutan væv
Almindelige: dermatitis (2,0% vs. 0%)
Ikke almindelig: vesiculobullous erythema (0,7% vs. 0%)
Muskuloskeletale og bindevævssygdomme
Almindelige: muskuloskeletale smerter (6,7% vs. 2,6%), nakkesmerter (2,7% vs. 0%), gigt (1,3% vs. 0,7%)
Nyre- og urinlidelser
Almindelig: urinhastighed (1,3% vs. 0,7%)
Generelle lidelser og tilstande på administrationsstedet
Almindelig: feber (2,7% vs. 1,3%), utilpashed (2% vs. 0%)
Foreningsterapi
Følgende er bivirkninger set med en højere forekomst i placebokontrollerede undersøgelser hos patienter, der fik rasagilin 1 mg / dag (rasagilin gruppe n = 380, placebogruppe n = 388). Antallet i parentes (% af patienterne) angiver forekomsten af bivirkningen i henholdsvis rasagilin vs. placebogruppen.
Bivirkninger med mindst 2% forskel fra placebo er rapporteret i kursiv.
Bivirkninger er blevet rangeret efter hyppighed ved hjælp af følgende konventioner: meget almindelig (> 1/10), almindelig (> 1/100 til 1 / 1.000 til 1 / 10.000 til
Godartede, ondartede og uspecificerede neoplasmer (herunder cyster og polypper)
Ikke almindelig: kutant melanom (0,5% vs. 0,3%)
Metabolisme og ernæringsforstyrrelser
Almindelig: nedsat appetit (2,4% vs. 0,8%)
Psykiatriske lidelser
Almindelig: hallucinationer (2,9% vs. 2,1%), unormale drømme (2,1% vs. 0,8%)
Ikke almindelig: forvirring (0,8% vs. 0,5%)
Nervesystemet lidelser
Meget normal: dyskinesi (10,5% vs. 6,2%)
Almindelig: dystoni (2,4% vs. 0,8%), karpaltunnelsyndrom (1,3% vs. 0%), balanceforstyrrelser (1,6% vs. 0,3%)
Ikke almindelig: cerebrovaskulær slagtilfælde (0,5% vs. 0,3%)
Hjertepatologier
Ikke almindelig: angina pectoris (0,5% vs. 0%)
Vaskulære patologier
Almindelige: ortostatisk hypotension (3,9% vs. 0,8%)
Gastrointestinale lidelser
Almindelige: mavesmerter (4,2% vs. 1,3%), forstoppelse (4,2% mod 2,1%), kvalme og opkastning (8,4% vs. 6,2%), mundtørhed (3,4% vs. 1,8%)
Hud og subkutan væv
Almindelig: Hududslæt (1,1% vs. 0,3%)
Muskuloskeletale og bindevævssygdomme
Almindelig: artralgi (2,4% vs. 2,1%), nakkesmerter (1,3% vs. 0,5%)
Diagnostiske tests
Almindelige: fald i kropsvægt (4,5% vs. 1,5%)
Skade, forgiftning og komplikationer fra traumer
Almindelig: Efterår (4,7% vs. 3,4%)
Parkinsons sygdom er forbundet med symptomer såsom hallucinationer og forvirring. Efter markedsføring er disse symptomer også set hos patienter med Parkinsons sygdom behandlet med rasagilin.
Forekomsten af alvorlige bivirkninger kendes ved samtidig brug af SSRI'er, SNRI'er, tricykliske og tetracykliske antidepressiva og MAO-hæmmere. Efter markedsføring er der rapporteret tilfælde af serotoninsyndrom forbundet med uro, forvirring, stivhed., Pyreksi og myoklonus hos patienter behandlet med antidepressiva / SNRI'er samtidigt med rasagilin.
I kliniske forsøg med rasagilin var samtidig brug af fluoxetin eller fluvoxamin og rasagilin ikke tilladt, men brug af følgende antidepressiva var tilladt i følgende doser: amitriptylin ≤ 50 mg dagligt, trazodon ≤ 100 mg pr. Dag, citalopram ≤ 20 mg dag, sertralin ≤ 100 mg pr. dag og paroxetin ≤ 30 mg pr. dag. Der blev ikke rapporteret tilfælde af serotoninsyndrom under det rasagilinske kliniske program, hvor 115 patienter blev behandlet samtidigt med rasagilin og tricykliske og 141 patienter blev behandlet med rasagilin og SSRI / SNRI.
Efter markedsføring er der rapporteret tilfælde af forhøjet blodtryk hos patienter, der får rasagilin, herunder sjældne tilfælde af hypertensiv krise efter indtagelse af tyraminrige fødevarer i ukendte mængder.
Tilfælde af lægemiddelinteraktioner med samtidig brug af sympatomimetiske lægemidler er blevet rapporteret med MAO -hæmmere.
Efter markedsføring blev der rapporteret om et tilfælde af forhøjet blodtryk hos en patient, der også brugte en tetrahydrozolinhydrochlorid oftalmisk vasokonstriktor under behandling med rasagilin.
Impulskontrolforstyrrelser
Hos patienter behandlet med dopaminagonister og / eller andre dopaminerge behandlinger kan der opstå patologisk hasardspil, øget libido, hyperseksualitet, tvangshandel eller shopping, overspisning og tvangsspisning. Et lignende billede af impulskontrolforstyrrelser blev registreret, som også omfattede tvang, obsessive tanker og impulsiv adfærd (se pkt. 4.4).
04.9 Overdosering
Overdosering: Symptomer rapporteret efter overdosering med Azilect i doser fra 3 mg til 100 mg inkluderede dysfori, hypomani, hypertensiv krise og serotoninsyndrom.
Overdosering kan være forbundet med betydelig hæmning af MAO-A og MAO-B.
Friske frivillige blev behandlet med 20 mg / dag af produktet i en enkeltdosisundersøgelse eller med 10 mg / dag i et ti-dages studie. De observerede bivirkninger blev vurderet som milde eller moderate og ikke relateret til behandling med rasagilin. Kardiovaskulære bivirkninger (inklusive hypertension og postural hypotension) blev rapporteret i en dosis-eskaleringsundersøgelse hos patienter i kronisk levodopa-behandling behandlet med rasagilin 10 mg / dag og forsvandt ved afbrydelse af behandlingen. De ligner dem, der blev observeret for ikke-selektive MAO-hæmmere.
Der er ingen specifik modgift. I tilfælde af overdosering skal du overvåge patienterne og gribe ind med "tilstrækkelig symptomatisk og understøttende behandling."
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: antiparkinsonmedicin, monoaminoxidasehæmmere -B
ATC -kode: N04BD02
Handlingsmekanisme:
Rasagilin har vist sig at være en potent og irreversibel selektiv MAO-B-hæmmer, hvilket kan føre til en stigning i ekstracellulære dopaminniveauer i striatum. Stigningen i dopaminniveauer og den deraf følgende stigning i dopaminerge aktivitet kan være ansvarlig for de gavnlige virkninger observeret med rasagilin i dopaminerge-baserede modeller for motorisk dysfunktion.
1-Aminoindan er den største aktive metabolit af rasagilin og er ikke en MAO-B-hæmmer.
Kliniske undersøgelser:
Effekten af rasagilin blev dokumenteret af resultaterne af tre undersøgelser: monoterapi i studie I og kombinationsbehandling i undersøgelser II og III.
Monoterapi:
I studie I blev 404 patienter randomiseret og behandlet i 26 uger med placebo (138 patienter) med rasagilin 1 mg / dag (134 patienter) eller rasagilin 2 mg / dag (132 patienter) uden anden aktiv komparator.
I denne undersøgelse var det primære effekt-endepunkt ændringen fra baseline i total score på Unified Parkinson's Disease Rating Scale (UPDRS, dele I-III). Forskellen mellem den gennemsnitlige ændring mellem baseline og den ved 26 uger / afsluttet behandling (LOCF, Last Observation Carried Forward) var statistisk signifikant (UPDRS, del I -III: for rasagilin 1 mg sammenlignet med placebo -4, 2, 95% Cl [-5,7 -2,7];
Foreningsterapi:
I studie II blev patienter randomiseret og behandlet i 18 uger med placebo (229 patienter) eller rasagilin 1 mg / dag (231 patienter) eller entacapon 200 mg (227 patienter), en catechol-O-methyltransferasehæmmer (COMT), taget sammen med den planlagte dosis levodopa (LD) / decarboxylase -hæmmer. I studie III blev patienter randomiseret og behandlet i 26 uger med placebo (159 patienter), rasagilin 0,5 mg / dag (164 patienter) eller rasagilin 1 mg / dag (149 patienter).
I begge undersøgelser var det vigtigste mål for effektiviteten ændringen mellem baseline og behandlingsperiode i det gennemsnitlige antal timer, der blev brugt i "off" -tilstand i løbet af dagen (baseret på tidsskrifter, der blev samlet hjemme i 24 timer og samlet i tre dage før hver vurderingsbesøg).
I studie II var den gennemsnitlige forskel i antallet af timer brugt i "off" -tilstand sammenlignet med placebo -0,78 timer, 95% CI [-1,18 -0,39 timer], p = 0,0001. Den gennemsnitlige samlede daglige reduktion i "off" -tid observeret i entacapongruppen (-0,80 timer, 95% CI [-1,20 -0,41], p
Sekundære effektforanstaltninger omfattede eksaminatorens overordnede vurdering af forbedringsgraden, aktiviteten i dagliglivets (ADL) subscale score i "off" tilstand og UPDRS score i "on" tilstand. Sammenlignet med placebo resulterede behandling med rasagilin i en statistisk signifikant fordel.
05.2 "Farmakokinetiske egenskaber
Absorption: Rasagilin absorberes hurtigt og når maksimal plasmakoncentration (Cmax) på cirka 0,5 timer. Den absolutte biotilgængelighed af enkeltdosis rasagilin er ca. 36%.
Fødevarer påvirker ikke rasagilines Tmax, selvom der er et fald i Cmax og eksponering (AUC) på henholdsvis cirka 60% og 20%, hvis lægemidlet indtages med et fedtfattigt måltid. AUC ændres ikke væsentligt, kan rasagilin tages enten på fuld mave eller på tom mave.
Fordeling: Den gennemsnitlige fordelingsvolumen for rasagilin efter enkeltdosis intravenøs injektion er 243 l. Plasmaproteinbinding efter enkelt oral dosis 14C -mærket rasagilin er cirka 60% -70%.
MetabolismeFør rasagilin udskilles, gennemgår den næsten fuldstændig biotransformation i leveren. De vigtigste metaboliske veje for rasagilin er to: N-dealkylering og / eller hydroxylering med dannelsen af: 1-Aminoindan, 3-hydroxy-N-propargyl-1 aminoindan og 3-hydroxy-1-aminoindan. Eksperimenterne in vitro indikere, at begge metaboliske veje for rasagilin er afhængige af cytochrom P450 -systemet; CYP1A2 er det vigtigste isoenzym, der er involveret i metabolismen af rasagilin. Det har også vist sig, at konjugering af rasagilin og dets metabolitter er en af de vigtigste eliminationsveje med dannelsen af glucuronider.
Udskillelse: Efter oral administration af 14C-mærket rasagilin blev lægemidlet primært elimineret via urin (62,6%) og afføring (21,8%) med en samlet genopretning på 84,4% af dosis over en periode på 38 dage. Mindre end 1% af rasagilin er udskilles i urinen som uændret lægemiddel.
Linearitet / ikke-linearitet: Rasagilins farmakokinetik er lineær over doser i området 0,5 til 2 mg. Dens sidste halveringstid er 0,6-2 timer.
Karakteristika hos patienter
Patienter med leverinsufficiens: Hos personer med let leverinsufficiens blev AUC og Cmax øget med henholdsvis 80% og 38%. Hos personer med moderat nedsat leverfunktion blev AUC og Cmax øget med henholdsvis 568% og 83% (se pkt. 4.4).
Patienter med nyreinsufficiens: Rasagilins farmakokinetik hos patienter med mild (CLcr 50-80 ml / min) til moderat (CLcr 30-49 ml / min) nyreinsufficiens var den samme som hos raske forsøgspersoner.
05.3 Prækliniske sikkerhedsdata
Ikke-kliniske data afslører ingen særlig fare for mennesker baseret på konventionelle undersøgelser af sikkerhed, toksicitet ved gentagne doser og reproduktionstoksicitet.
Rasagilin har intet genotoksisk potentiale in vivo og i mange systemer in vitro ved hjælp af bakterier og / eller hepatocytter. I nærvær af aktive metabolitter fremkalder rasagilin en stigning i kromosomale aberrationer ved overdrevne cytotoksiske koncentrationer, som ikke anvendes under betingelserne for klinisk brug.
Rasagilin var ikke kræftfremkaldende hos rotter ved en systemisk eksponering 84-339 gange den forventede humane plasmakoncentration ved 1 mg / dag dosis.
Hos mus blev der observeret en stigning i forekomsten af kombineret bronchiolært / alveolært adenom og / eller carcinom med en systemisk eksponering 144-213 gange større end den forventede humane plasmakoncentration ved 1 mg / dag dosis.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Mannitol
Majsstivelse
Pregelatiniseret majsstivelse
Vandfri kolloid silica
Stearinsyre
Talc
06.2 Uforenelighed
Ikke relevant.
06.3 Gyldighedsperiode
Blister: 3 år
Flasker: 3 år
06.4 Særlige opbevaringsforhold
Må ikke opbevares over 25 ° C.
06.5 Den umiddelbare emballages art og emballagens indhold
Blisterpakninger: Aluminium / aluminiumblister, pakninger med 7, 10, 28, 30, 100 eller 112 tabletter.
Flasker: Hvid polyethylenflaske med høj densitet med eller uden børnesikret sikkerhedsdæksel indeholdende 30 tabletter.
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Teva Pharma GmbH
Graf-Arco-Str. 3
89079 Ulm
Tyskland
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
EU / 1/04/304 / 001-007
036983017
036983029
036983031
036983043
036983056
036983068
036983070
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
Dato for første godkendelse: 21. februar 2005
Dato for sidste fornyelse: 21. september 2009
10.0 DATO FOR REVISION AF TEKSTEN
D.CCE november 2013












.jpg)