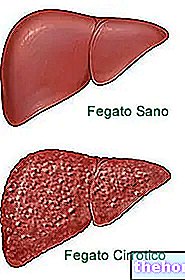
Som det er kendt, transporterer røde blodlegemer (RBC'er) ilt til vævene og i udholdenhedssport, såsom cykling, langrend osv., Er iltbehovet meget højt.
I nogen tid er der derfor blevet undersøgt strategier for at øge produktionen af RBC'er for at forbedre sportens præstationer.
Den seneste strategi er baseret på erythropoietins (EPO) rolle i stimulering af knoglemarven til at producere røde blodlegemer (RBC'er).
Rekombinant human EPO (rHuEPO) og beslægtede stoffer (f.eks. Darbepoietin) anvendes som doping.
EPO har en relativt kort levetid i kroppen, mens dens stimulerende effekt kan vare op til to uger
d "ilt1985 Lin og Jacobs klonede erythropoietingenet og udviklede en transficeret cellelinie (CHO -celler), der var i stand til at producere rekombinant humant erythropoietin
Erythropoiesis og hypoxi
Erythropoiesis (produktion af nye røde blodlegemer) styres af et meget følsomt feedback -system, hvor en sensor på nyreniveau registrerer ændringer i iltforsyningen.
Mekanismen er baseret på tilstedeværelsen af en heterodimer transkriptionsfaktor (Hypoxia-inducerbar faktor, HIF-1) (HIF-1α og HIF-1β), som øger ekspressionen af erythropoietingenet.
HIF-1α er ustabil i nærvær af ilt og nedbrydes hurtigt af prolyl-hydroxylase med bidraget fra von Hippel-Lindau-proteinet.
Under hypoxi er propyl-hydroxylase inaktiv, og derfor akkumuleres HIF-1α, der aktiverer ekspressionen af erythropoietin, som stimulerer den hurtige ekspansion af erythroid progenitorer.
(men de første 27 deles under sekretion).
Det produceres hovedsageligt af peritubulære interstitielle celler i nyrerne, under kontrol af et gen på kromosom 7.
Efter sekretion binder erythropoietin i det hæmatopoietiske væv (knoglemarv) sig til en receptor (EPO-R) placeret på overfladen af erythroid progenitorerne og internaliseres.
I nærvær af anæmi eller hypoxæmi øges syntesen af EPO hurtigt mere end 100 gange og øger følgelig overlevelse, spredning og modning af knoglemarvs stamceller også gennem inhibering af apoptose (programmeret celledød).
Normale niveauer af EPO i blodet er ca. 2-25 mU / ml, men kan stige 100-1000 gange som reaktion på hypoxi.
Iltsensormekanismen fører til afbrydelse af EPO -produktionen, når antallet af røde blodlegemer og / eller iltforsyning til vævene vender tilbage til ligevægt
Feedbackmekanismen sikrer tilstrækkelig produktion af RBC'er for at forhindre anæmi og vævshypoxi, men ikke for høj til at føre til polycytæmi med overdreven blodviskositet og deraf følgende kardiovaskulære risici.
Overproduktionen af EPO, der fører til polycytæmi (sekundært at skelne fra polycythemia vera eller primær: myeloproliferativ lidelse, hvor EPO-uafhængige kloner af stamceller formerer sig med en stigning i både RBC'er og granulocytter og blodplader) kan skyldes hjerte- eller luftvejssygdomme, fra højde , fra forhindringer af blodgennemstrømning til EPO-produktionsstedet, fra EPO-producerende tumorer.
Ved sekundær polycytæmi er EPO -niveauer generelt høje, men de kan også være normale på grund af en stigning i dens omsætning.
Det er kendt, at de eksisterende genetiske forskelle mellem atleter kan være et element på grundlag af de forskellige præstationskapaciteter.
Blandt de mulige genetiske forskelle kan nogle vedrøre erythropoiesis generelt og specifikt erythropoietin.
Et eksempel er historien om den finske langrendsløber Eero Mäntyranta, dobbeltguldmedaljevinder ved OL i 1964 i Innsbruck.
Han blev født med en Epo-genmutation (udtrykt på receptorniveau), der øgede hans iltbærende kapacitet med røde blodlegemer med 25-50%.
Denne parafysiologiske tilstand kunne reproduceres ved genmanipulation.
Antallet af EPO-receptorer varierer i de forskellige celler i erythrocytlinjen.Maksimumet forekommer i CFU-E, antallet falder, efterhånden som differentieringen og modningen af erytrocytcellerne skrider frem. EPO.
EPO -receptorer er også blevet identificeret på myocytter, endotelceller, CNS, æggestokke og testikler.
EPO menes derfor at spille en fysiologisk rolle i hjerte- og hjerneudvikling.
EPO beskytter hjerte- og nervevæv mod betændelse og iskæmisk skade: både gennem direkte stimulering af nerve- og hjerteceller og indirekte ved at mobilisere endotelcellestamceller og dermed fremme neo-vaskularisering.
) med hensyn til den fysiologiske EPO, som dog afspejles i molekylets kemiske og fysiske adfærd, for eksempel er der forskelle i den elektriske ladning.Til ergogene formål bruges rHuEPO sammen med injicerbare administrationer hver 2-3 dage i 3-4 uger i forbindelse med jernpræparater. Faktisk bliver det ved betingelser med erythropoietin -stimulering nødvendigt at få syntetiseret hæmoglobin hos atleter med en meget højere hastighed end normalt, og dette kræver en tilstrækkelig tilførsel af jern for at opretholde erytropoietisk effektivitet. Halveringstid i.v. 8,5 timer.
Når vedligeholdelsesfasen er nået, kan indtagelsen finde sted ved lavere doser, som er vanskeligere at identificere ved dopingkontrol.
Darbepoietin
Mere stabil end EPO, med længere halveringstid (i.v. 25,3 timer) og større effektivitet; det er lettere at identificere på grund af dets strukturelle egenskaber, der adskiller sig fra det endogene humane produkt og på grund af dets lavere clearance
Terapeutisk anvendelse af erythropoietin (epoetin; Eprex®, Globuren®, Neorecormon®; darbepoetin: Aranesp®, Nespo®)
- Anæmi ved kronisk nyresvigt
- Zidovudin-anæmi (anti-HIV)
- "Ildfast" anæmi
- Anæmi efter kemoterapi mod kræft
- Patologiske mangler ved EPO
- Myelom
- Myelodysplastiske syndromer.
Hurtig og kontinuerlig udvikling af forskning om erythropoietin:
Produkter, der efterligner EPO's aktivitet
Små peptider eller ikke-peptidforbindelser, der kan binde, aktivere dem, til EPO-receptorerne (Science 1996; 273: 458. Proc Natl Acad Sci USA 1999; 96: 12156)
For nylig har f.eks. In vitro-forsøg vist, at silkeormhæmolymfe har hæmmet apoptose af EPO-producerende celler ved at øge EPO-produktionen 5 gange (Biotechnol Bioeng 2005; 91: 793)
(hæmatokrit udtrykt i procent), hæmoglobinniveauer, retikulocyttalVed cykling fører hæmatokritmålinger over 50% til suspension. Værdier over 50% mistænkes af IOC
Det Internationale Skiforbund har indført en hæmoglobingrænse på 18,5 g / dL hos mænd og 16,5 g / dL hos kvinder, hvis atleten ikke kan deltage for at bevare sit helbred.
Det skal understreges, at hæmatokrit- og hæmoglobinværdier kan variere fra atlet til atlet og som reaktion på den samme øvelse. Det ideelle er at have den hæmatologiske profil for hver atlet over tid:
undersøgelserne for at identificere brugen af EPO har strakt sig til forskellige sportsgrene og naturligvis til OL
Marco Pantani blev diskvalificeret fra Tour of Italy for en hæmatokritværdi på 52%
I 2003 testede den kenyanske mellemdistanceløber Bernard Lagat (næstbedste tid nogensinde på 1500 m) positiv (forskning af rHuEPO i urinen) for EPO-indtag inden VM i atletik i Paris (hvor han ikke kunne deltage) efterfølgende mod- analyser rensede ham dog. Denne sag viste behovet for at søge mere pålidelige tests.
En ny direkte isoelektrisk metode er for nylig blevet udviklet (med gode resultater) for at skelne eksogent fra endogent EPO i urinprøver, udviklet i det franske laboratorium i Chatenay-Malabry (Nature 2000; 405: 635; Anal Biochem 2002; 311: 119; Clin Chem 2003; 49: 901). Det var muligt at identificere eksogent EPO selv efter 3 dage fra indtagelsen
(Incidens 1-30%). Mekanismen er ikke fuldt ud forstået, "EPO har en" vasokonstriktiv virkning, og kronisk eksponering forårsager resistens over for vasodilaterende virkning af nitrogenoxid. Endelig fremmer EPO væksten af glatte muskelceller i karene med vaskulær ombygning og hypertrofi, som kan bidrage til opretholdelse af hypertension [Am J Kidney Dis 1999; 33: 821-8]).
Knoglesmerter (ikke-alvorlig, forbigående, høj forekomst = 40%).
Kramper (på grund af hurtig stigning i blodviskositet og hypoksisk vasodilatationstab med deraf følgende stigning i vaskulær resistens).
Hovedpine.
Tromboemboliske fænomener (PE, MI, slagtilfælde), alle relateret til blodhyperviskositet.
Anæmi efter behandling på grund af nedsat endogen EPO-produktion.
Ren rød celle aplasi (anti-EPO antistof dannelse?).
Myeloproliferative lidelser (dyreforsøg, langtidsbehandlinger?).
Skade fra erythropoietin som doping
Dataene om de ovenfor anførte bivirkninger af erythropoietin stammer næsten udelukkende fra terapeutiske behandlinger hos patienter med underliggende sygdomme
Der er ingen undersøgelser af skaden af erythropoietin brugt som doping på raske atleter
En undersøgelse af atleter, der fik EPO i 6 uger, fandt en signifikant stigning i systolisk blodtryk som reaktion på sub-maksimal træning.
Antallet af dødsfald blandt belgiske og hollandske cyklister mellem 1987 og 1990 har været relateret til brugen af EPO (Gambrell og Lombardo. Lægemidler og doping: bloddoping og rekombinant humant erythropoietin. I: Mellion, M.B. (red.): Sportsmedicinske hemmeligheder. Philadelphia: Hanley & Belfus, 1994, s. 130-3)
Det er ikke forkert at tro, at de bivirkninger, der ses hos patienter, også kan forekomme hos raske atleter, omend med en lavere forekomst.