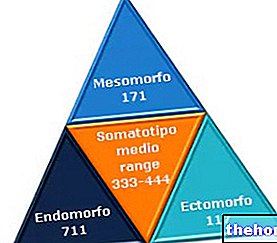
Aminosyrer og proteiner er mellemprodukterne fra passage fra mineralverden til levende stof.
Som deres navn angiver, er aminosyrer bifunktionelle organiske stoffer: bestående af aminofunktionen (-NH2) og carboxylfunktionen (-COOH); de kan være α, β, γ osv., afhængigt af den position, som aminogruppen indtager med hensyn til carboxygruppen:



De biologisk vigtige aminosyrer er alle a-aminosyrer.
Proteinstrukturerne består af tyve aminosyrer.
Som det ses af de generiske strukturer vist ovenfor, har aminosyrer alle en fælles del og en anden del, der kendetegner dem (repræsenteret generisk med R).
Af de tyve aminosyrer er nitten optisk aktive (de afbøjer planet for polariseret lys).
De fleste aminosyrer har kun en aminogruppe og en carboxyl, derfor kaldes de neutrale aminosyrer; dem der har et ekstra carboxyl kaldes sure aminosyrer mens dem med en ekstra aminogruppe er basiske aminosyrer.
Aminosyrer er krystallinske faste stoffer og har god vandopløselighed.
Manglen på nogle aminosyrer i kosten forårsager alvorlige ændringer i udviklingen; faktisk er den menneskelige organisme ikke i stand til at syntetisere nogle aminosyrer, som netop kaldes essentielle (de skal indføres med kosten), mens den kun kan producere nogle aminosyrer (de ikke-essentielle).
En af sygdommene på grund af manglen på essentielle aminosyrer er den, der er kendt under navnet kwashiorkor (et ord, der stammer fra en afrikansk dialekt, som oversat betyder "første og anden"); denne sygdom rammer den førstefødte, men efter fødslen af det andet barn, fordi det første barn mangler modermælk, som indeholder den korrekte tilførsel af proteiner. Denne sygdom er derfor udbredt blandt underernærede populationer og involverer diarré, mangel på appetit, hvilket fører til en gradvis svækkelse af organismen.
Som allerede nævnt har naturlige aminosyrer, med undtagelse af glycin (det er en a-aminosyre med et hydrogen i stedet for R-gruppen og er den mindste af de tyve), optisk aktivitet på grund af tilstedeværelsen af mindst en asymmetrisk kulstof. I naturlige aminosyrer tilhører den absolutte konfiguration af det asymmetriske carbon, som kun amino- og carboxygrupperne er knyttet til L -serien;
D-aminosyrer bliver aldrig en del af strukturen af et protein.
Vi husker, at:
DNA ---- transkription → m-RNA ---- oversættelse → protein
Transkriptionen er i stand til at kode som L-aminosyrer; D-aminosyrer kan være indeholdt i ikke-proteinstrukturer (f.eks. I foring af bakterier: i bakterier er der ingen "genetisk information for at have D-aminosyrer til en beskyttende rolle, men der er" genetisk information om enzymer som omhandler den bakterielle foringsvæg).
Lad os gå tilbage til aminosyrer: R -gruppens forskellige struktur definerer de enkelte karakteristika for hver aminosyre og yder et specifikt bidrag til egenskaberne ved proteiner.
Det blev derfor antaget at opdele aminosyrer baseret på arten af R -gruppen:
Polære men uladede aminosyrer:
Glycin (R = H-)
Serin (R = HO-CH2-)
Threoninvigtig
Threonin har to symmetricentre: kun 2S, 3R threonin findes i naturen.
Threonin er en essentiel aminosyre (ikke at forveksle med uundværlig: alle aminosyrer er essentielle), så den skal tages sammen med kosten, dvs. ved at spise mad, der indeholder den, fordi den genetiske arv, som allerede nævnt, ikke er til stede i menneskers celler. i stand til at producere denne aminosyre (denne arv findes i mange planter og bedre).
Hydroxylgruppen af serin og threonin kan esterificeres med en phosphorylgruppe (opnåelse af phosphoserin og phosphotreonin), denne proces kaldes fosforylering; fosforylering bruges i naturen til translation af signaler mellem indersiden og ydersiden af cellen.
Cystein (R = HS-CH2-)
Sulfhydryl af cystein er lettere protonerbar end hydroxyl af serin: svovl og ilt er begge af den sjette gruppe, men svovl er lettere oxiderbart, fordi det har større dimensioner.
Tyrosin [R = HO- (C6H4) -CH2-]
N.B.
(C6H4) = di-substitueret benzenring
Som med serin og threonin kan hydroxyl esterificeres (phosphoryleres).Asparagin (R = NH2-CO-CH2-)
Glutamin (R = NH2-CO-CH2-CH2-)
Ikke-polære aminosyrer
have hydrofobe sidegrupper; inden for denne klasse skelner vi:
Alifatisk:
Alanin (R = CH3-)
Valine (R = (CH3) 2-CH-) essentiel
Leucin (R = (CH3) 2-CH-CH2-) essentiel
Isoleucin (R =
) vigtig
Methionin (R = CH3-S-CH2-CH2-) afgørende
Cellemembraner består af et lipid -dobbeltlag med proteiner forankret takket være deres hydrofobe karakter, derfor indeholder de alanin, valin, isoleucin og leucin. Methionin, på den anden side, er en aminosyre, der næsten altid er til stede i små mængder (ca. 1%).
Proline
Aromatisk:
Phenylalanin (R = Ph-CH2-) Ph = phenyl: essentiel monosubstitueret benzen
Tryptophan (R =
vigtig
Disse to aminosyrer, som er aromatiske, absorberer nær ultraviolet stråling (ca. 300 nm); derfor er det muligt at udnytte teknikken til UV -spektrofotometri til at bestemme koncentrationen af et kendt protein, der indeholder disse aminosyrer.
Ladede aminosyrer
Til gengæld er de opdelt i:
Sure aminosyrer (med polære rester med negativ ladning ved pH 7) er sådanne, fordi de er i stand til at give en positiv H + ladning:
Aspartinsyre
Glutaminsyre (R =
)
Disse aminosyrer stammer fra henholdsvis asparagin og glutamin; alle fire findes i naturen, og det betyder, at c "er en specifik information for hver af dem, det vil sige c" er en basistriplet i DNA'et, der koder for hver af dem.
Grundlæggende aminosyrer (med polære rester med en positiv ladning ved pH 7) er sådanne, fordi de er i stand til at acceptere en positiv H + ladning:
Lysin (R =
) vigtig
Arginin (R =
)
Histidin (R =
)
Der er proteiner, hvor der er derivater af aminosyrer i sidekæderne: for eksempel kan der være en phosphoserin til stede (der er ingen genetisk information, der koder for phosphoserin, kun den for serin); phosphoserin er en modifikation post-translationel: efter proteinsyntese er sket
DNA ---- transkription → m-RNA ---- oversættelse → protein
sådanne posttranslationelle ændringer kan forekomme på proteinets sidekæder.
Se også: Proteiner, et kig på kemi












.jpg)







.jpg)