Aktive ingredienser: Mepivacaine (Mepivacaine hydrochlorid)
CARBOCAINE 10 mg / ml injektionsvæske, opløsning
CARBOCAINE 20 mg / ml injektionsvæske, opløsning
Indlægsseddel: AIFA (Italian Medicines Agency). Indhold offentliggjort i januar 2016. De foreliggende oplysninger er muligvis ikke opdaterede.
For at få adgang til den mest opdaterede version er det tilrådeligt at få adgang til webstedet AIFA (Italian Medicines Agency). Ansvarsfraskrivelse og nyttige oplysninger.
01.0 LÆGEMIDLETS NAVN
CARBOCAINE
02.0 KVALITATIV OG KVANTITATIV SAMMENSÆTNING
CARBOCAINE 10 mg / ml injektionsvæske, opløsning
1 ml indeholder:
aktiv ingrediens: mepivacainhydrochlorid 10 mg
CARBOCAINE 20 mg / ml injektionsvæske, opløsning
1 ml indeholder:
aktiv ingrediens: mepivacainhydrochlorid 20 mg
Den fulde liste over hjælpestoffer findes i afsnit 6.1.
03.0 LÆGEMIDDELFORM
Injicerbar løsning.
04.0 KLINISKE OPLYSNINGER
04.1 Terapeutiske indikationer
Carbocain er angivet i alle interventioner vedrørende:
- generel kirurgi (mindre operation)
- Obstetrik og gynækologi
- urologi
- oftalmologi (retro-bulbar blok osv.)
- dermatologi (fjernelse af vorter, cyster, dermoider osv.)
- otolaryngologi (tonsillektomi, næseplastik, indgreb på mellemøret osv.)
- ortopædi (reduktion af brud og dislokationer osv.)
- almen medicin (ulykker, neuralgi osv.)
- sportsmedicin (muskelstammer, meniskopatier osv.).
04.2 Dosering og indgivelsesmåde
Den maksimale dosis til en rask voksen (ikke forbehandlet med beroligende midler) ved enkelt administration eller i flere gentagne administrationer på mindre end 90 minutter er 7 mg / kg uden nogensinde at overstige 550 mg. Den samlede dosis på 24 timer må aldrig overstige 1000 mg ; i pædiatri ikke overstige 5-6 mg / kg.
Når langvarig blokade anvendes, f.eks. Ved gentagen administration, bør risikoen for at nå toksiske plasmakoncentrationer og induktion af lokale neurale læsioner overvejes.
For at undgå intravaskulær administration er det nødvendigt at aspirere gentagne gange før og under administrationen af hoveddosis, som skal injiceres langsomt eller i stigende doser, nøje observere patientens vitale funktioner og opretholde verbal kontakt.
Utilsigtet intravaskulær administration kan genkendes ved en midlertidig stigning i puls, mens utilsigtet intratekal administration kan genkendes ved tegn på rygmarvsblok.
Hvis der opstår tegn på toksicitet, skal injektionen straks stoppes.
Anbefalede doser:
Kirurgi
Peridural og caudal blok: op til 400 mg nået med 15-30 ml af en 1% opløsning eller med 10-20 ml af en 2% opløsning.
Paravertebral blok: op til 400 mg med 1% opløsning til stellatganglionblokken og for vegetative blokke, ved 1-2% for den paravertebrale blok af de somatiske nerver.
Perifer cervikal, brachial, intercostal, paracervikal, pubendal og nerveender nerveblok: op til 400 mg opnåelig med 5-20 ml 1% eller 2% opløsning afhængigt af blokens område og omfang.
Infiltration: op til 400 mg i forhold til interventionsområdet, kan opnås med variable mængder op til 40 ml af en 0,5-1% opløsning.
Obstetrik
Paracervikal blok: op til 200 mg inden for en 90 minutters periode med 10 ml 1% opløsning til hver side.
Babyer
På grund af nedsat levermetabolisme bør mepivacain ikke anvendes til nyfødte.
Særlige populationer
Nedsat leverfunktion
Ingen dosisreduktion er nødvendig under kirurgisk anæstesi hos patienter med nedsat leverfunktion. Når langvarige blokke bruges, f.eks. Ved administration af gentagne doser af mepivacain, bør gentagne doser af mepivacain reduceres med 50% hos patienter med "Child-Pugh" grad C leversygdom, og en total dosis på 750 mg 24-timers mepivacain bør ikke overskrides (se pkt. 4.4).
Nedsat nyrefunktion
Ingen dosisreduktion er nødvendig under kirurgisk anæstesi op til 24 timer hos patienter med nedsat nyrefunktion (se pkt. 4.4 og 5.2).
Advarsel: hætteglassene indeholder ikke paraseptiske hjælpestoffer, der skal bruges til en enkelt administration. Eventuelle beholdninger vil blive kasseret.
04.3 Kontraindikationer
Overfølsomhed over for det aktive stof, over for andre lokalbedøvelsesmidler af amidtypen, over for andre nært beslægtede stoffer fra et kemisk synspunkt eller over for et eller flere af hjælpestofferne.
Kendt eller mistænkt graviditet.
04.4 Særlige advarsler og passende forholdsregler ved brug
Teknikkerne til lokal eller regional bedøvelse, med undtagelse af dem, der er ekstremt enkle, skal altid udføres i tilstrækkeligt udstyrede områder og af kvalificeret personale. Det er nødvendigt at have det nødvendige udstyr og lægemidler til rådighed øjeblikkeligt til overvågning af nødoplivning.
Hos patienter, der gennemgår større blokering eller får høje doser af lægemidlet, skal der indsættes et intravenøst kateter, inden lokalbedøvelsen administreres. Diagnose og behandling af uønskede virkninger, systemisk toksicitet eller andre komplikationer (4.9 "Overdosering").
Bedøvelsesopløsningen skal injiceres omhyggeligt i små doser cirka 10 sekunder efter en forebyggende aspiration. Især når meget vaskulariserede områder skal infiltreres, er det tilrådeligt at lade cirka to minutter gå, før du går videre til den aktuelle lokalregionale blok.
Produktet bør anvendes med absolut forsigtighed til personer, der behandles med MAO -hæmmere eller tricykliske antidepressiva.
Før brug skal lægen konstatere den fysiske tilstand hos de emner, der skal behandles.
En overdosis af bedøvelsesmidler bør undgås og aldrig gives to maksimale doser af sidstnævnte uden et minimumsinterval på 24 timer.
Det er imidlertid nødvendigt at bruge de laveste doser og koncentrationer, der kan tillade at opnå den ønskede effekt.
Nogle lokalbedøvelsesteknikker kan være forbundet med alvorlige bivirkninger, uanset hvilken lokalbedøvelse der bruges, såsom:
- Centralnervøs blok: kan forårsage kardiovaskulær depression især i nærvær af hypovolæmi. Epidural anæstesi bør anvendes med forsigtighed til patienter med nedsat kardiovaskulær funktion;
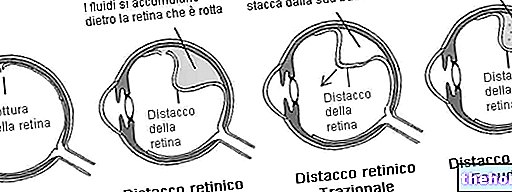
- Retrobulbar -injektioner: de kan i meget sjældne tilfælde nå hjernens subaraknoidale rum og forårsage midlertidig blindhed, kardiovaskulær kollaps, apnø, kramper osv. Sådanne reaktioner skal diagnosticeres og behandles med det samme;
- Retro og peribulbar injektioner af lokalbedøvelse: bærer en lav risiko for vedvarende muskeldysfunktion i øjet. Primære årsager omfatter traumer og / eller lokale toksiske virkninger på muskler og / eller nerver. Alvorligheden af disse vævsreaktioner er relateret til omfanget af traumet, koncentrationen af lokalbedøvelse og varigheden af vævseksponering for lokalbedøvelsen. Som med alle lokale bedøvelsesmidler er det derfor nødvendigt at bruge de laveste doser og koncentrationer. kan tillade at opnå den ønskede effekt. Vasokonstriktorer kan forværre vævsreaktioner og bør kun bruges, hvis det er angivet.
- Utilsigtede intra-arterielle injektioner i kraniet og livmoderhalsen kan forårsage alvorlige symptomer, selv ved lave doser.
- Carbocain anbefales ikke ved fødsel og fødsel, da placentapassage af mepivacain er relativt høj, mens neonatal metabolisme er langsom. Dette øger den potentielle toksicitet for fosteret og det nyfødte.
- Kontinuerlig intraartikulær infusion er ikke en godkendt indikation for Carbocaine.
Imidlertid er post-marketing tilfælde af kondrolyse hos patienter, der modtager kontinuerlig postoperativ intraartikulær infusion af lokalbedøvelsesmidler, udelukkende blevet registreret i Nordamerika. Størstedelen af de rapporterede chondrolysetilfælde involverede skulderleddet. Der er ikke fundet årsagssammenhæng.
For at reducere risikoen for farlige bivirkninger skal der lægges særlig vægt på:
• patienter med fremskreden leversygdom eller svært nedsat nyrefunktion.
Hos patienter med fremskreden Child-Pugh grad C leversygdom tyder data fra lidokain på, at clearance kan reduceres med cirka 50% (se pkt.4.2).
Et klinisk relevant fald i mepivacain -clearance forventes kun hos patienter med svært nedsat nyrefunktion (CL (cr) hæmodialyse.
Reduktionen i clearance fører ikke til toksicitet forårsaget af høje plasmakoncentrationer efter administration af enkeltdoser under kirurgisk anæstesi.Ved kronisk nyreinsufficiens er clearance af metabolitten PPX udskilt af nyrerne forringet, og efter gentagen administration kan det være muligt . kontrollere akkumulering (se afsnit 4.2);
• patienter med delvis eller fuldstændig hjerteblok, da lokalbedøvelsesmidler kan undertrykke hjerteledning;
• ældre patienter eller patienter under usikre generelle tilstande;
• Patienter, der behandles med klasse III antiarytmiske lægemidler (f.eks. Amiodaron), bør overvåges nøje, og EKG -overvågning bør overvejes, da virkningerne på hjertets niveau kan være additive;
• Carbocain injektionsvæske, opløsning er sandsynligvis porfyrinogen og bør kun ordineres til patienter med akut porfyri, når sikrere alternativer ikke er tilgængelige. Der skal træffes passende forholdsregler hos sårbare patienter.
N.B. Patienter under dårlige generelle tilstande på grund af alder eller andre kompromitterende faktorer, såsom delvis eller fuldstændig blokering af hjerteledning, fremskreden leversygdom eller alvorligt nedsat nyrefunktion, kræver særlig opmærksomhed på trods af, at regionalbedøvelse ofte er den anæstetiske teknik til valg hos sådanne patienter.
Epidural anæstesi kan forårsage hypotension og bradykardi.Risikoen kan reduceres ved på forhånd at fylde cirkulationen med krystalloid eller kolloid opløsning.
Hypotension bør straks behandles med administration, eventuelt gentaget, af et sympatomimetikum som efedrin 5-10 mg intravenøst.
04.5 Interaktioner med andre lægemidler og andre former for interaktion
Mepivacain bør anvendes med forsigtighed til patienter, der behandles med andre lokalbedøvelsesmidler eller stoffer, der strukturelt er relateret til lokalbedøvelsesmidler af amidtypen, f.eks. Visse antiarytmika såsom mexiletin, da de systemiske toksiske virkninger er additive. Forsigtighed tilrådes hos patienter behandlet med klasse III antiarytmika (f.eks. Amiodaron) på trods af fravær af specifikke interaktionsundersøgelser af lægemiddelklasse (se pkt. 4.4).
Der bør udvises ekstrem forsigtighed hos personer, der behandles med MAO -hæmmere eller tricykliske antidepressiva (se pkt. 4.4).
04.6 Graviditet og amning
Graviditet
Produktet er kontraindiceret i tilfælde af bekræftet eller formodet graviditet.
Mepivacain anbefales ikke under arbejde og fødsel (se 4.4).
Fodringstid
Ligesom andre lokalbedøvelsesmidler kan mepivacain udskilles i modermælk.
04.7 Virkninger på evnen til at føre motorkøretøj og betjene maskiner
Lokalbedøvelsesmidler kan udover den direkte bedøvelseseffekt have en meget mild effekt på mental funktion og koordination, selv i mangel af tydelig centralnervesystemtoksicitet, og kan midlertidigt påvirke bevægelse og grad af opmærksomhed negativt.
04.8 Bivirkninger
Generel
Bivirkningsprofilen for Carbocaine er sammenlignelig med den for andre lokalbedøvelsesmidler af amidtypen. Uønskede lægemiddelreaktioner er vanskelige at skelne fra fysiologiske virkninger som følge af nerveføringsblok (såsom nedsat blodtryk, bradykardi) og fra hændelser forårsaget af direkte indsprøjtning (f.eks. Nervefibertraume) eller indirekte (f.eks. Epidural abscess)).
Toksiske reaktioner og allergiske reaktioner på både bedøvelsesmidlet og vasokonstriktoren kan forekomme. Blandt de førstnævnte rapporteres fænomener om centralnervestimulering med spænding, rysten, desorientering, svimmelhed, mydriasis, øget stofskifte og kropstemperatur og, ved meget høje doser, trismus og kramper; hvis medulla oblongata er involveret, er der en deling af de kardiovaskulære, respiratoriske og emetiske centre med svedtendens, arytmier, hypertension, takypnø, bronkodilatation, kvalme og opkastning. Perifere effekter kan påvirke det kardiovaskulære system med bradykardi og vasodilatation. Allergiske reaktioner forekommer hovedsageligt hos overfølsomme forsøgspersoner, men mange tilfælde er rapporteret med fravær af individuel overfølsomhed over for anamnesen. Lokale manifestationer omfatter forskellige hududslæt, urticaria, kløe; dem af generel art bronkospasme, larynxødem op til kardiorespiratorisk kollaps fra anafylaktisk shock .
Tabel over bivirkninger
* Hyppigere bivirkninger efter epidural blokering
Akut systemisk toksicitet
Systemiske toksiske reaktioner involverer primært centralnervesystemet (CNS) og det kardiovaskulære system (CVS). Disse reaktioner er forårsaget af en "høj blodkoncentration af lokalbedøvelse, der kan udløses af" utilsigtet intravaskulær injektion, overdosis eller usædvanlig hurtig absorption fra et "stærkt vaskulariseret område (se pkt. 4.4). CNS -reaktioner er ens. For alle lokalbedøvelser af amidtypen, mens hjertereaktioner er mere afhængige af lægemidlet, både kvantitativt og kvalitativt.
Centralnervesystemets toksicitet forekommer ofte gradvist med symptomer og tegn på stigende sværhedsgrad. De første symptomer er sædvanligvis svimmelhed, paræstesi i det omkringliggende område, følelsesløshed i tungen, tinnitus og synsforstyrrelser. Dysartri, rykninger og muskelrysten er mere alvorlige manifestationer og går forud for begyndelsen af generaliserede kramper. Disse tegn må ikke forveksles med eretisk adfærd.
Bevidstløshed og grand mal -anfald kan følge, hvilket kan vare fra få sekunder til flere minutter. Efter kramper forekommer hypoxi og hyperkapni hurtigt på grund af øget muskelaktivitet, forstyrrelse af normal vejrtrækning og mangel på luftvejspatentitet. I alvorlige tilfælde kan der opstå apnø. Acidose, hyperkalæmi, hypocalcæmi og hypoxi øger og forlænger de toksiske virkninger af lokalbedøvelse.
Patientens tilbagevenden til den oprindelige kliniske tilstand skyldes omfordeling af lokalbedøvelsen fra centralnervesystemet og efterfølgende metabolisme og udskillelse.Gendannelse kan være hurtig, hvis store mængder af lægemidlet ikke er blevet administreret.
I alvorlige tilfælde kan der opstå kardiovaskulære virkninger, som generelt er forudgået af tegn på toksicitet i centralnervesystemet.
Hos patienter, der gennemgår generel anæstesi eller dybt bedøvet, kan symptomer på prodromal centralnervesystem være fraværende. Som følge af høje systemiske koncentrationer af lokalbedøvelse kan hypotension, bradykardi, arytmier og endda hjertestop genereres. Hjertestop opstod i sjældne tilfælde uden forekomst af prodromale virkninger af centralnervesystemet.
Behandling af akut systemisk toksicitet
Administration af lokalbedøvelsen skal straks afbrydes, hvis der opstår tegn på akut systemisk toksicitet, og CNS -symptomer (kramper, CNS -depression) hurtigt skal behandles med passende ventilation / åndedrætshjælp og administration af antikolvulsiva.
Hvis der opstår cirkulationsstop, skal hjerte -lungeredning udføres med det samme. Det er afgørende at sikre optimal iltning, ventilation, understøtte cirkulation og behandle acidose.
I tilfælde af kardiovaskulær depression (hypotension, bradykardi) bør behandling med intravenøse væsker, vasokonstriktorer, kronotrope og eller inotropiske midler overvejes. Doserne til børn bør tage højde for alder og vægt.
Der bør administreres ilt, og om nødvendigt bør der foretages assisteret ventilation (maske og Ambu -pose eller tracheal intubation). Hvis anfald ikke spontant ophører efter 15-20 sekunder, bør et intravenøst antikonvulsivt middel administreres for at lette tilstrækkelig ventilation og iltning, f.eks. Intravenøst natriumthiopental 1-3 mg / kg. Alternativt kan diazepam 0,1 mg / kg legemsvægt administreres intravenøst, selvom dets virkning er langsom. Langvarige anfald kan forringe patientens ventilation og iltning.I dette tilfælde letter administrationen af et muskelafslappende middel (f.eks. Succinylcholin 1 mg / kg legemsvægt) ventilation og iltkontrol. I sådanne situationer bør endotracheal intubation overvejes med det samme.I tilfælde af tydelig kardiovaskulær depression (hypotension, bradykardi) kan et sympatomimetikum administreres, f.eks. Efedrin 5-10 mg. Administrationen kan gentages om nødvendigt efter 2 - 3 minutter.
Anvendelse af bulbar analeptika bør undgås for ikke at forværre situationen ved at øge forbruget af ilt Mulige kramper kan kontrolleres ved brug af diazepam i en dosis på 10-20 mg intravenøst; barbiturater, som kan fremhæve bulbar depression, anbefales ikke. Cirkulationen kan understøttes ved administration af corticoider i passende intravenøse doser; fortyndede opløsninger af alfa-beta-stimulanter med vasokonstriktiv virkning (mefentermin, metaraminol og andre) eller af atropinsulfat kan tilsættes.
Som en antacida kan natriumbicarbonat anvendes i en målrettet koncentration, intravenøst.
Indberetning af formodede bivirkninger
Rapportering af formodede bivirkninger, der opstår efter godkendelse af lægemidlet, er vigtig, da det giver mulighed for løbende overvågning af fordelene / risikobalancen ved lægemidlet. Sundhedspersonale anmodes om at rapportere alle formodede bivirkninger via det nationale rapporteringssystem. Websted www.agenziafarmaco .gov.it/it/responsabili.
04.9 Overdosering
Utilsigtet intravaskulær injektion af lokalbedøvelse kan forårsage umiddelbare systemiske toksiske reaktioner (fra sekunder til minutter). I tilfælde af overdosering opstår systemisk toksicitet senere (15-60 minutter efter injektion), og det skyldes en langsom stigning i blodkoncentrationer af lokale bedøvelsesmiddel (se pkt. 4.8).
05.0 FARMAKOLOGISKE EGENSKABER
05.1 Farmakodynamiske egenskaber
Farmakoterapeutisk gruppe: lokalbedøvelse - stivelse.
ATC -kode: N01BB03.
Mepivacainhydrochlorid (Carbocaine) er et hurtigtvirkende, middelvarigt, lokalbedøvelsesmiddel af amidtype. Dens styrke ligner den for lidokain. 2% -opløsningen, til epidural administration, har en virkningstid på 1,5-2 timer og op til 5 timer med perifere nerveblokke. 1% -opløsningen har en lavere effekt på motoriske nervefibre og en længere varighed af kortere handling. aktivitetens begyndelse og varigheden af den lokalbedøvende effekt af mepivacain afhænger af dosis og indgivelsessted.
Ligesom andre lokalbedøvelsesmidler blokerer mepivacain reversibelt nerveledning og forhindrer natriumioner i at komme ind gennem nervefibercellemembranen. Natriumkanalen i nervefibermembranen betragtes som den receptor, som lokalbedøvelsesmidler virker på.
Lokalbedøvelse kan have lignende virkninger på andre ophidsede membraner, såsom hjernen og myokardiet. Hvis store mængder af lægemidlet når den systemiske cirkulation, kan der forekomme symptomer og tegn på toksicitet, der hovedsageligt påvirker centralnervesystemet og det kardiovaskulære system.
Centralnervesystemets toksicitet forekommer ved lavere plasmakoncentrationer og går generelt forud for kardiovaskulære effekter (se pkt. 4.8). Direkte virkninger af lokalbedøvelse på myokardiet omfatter langsom ledning, negativ inotropisme op til cadiac arrest.
Indirekte kardiovaskulære virkninger (hypotension, bradykardi) kan forekomme efter epidural administration og er relateret til forlængelse af den samtidige sympatiske blok.
05.2 Farmakokinetiske egenskaber
Mepivacaine har en pKa på 7,8 og en olie / vand -fordelingskoefficient på 0,8.
Blodtoppen af carbocain afhænger af dosis, indgivelsesvej og vaskularitet på injektionsstedet. Distributionsvolumen ved steady state er 84 liter. Mepivacain er 78% bundet til plasmaproteiner og hovedsageligt til alfa-1-syre glycoprotein.
Clearance af mepivacain sker hovedsageligt via metaboliske processer i leveren og afhænger af leverens blodgennemstrømning og aktiviteten af metaboliserende enzymer.Den totale clearance af mepivacain er 0,8 liter / minut, den terminale halveringstid er 1,9 timer og leverekstraktionen forhold på 0,5.
Den terminale halveringstid hos det nyfødte er 3 gange højere end hos den voksne.
Mepivacain krydser placentabarrieren, og ligevægt mellem bundne og frie fraktioner opnås let.Graden af plasmaproteinbinding i fosteret er mindre end den, der ses hos moderen, hvilket resulterer i en lavere total plasmakoncentration i fosteret.
De tilgængelige oplysninger om udskillelse af mepivacain i modermælk er ikke tilstrækkelige til at bestemme risikoen for det ammende barn.
Kun 4% af mepivacain udskilles uændret i urinen. Lægemidlet nedbrydes ved hydroxylering og konjugering. Ca. 50% passerer ind i galden i form af metabolitter og udskilles i urinen, mens der kun findes en lille mængde i fæces. Hovedmetabolitterne er 3-OH-derivatet (16%), 4-OH-derivatet (12%) og det N-demethylerede derivat PPX (2,5%).
Nedsat nyrefunktion
Nedsat nyrefunktion har ringe eller ingen indflydelse på tolerancen af mepivacain ved kortvarig brug ved kirurgisk anæstesi.
Plasmakoncentrationer af mepivacain blev evalueret efter aksillær blokering med mepivacain uden adrenalin (600 mg til axillær blok og 50 mg til tilskud) hos 8 patienter med kronisk nyresvigt i slutstadiet.
De samlede plasmakoncentrationer udtrykt i mcg / ml som medianer og deres intervaller var 1,69 (1,23-7,78) efter 5 minutter, 5,61 (4,36-8,19) efter 30 minutter, 8,28 (3,83-11,21) efter 60 minutter, 7,93 (5,63-11,1) på 90 minutter og 6,49 (5,56-8,35) ved 150 minutter. Der blev ikke observeret toksicitetssymptomer. Til sammenligning havde patienter uden nyreinsufficiens, der modtog 600 mg mepivacain til aksillær plexusblok, gennemsnitlige samlede plasmakoncentrationer på 3,33 mcg / ml med en enkelt top på 5,21 mikrog / ml.
Patienter med kronisk nyresvigt har øgede koncentrationer af AAG og derfor øget plasmaproteinbinding og øgede samlede koncentrationer, mens koncentrationen af frit, farmakologisk aktivt mepicavain muligvis ikke øges til niveauer, hvor toksicitet forekommer.
Renal clearance af metabolitten PPX er signifikant korreleret med kreatininclearance. Manglende sammenhæng mellem total eksponering, udtrykt som AUC, med kreatininclearance indikerer, at total PPX-clearance omfatter ikke-renal eliminering ud over renal udskillelse. Nogle patienter med nedsat nyrefunktion kan vise øget eksponering for PPX på grund af reduceret ikke-renal clearance.På grund af den reducerede CNS-toksicitet af PPX sammenlignet med mepivacain anses de kliniske konsekvenser for ubetydelige ved kortvarig behandling.
05.3 Prækliniske sikkerhedsdata
I dyreforsøg er tegn og symptomer på toksicitet observeret efter høje doser mepivacain et resultat af virkningen på centralnervesystemet og det kardiovaskulære system. Ingen lægemiddelrelaterede bivirkninger blev observeret i reproduktionstoksicitetsundersøgelser. Det mutagene potentiale for mepivacain er ikke undersøgt. I betragtning af området og varigheden af terapeutisk brug af lægemidlet er der ikke udført carcinogenicitetsundersøgelser med mepivacain.
06.0 LÆGEMIDDELOPLYSNINGER
06.1 Hjælpestoffer
Carbocain 10 mg / ml injektionsvæske, opløsning i glasampul
natriumchlorid (tonisk middel),
vand til injektionsvæsker.
Carbocain 20 mg / ml injektionsvæske, opløsning i polyethylenampul
natriumchlorid (tonisk middel),
natriumhydroxid (pH -regulator),
saltsyre (pH -regulator),
vand til injektionsvæsker.
06.2 Uforenelighed
Opløseligheden af mepivacain over pH 6,5 er begrænset. Dette bør tages i betragtning, når alkaliske opløsninger, såsom carbonater tilsættes, hvilket kan udfælde opløsningen.
06.3 Gyldighedsperiode
Carbocain 10 mg / ml injektionsvæske, opløsning i glasampul
Gyldigheden af det intakte emballerede produkt i alle dets præsentationer er 3 år.
Carbocain 20 mg / ml injektionsvæske, opløsning i polyethylenampul
Gyldigheden af det intakte emballerede produkt i alle dets præsentationer er 2 år.
06.4 Særlige opbevaringsforhold
Carbocain 10 mg / ml og 20 mg / ml injektionsvæske, opløsning
Må ikke opbevares over 25 ° C.
Opløsningerne indeholder ikke konserveringsmidler og skal bruges umiddelbart efter åbning af hætteglasset. Eventuelt resterende lægemiddel skal kasseres.
Re-sterilisering af Carbocaine anbefales ikke.
06.5 Den umiddelbare emballages art og emballagens indhold
Ikke alle pakningsstørrelser er nødvendigvis markedsført.
Carbocain 10 mg / ml injektionsvæske, opløsning
5 og 10 ml hætteglas i neutralt glas
5 ampuller på 5 ml - 5 ampuller på 10 ml.
Carbocain 20 mg / ml injektionsvæske, opløsning
5 ml hætteglas af polyethylen
10 hætteglas med 5 ml.
06.6 Brugsanvisning og håndtering
Ingen særlige instruktioner.
07.0 INDEHAVER AF MARKEDSFØRINGSTILLADELSE
Aspen Pharma Trading Limited
3016 Citywest Business Campus
Dublin24
Irland
08.0 MARKEDSFØRINGSTILLADELSESNUMMER
Carbocain 10 mg / ml injektionsvæske, opløsning
- 5 hætteglas 5 ml - AIC 016691558
- 5 hætteglas 10 ml - AIC 016691560
Carbocain 20 mg / ml injektionsvæske, opløsning
- 10 hætteglas 5 ml - AIC 016691634
09.0 DATO FOR FØRSTE TILLADELSE ELLER FORNYELSE AF TILLADELSEN
13.04.1961 / juni 2005
Carbocain 10 mg / ml injektionsvæske, opløsning
- 5 hætteglas 5 ml: 30.10.2003 / juni 2005
- 5 ampuller 10 ml: 30.10.2003 / juni 2005
Carbocain 20 mg / ml injektionsvæske, opløsning
- 10 ampuller 5 ml: 26.07.2016
10.0 DATO FOR REVISION AF TEKSTEN
AIFA -afgørelse af 25. marts 2017

















.jpg)







