Forsøger at opsummere konceptet på en enklere måde, kan to lægemidler betragtes som bioækvivalente, når den terapeutiske ækvivalens mellem de to formuleringer, der indeholder den samme aktive ingrediens ved den samme koncentration, er blevet påvist.
og at beholderen og lukningssystemet ikke interagerer med medicinen. Indehavere af sterile lægemidler skal indsende sterilitetsdata, der viser produkternes mikrobiologiske integritet.Hjælpestoffer
I modsætning til hvad der sker for de aktive ingredienser, som skal være de samme med hensyn til type og dosering, kan hjælpestofferne være forskellige mellem ækvivalent lægemiddel og mærkevare.
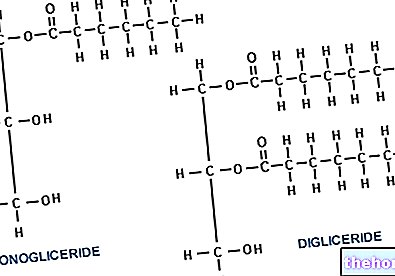
Hjælpestofferne er faktisk inaktive stoffer, ikke farmakologisk aktive, hvis anvendelse er nødvendig for at gøre det aktive princip administrerbart og for at tillade stabilitet og holdbarhed for den farmaceutiske formulering.
På den anden side kan brugen af visse hjælpestoffer have konsekvenser for visse kategorier af patienter (tænk f.eks. På allergiske fænomener, intolerancer, tilstedeværelsen af stoffer, der kan forstyrre eksisterende patologier osv.). Lignende aspekter derfor, skal håndteres gennem korrekt uddannelse på indlægssedlen og produktets produktresumé efter bestemmelserne i den europæiske retningslinje i forhold til afsnittet "Særlige advarsler: vigtig information om nogle af hjælpestofferne i lægemidlet X". Disse vigtige oplysninger vil tillade både lægen og patienten at anvende den tilsvarende medicin med bevidsthed og ro.








.jpg)