Hvad er Bonviva?
Bonviva er et lægemiddel, der indeholder det aktive stof ibandronsyre. Det kommer i form af aflange hvide tabletter (150 mg) og en injektionsvæske, opløsning (3 mg).
Hvad bruges Bonviva til?
Bonviva er indiceret til behandling af osteoporose (en sygdom, der gør knoglerne skrøbelige) hos postmenopausale kvinder med risiko for knoglebrud. Nogle undersøgelser, dens effektivitet med hensyn til risikoen for brud på lårhalsen, er endnu ikke fastlagt.
Medicinen kan kun fås på recept.
Hvordan bruges Bonviva?
Bonviva kan administreres enten via munden som en tablet eller ved intravenøs injektion. I det første tilfælde er dosis en tablet om måneden. Tabletten bør altid tages efter en faste om natten, en time før mad eller drikke, undtagen vand, og med et glas rent vand. I timen efter tablet-indtagelse bør patienten ikke lægge sig ned. Til injektion er dosis 3 mg en gang hver tredje måned.
Patienter behandlet med Bonviva bør supplere deres kost med D -vitamin og calcium, hvis madindtaget er utilstrækkeligt. Bonviva anbefales ikke til patienter med alvorlige nyreproblemer.
Hvordan fungerer Bonviva?
Osteoporose opstår, når der ikke produceres tilstrækkelig ny knogle til at erstatte det, der forbruges naturligt. Knoglerne bliver gradvist tyndere og mere skrøbelige og mere tilbøjelige til at bryde. Osteoporose er mere almindelig hos postmenopausale kvinder, når niveauerne af det kvindelige hormon østrogen. Ibandronsyre, den aktive stof i Bonviva, er et bisphosphonat. Det hæmmer virkningen af osteoklaster, kroppens celler, der er ansvarlige for nedbrydning af knoglevæv, og reducerer dermed knogletab.
Hvordan er Bonviva blevet undersøgt?
Bonviva er blevet undersøgt i tre hovedundersøgelser med kvinder med osteoporose. I den første undersøgelse blev Bonviva 2,5 mg tabletter én gang dagligt sammenlignet med placebo (en dummy -behandling) hos cirka 3.000 kvinder, og antallet af brud rapporteret af patienter over tre år blev observeret.
I de to andre undersøgelser blev månedlige 150 mg tabletter (hos 1.609 patienter) og injektioner (hos 1.395 patienter) sammenlignet med 2,5 mg daglige tabletter. Undersøgelserne så på ændringen i knogletæthed i rygsøjlen og hoften over to år.
Det bemærkes, at de 2,5 mg daglige tabletter, der anvendes i undersøgelserne, ikke længere er godkendte.
Hvilken fordel har Bonviva vist under undersøgelserne?
I den første undersøgelse reducerede Bonviva 2,5 mg daglig tabletterapi risikoen for vertebrale frakturer med 62% sammenlignet med placebo.
De to andre undersøgelser viste, at de 150 mg månedlige tabletter og injektioner var mere effektive end de 2,5 mg daglige tabletter til at øge knogletætheden i rygsøjlen og hoften. Over to år steg knogletætheden i rygsøjlen med 7% med månedlige tabletter og 6% med injektioner, sammenlignet med 5% med daglige tabletter. Hoftebenstæthed steg med 4%. Med månedlige tabletter og 3% med injektioner mod 2% med daglige tabletter.
Hvilken risiko er der forbundet med Bonviva?
De mest almindelige bivirkninger (ses hos 1 til 10 patienter ud af 100) er gastritis (mavebetændelse), diarré, mavesmerter, dyspepsi (fordøjelsesbesvær), kvalme, influenzalignende symptomer, træthed, muskuloskeletale smerter (smerter i muskler og knogler ), artralgi (ledsmerter), myalgi (muskelsmerter) og stivhed i bevægeapparatet. Forstoppelse, hovedpine og rygsmerter ses også hos 1 til 10 ud af 100 patienter til injektionen. Se den fulde liste over bivirkninger rapporteret med Bonviva i indlægssedlen.
Bonviva må ikke bruges til personer, der er overfølsomme (allergiske) over for ibandronsyre eller et af de øvrige indholdsstoffer.
Det må ikke gives til personer med hypokalcæmi (med lavt calciumindhold i blodet).
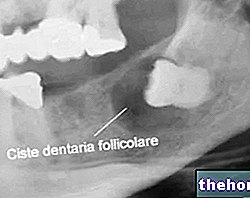
Behandling med Bonviva kan være forbundet med osteonekrose i kæben (sammenbrud af knogle i kæben).
Der skal udvises forsigtighed ved administration af lægemidlet til patienter med igangværende tandbehandling.
Hvorfor er Bonviva blevet godkendt?
Udvalget for Lægemidler til Mennesker (CHMP) besluttede, at fordelene ved Bonviva er større end risiciene ved behandling af osteoporose hos postmenopausale kvinder med øget risiko for brud. Udvalget anbefalede udstedelse af markedsføringstilladelse.
Lær mere om Bonviva
Den 23. februar 2004 tildelte Europa -Kommissionen Roche Registration Limited en "markedsføringstilladelse" for Bonviva, der er gyldig i hele EU. "Markedsføringstilladelsen" blev fornyet den 23. februar 2009.
For den fulde version af Bonvivas EPAR klik her.
Sidste opdatering af denne oversigt: 02-2009.
Oplysningerne om Bonviva - ibandronsyre offentliggjort på denne side kan være forældede eller ufuldstændige. For en korrekt brug af disse oplysninger, se siden Ansvarsfraskrivelse og nyttige oplysninger.